
科目: 来源: 题型:
【题目】上海磁悬浮铁路是世界上第一条投入运营的商业磁悬浮铁路。磁悬浮的核心技术是利用超导体的反磁性。以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Ox。现欲合成0.5mol此高温超导物质,理论上需取Y2O3、BaCO3和CuO的物质的量(mol)分别为( )
A.0.25、0.50、0.50B.0.50、1.00、1.50
C.0.25、1.00、1.50D.1.00、0.25、0.17
查看答案和解析>>
科目: 来源: 题型:
【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质:
)等产品。下表列出了有关物质的部分物理性质:
名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 (d水=1g·cm-3) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体,易燃、易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶; 酸性:苯甲酸>醋酸
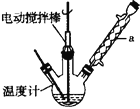
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作溶剂不参加反应)和2mL甲苯,搅拌升温至70℃ ,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。请回答下列问题:
(1)装置a的名称是 ________,主要作用是 ________;三颈瓶中发生反应的化学方程式为 ________,此反应的原子利用率理论上可达 ________(保留四位有效数字)。
(2)经测定,反应温度过高时,苯甲醛的产量有所减少,可能的原因是 ________。
(3)反应完毕后,反应混合液经过自然冷却至室温后,还应经过 ________、 ________
(填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是 ________ (按步骤顺序填字母)。
a.对混合液进行分液 b.与适量碳酸氢钠溶液混合振荡
c.过滤、洗涤、干燥 d.水层中加入盐酸调节pH=2
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取1.500g产品,溶于乙醇配成100mL溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol·L-1 KOH标准溶液滴定,到达滴定终点时消耗KOH溶液20.00mL。产品中苯甲酸的质量分数为 ________ (保留四位有效数字)。
③下列情况会使测定结果偏低的是 ________ (填字母)。
A.滴定终点时仰视读取耗碱量
B.锥形瓶洗净后还留有蒸馏水
C.配置KOH标准溶液时俯视定容
D.碱式滴定管滴定前有气泡,滴定终点时气泡消失
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是以实验为基础的学科。
(1)下列有关实验叙述正确的是________(填序号)。
a.试管、烧杯均可用于给液体、固体加热
b.使食盐水中NaCl结晶析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥三角
c.用铁坩埚灼烧烧碱
d.分液时,下层液体先从分液漏斗下口放出,换一个接收容器,再将上层液体从分液漏斗下口放出
e.用托盘天平称取25.20g氯化钠
f.取用金属钠或钾时,没用完的钠或钾要放回原瓶
(2)实验室用密度为1.25g/mL,质量分数为36.5%的浓盐酸配制240mL 0.1mol/L的盐酸,应量取浓盐酸体积________mL。使用的仪器除玻璃棒、烧杯、量筒外,还需要_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】水蒸气通过的灼热的焦炭后,流出气体的主要成分是 CO 和 H2,还有 CO2和水蒸气等。现利用下图中提供实验装置,证明上述混合气体中有CO 和 H2。(A中加热装置在图中略去)回答下列问题:
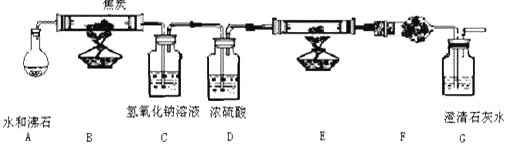
(1) C装置的用途是____________
(2)仪器 E 中需加入的试剂是_____________
(3)仪器 F 中需加入的试剂是:______,其目的是_________________
(4)装置F和G的位置能否颠倒_____,(填“能”或“否”)理由是____________________
(5)能证明混合气中含有 CO 的实验现象是________________________
(6)有人认为该实验装置存在一个缺陷,你认为这个缺陷是___________
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列说法正确的是
A. 1mol·L-1的Ca(ClO)2溶液中含Ca2+数目为NA
B. 22.4L Cl2分别与足量的Cu、Fe完全反应转移电子数分别为2NA、3NA
C. 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D. 1mol -OH与1mol OH-所含电子数均为9NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物的结构简式如图所示, 下列说法中不正确的是( )

A. 1mol该有机物和过量的金属钠反应最多可以生成1.5 molH2
B. 该有机物消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
C. 可以用酸性KMnO4溶液检验其中的碳碳双键
D. 该有机物能够在催化剂作用下发生酯化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.22.4LN2中一定含有6.02×1023个氮分子
B.1molCCl4在标准状况下的体积是22.4L
C.在常温常压下,20mLNH3与60mLO2所含的分子个数比为1:3
D.将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质变化和分类的说法正确的是( )
A. 胆矾、冰水混合物、四氧化三铁都不是混合物
B. 电解熔融态的Al2O3、12C转化为14C都属于化学变化
C. 葡萄糖溶液和淀粉溶液的本质区别是能否产生丁达尔效应
D. SiO2、NO2、Al2O3都属于酸性氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用某化合物X(两种短周期元素组成的纯净物)进行了如下实验:

实验步骤②中还观测到生成黑色固体和无色无味气体,生成的溶液可作为建筑行业的一种黏合剂。
请回答:
(1)X的化学式是____,步骤①的离子方程式是___。
(2)步骤②的化学方程式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有下列几种有机物: ①CH3COOCH3 ②CH2=CHCH2Cl ③![]() ④CH2=CH-COOCH3 ⑤ CH2=CH-CHO
④CH2=CH-COOCH3 ⑤ CH2=CH-CHO
其中既能发生水解反应,又能发生加成反应的是( )
A. ①④B. ①③④C. ②⑤D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com