
科目: 来源: 题型:
【题目】下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。说法正确的是( )
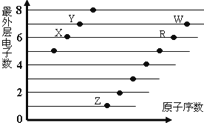
A. X与W形成的化合物中只有共价键
B. X与Z形成的化合物中只有离子键
C. 元素的非金属性:X>R>W
D. 简单离子的半径:W>R>X
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组在实验室用下图所示装置快速制取氨并验证氨的某些性质,同时收集少量纯净的氮气,请回答。
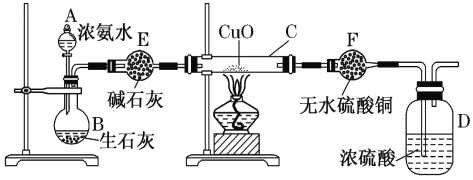
(1)写出用生石灰和浓氨水反应制氨的化学方程式____________________________,解释放出NH3的原因_______________________________________________________。
(2)实验进行一段时间,观察到硬质玻璃管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管口处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃管内发生反应的化学方程式:___________________________________,
(3)在最后的出气导管口处收集干燥、纯净的氮气,收集方法是________。
A.排空气法 B.排水法 C.用气囊收集
(4) E中的碱石灰________(填“能”或“不能”)换成CaCl2。
(5) 在浓硝酸中放入铜片,若铜有剩余,开始反应的化学方程式为 __________________,
(6) 若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生NO和NO2 气体V L(标准状况),将产生的气体与一定量的氧气混合恰好被一定量的NaOH溶液吸收生成硝酸盐,则通入氧气的物质的量是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有一混合物的水溶液,只可能含有以下离子中的若干种:K+、![]() 、Cl-、Mg2+、Ba2+、
、Cl-、Mg2+、Ba2+、![]() 、
、![]() ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.08mol气体;
第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知, ![]() +OH-
+OH-![]() H2O+NH3↑)
H2O+NH3↑)
根据上述实验,回答以下问题。
(1)由第一份进行的实验推断该混合物是否一定含有Cl-?____________(答是或否)。
(2)由第二份进行的实验得知混合物中应含有____________(填离子符号),其物质的量浓度为____________。
(3)由第三份进行的实验可知12.54g沉淀的成分为____________。
(4)综合上述实验,你认为以下结论正确的是(______)
A.该混合液中一定含有K+、![]() 、
、![]() 、
、![]() ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04mol
B.该混合液中一定含有![]() 、
、![]() 、
、![]() ,可能含K+、Cl-
,可能含K+、Cl-
C.该混合液中一定含有![]() 、
、![]() 、
、![]() ,可能含Mg2+、K+、Cl-
,可能含Mg2+、K+、Cl-
D.该混合液中一定含有![]() 、
、![]() ,可能含Mg2+、K+、Cl-
,可能含Mg2+、K+、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A. 氯水使有色布条褪色,说明氯水中含有![]()
B. 向氯水中加入![]() 溶液产生白色沉淀,说明氯水中含有
溶液产生白色沉淀,说明氯水中含有![]()
C. 向氯水中加入![]() 粉末,有气泡产生,说明氯水中含有
粉末,有气泡产生,说明氯水中含有![]()
D. 向氢氧化钠溶液中滴加氯水,溶液黄绿色消失,说明氯水中含有![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是______________。(填化学式)
(2)该反应中,发生还原反应的过程是________→________。(填化学式)
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:____________________________________________________________。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________。
(5)反应8NH3+3Cl2=6NH4Cl+N2中,氧化剂与还原剂的物质的量之比是_________。
(6)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列关于充电电池、干电池的叙述合理的是___________。
①干电池可以实现化学能向电能的转化和电能向化学能的转化
②锌锰干电池长时间连续使用时内装糊状物可能流出腐蚀电器
③充电电池可以无限制地反复放电、充电
④充电是使放电时的氧化还原反应逆向进行
(2)铅蓄电池中,正极材料为PbO2,负极材料为Pb,放电时其负极反应式为_____________。
(3)原电池在NaOH溶液介质中,铝为负极,其负极反应式为_______________。
(4)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图。b电极是_____极,请写出负极的电极反应方程式:___________________________。
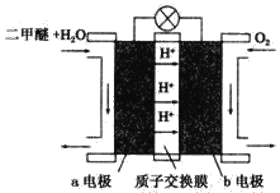
查看答案和解析>>
科目: 来源: 题型:
【题目】2018年8月“非洲猪瘟”首次传入我国,已从最初的单点爆发演变为区域性爆发。(其病毒结构如图所示)疫情的爆发和蔓延对全国生猪市场产生了重大影响,今年5月份以来各地猪肉价格飞涨。中国科学家们正在努力研制疫苗,以帮助保护全世界的猪肉供应。9月10日,中国农业科学院院长、中国工程院院士唐华俊在中国农业科学院非洲猪瘟防控与生猪复养技术推介会上介绍,我国非洲猪瘟疫苗研制在今年4月实验室研究工作取得成功后,疫苗研发工作又取得了新的重要进展。我国非洲猪瘟疫苗将进入临床试验阶段。下列有关说法中错误的是( )
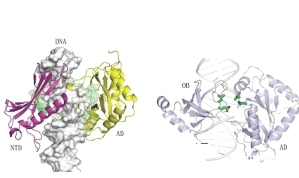
A. 疫苗一般应冷藏存放,以避免蛋白质变性
B. 非洲猪瘟迅速在全国蔓延,有可能通过空气传播
C. 非洲猪瘟病毒DNA分子内存在氢键,氢键是一种共价键
D. 非洲猪瘟病毒,可以通过高温方式进行杀灭
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签,

试根据有关数据回答下列问题:
(1)该浓盐酸的物质的量浓度为___________mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是__________。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某实验需要480 mL物质的量浓度为0.3 mol/L稀盐酸。某学生用上述浓盐酸和蒸馏水进行配制。
①该学生需要用量筒量取___________ mL上述浓盐酸进行配制。该实验中玻璃棒的作用有_________________________________。
②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)_________________。
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填 “偏高”或“偏低”或“无影响”)。
用量筒量取浓盐酸时俯视观察凹液面_________________。
溶液注入容量瓶前没有恢复到室温就进行定容_________________。
容量瓶用水洗完后,用稀盐酸润洗,且没有干燥就直接使用_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)在标准状况下,V L H2 中含有 N 个氢分子,则阿伏加德罗常数为_____mol-1
(2)8.5 g氢氧根离子含有的电子数目为________。
(3)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的相对分子质量为_________。
(4)标准状况下,8.96L的CH4和CO的混合气体,该混合气体对氢气的相对密度是9.5,则混合气体平均摩尔质量为____________,混合气体中CH4与CO的体积比为____。
(5)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________mol/L。(用带字母的表达式回答)
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为_____________
(2)W与Y 可形成化合物W2Y,该化合物的电子式为________________________。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为_________________________。Y的最高价氧化物是否满足8电子稳定结构______________(填是.否)
(4)比较Y、Z气态氢化物的稳定性由大到小的顺序是________________(用分子式表示)。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是
____________________________________________________。(用离子符号表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com