
科目: 来源: 题型:
【题目】实验室欲用氢氧化钠固体配制1.0mol·L-1的氢氧化钠溶液240mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为___。必须用到的玻璃仪器有烧杯、胶头滴管、___。
(2)某同学欲称量氢氧化钠的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为___g,要完成本实验该同学应称出__g氢氧化钠。
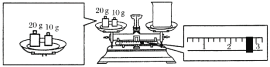
(3)如图是该同学转移溶液的示意图,图中有两处错误,请写出:
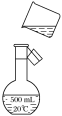
①____;
②____。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是__(填字母)。
A.所用氢氧化钠已经潮解
B.溶液未冷却至室温就注入容量瓶中定容
C.在配置过程中未洗涤烧杯和玻璃棒
D.定容时,俯视容量瓶刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】已知2NaHCO3![]() Na2CO3 + H2O+CO2 ,现把14.8g Na2CO310H2O和NaHCO3组成的固体混合物溶于水配成100mL溶液,其中c(Na+)=1.2molL﹣1,若把等质量的固体混合物加热至恒重,残留固体质量是( )
Na2CO3 + H2O+CO2 ,现把14.8g Na2CO310H2O和NaHCO3组成的固体混合物溶于水配成100mL溶液,其中c(Na+)=1.2molL﹣1,若把等质量的固体混合物加热至恒重,残留固体质量是( )
A. 6.36gB. 3.18gC. 4.22gD. 5.28g
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应在日常生活和生产中应用广泛,结合相关知识回答下列问题:
I.根据反应①~③,回答下列问题:
①Cl2+2KI=2KCl+I2 ②2FeCl2+Cl2=2FeCl3 ③2FeCl3+2HI=2FeCl2+2HCl+I2
(1)反应②的反应类型为___(填字母)。
A.置换反应 B.复分解反应 C.分解反应 D.氧化还原反应
(2)对于反应③,氧化产物是___,还原产物是___。
(3)根据上述三个反应可判断出Cl-、I-、Fe2+三种物质的还原性由强到弱顺序为___。
II.实验室可以用 KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:__KMnO4+__HCl(浓)-__KCl+__MnCl2+__Cl2↑+__H2O,回答下列问题:
(1)请配平上述化学方程式。___
(2)浓盐酸在反应中表现的性质是___。
(3)该反应中氧化剂和还原剂的物质的量之比为___。
III.饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,请回答下列问题:
(1)上述反应中,被还原的物质是___。
(2)用双线桥标出反应中电子转移的方向和数目。___
(3)上述反应中若标准状况下产生11.2L气体,则转移电子的数目为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对有机物![]() 的叙述中,不正确的是( )
的叙述中,不正确的是( )
A. 它不能使溴水褪色,也不能使酸性KMnO4溶液褪色
B. 在FeBr3作催化剂时与Br2发生取代反应可生成三种一溴代物
C. 在一定条件下可发生加成反应
D. 一定条件下可以和浓硝酸、浓硫酸的混合物发生硝化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色溶液中可能含有Na+、Ba2+、Cu2+、CO32-、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
(1)原溶液中一定含有的离子是________,一定不含有的离子是________,不能确定是否含有的离子是________。
(2)②中反应的离子方程式为___________________。
(3)若另取10mL①的溶液于锥形瓶中,然后向此溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。
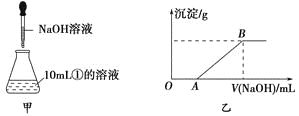
①OA段反应的离子方程式为_____________________。
②AB段反应的离子方程式为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L
B. 从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C. 配制500mL 0.1mol/L的CuSO4溶液,需8.0g硫酸铜固体
D. 0.1mol/L MgCl2溶液中Cl-物质的量为0.2mol
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关铜的化合物说法正确的是( )
A. 根据铁比铜金属性强,在实际应用中可用FeCl3腐蚀Cu刻制印刷电路板
B. CuSO4溶液与H2S溶液反应的离子方程式为:Cu2++S2-![]() CuS↓
CuS↓
C. 用稀盐酸除去铜锈的离子方程式为CuO+2H+===Cu2++H2O
D. 化学反应:CuO+CO![]() Cu+CO2的实验现象为黑色固体变成红色固体
Cu+CO2的实验现象为黑色固体变成红色固体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A. 因为二氧化硫具有漂白性,所以它能使品红溶液、溴水、高锰酸钾溶液褪色
B. 100mL0.5mol/LH2O2溶液与足量SO2完全反应,转移的电子数为0.1NA
C. 二氧化硫、Cl2以及活性炭都能使红墨水褪色,其原理不同
D. 等物质的量的二氧化硫和氯气相遇在溶液中具有更强的漂白能力
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。(已知:NH4HCO3=NH3↑+CO2↑+H2O)

(1)操作②为什么不用硝酸钡溶液,其理由是_______________________________;
(2)进行操作②后,如何判断SO42-已除尽,方法是___________________________;
(3)操作③的目的是____________,其中涉及到的离子方程式是_______________;
(4)往滤液中加入盐酸的离子方程式是__________________________________;
(5)NH4HCO3在水溶液中的电离方程式_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )
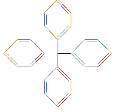
A. 分子式为C25H20
B. 所有碳原子不可能都在同一平面上
C. 完全燃烧生成CO2与H2O的物质的量之比为5∶2
D. 此物质不属于芳香烃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com