
科目: 来源: 题型:
【题目】下图为电解饱和食盐水的实验装置。据此,下列叙述不正确的是 ( )
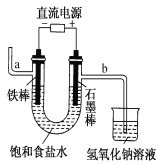
A.装置中a管能产生氢气
B.b管导出的是能使湿润的淀粉碘化钾试纸变蓝的气体
C.在石墨棒电极区域有NaOH生成
D.以电解饱和食盐水为基础制取氯气等产品的工业称为“氯碱工业”
查看答案和解析>>
科目: 来源: 题型:
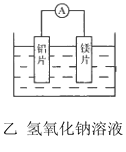
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol L-1的H2SO4溶液中,乙同学将电极放入6mol L-1NaOH的溶液中,如图所示。
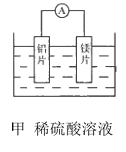
(1)写出甲电池中正极的电极反应式:________.
(2)写出乙电池中总反应的离子方程式:_________.
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出______(填写元素符号,下同)的金属活动性更强,而乙会判断出___的金属活动性更强。
(4)由此实验,可得到如下哪些正确结论(______)
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属活动性不一定比铝的金属活动性强
C.该实验说明金属活动性顺序已过时,已没有使用价值
D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)将5.1g镁铝合金溶于60 mL5.0 mol L-1H2SO4溶液中,完全溶解后再加入65mL10.0mol L-1的NaOH溶液,得到沉淀质量为9.7g,继续滴加NaOH溶液时沉淀会减少。
①当加入____mLNaOH溶液时,可使溶解在硫酸中的Mg2+和Al3+恰好完全沉淀。
②计算合金溶于硫酸时所产生的氢气在标准状况下为_____L
查看答案和解析>>
科目: 来源: 题型:
【题目】磷及其化合物有重要的用途,回答下列问题:
(1)工业上将磷酸钙、石英砂和碳粉混和在电弧炉中焙烧来制取白磷,配平方程式:
______![]() +______
+______![]() +______
+______![]()
![]() ______
______![]() +______
+______![]() +______
+______![]() 。
。
(2)白磷易自燃,保存的方法是__________________,白磷有毒,皮肤上沾有少量的白磷,可以用硫酸铜溶液处理,发生的反应是:![]() ,该反应的氧化剂是________________________(填化学式)。
,该反应的氧化剂是________________________(填化学式)。
(3)![]() 俗称为膦,电子式为:________________________,沸点比较:
俗称为膦,电子式为:________________________,沸点比较:![]() __________
__________![]() (填”“高于”或“低于”)。
(填”“高于”或“低于”)。
(4)P2O5是常见的气体干燥剂,下列气体能用它干燥的是_______________。
A ![]() B
B![]() C SO2 D CO2
C SO2 D CO2
也可以发生反应:![]() ,该反应中
,该反应中![]() 表现的性质是_________。
表现的性质是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。
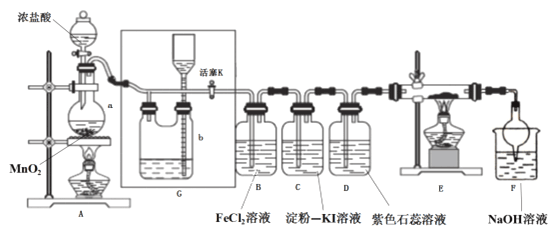
(1)A中发生反应的化学反应方程式为________
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯,回答下列问题:
①在装置C、D中能看到的实验现象分别是 ________ 、________;
②在装置E的硬质玻璃管内盛有碳粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为_________;
③装置F中球形干燥管的作用是__________;
(3)储气瓶b内盛放的试剂是___________;
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如下图所示的三套实验装置:
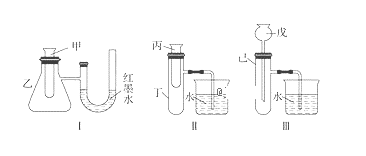
(1)上述3个装置中,不能验证“铜与浓硝酸的反应是吸热反应还是放热反应”的装置是_____(填装置序号)。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管中加入适量Ba(OH)2溶液与稀硫酸,U形管中可观察到的现象是___________。说明该反应属于______(填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在丙试管中进行)。
若观察到烧杯中产生气泡,则说明M溶于水___(填“一定是放热反应”、“一定是吸热反应”或“可能是放热反应”),理由是_____。
(4)至少有两种实验方法能验证超氧化钾与水的反应(4KO2+2H2O![]() 4KOH+3O2↑)是放热反应还是吸热反应。
4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择装置______(填装置序号)进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是_____(填“吸热”或“放热”)反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为1 NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C. 常温常压下,1 NA 个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。请回答:

(1)写出铜和浓硫酸反应的化学方程式:_____________。
(2)装置D中试管口放置的棉花中浸有NaOH溶液,其作用是______。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是__,B中应放置的液体是____(填序号)。
A.水 B.酸性KMnO4溶液 C.浓溴水 D.饱和NaHSO3溶液
(4)取一定质量的铜片和一定体积浓度为18.4 mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中铜和硫酸都有剩余。若想使烧瓶中剩余的铜片溶解,可向烧瓶中加入下列试剂中的____(填序号)。
A.HNO3 B.NaNO3 C.NaHCO3 D.Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E是五种由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的不同的阴阳离子组成,且均易溶于水的物质,分别取它们的水溶液进行实验,现象如下:
中的不同的阴阳离子组成,且均易溶于水的物质,分别取它们的水溶液进行实验,现象如下:
①分别向五种溶液中加入稀盐酸,C、E均有气泡产生,且E的液面上出现红棕色气体
②C、D混合时,剧烈反应,同时产生白色沉淀和大量气体;A、C混合时,仅有刺激性气味气体产生
③少量A与D混合时,产生白色沉淀,过量A与D混合时,无现象
回答下列问题:
(1)实验①,C中产生的气体是________________(填化学式)。
(2)物质A、D的化学式分别是_____________,________________。
(3)C、D混合时发生反应的离子方程式是__________________________。
(4)将A、E的溶液在烧杯中混合,其现象是________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。
下面是某些短周期元素的x值:
元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值变化规律,确定Mg的x值范围:____<x(Mg)< _____。
(2)推测x值与原子半径的关系是____;根据短周期元素的x值变化特点,体现了元素性质的________变化规律。
(3)某有机化合物结构式为![]() ,其中S—N中,你认为共用电子对偏向谁?__(写原子名称)。
,其中S—N中,你认为共用电子对偏向谁?__(写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的差值(Δx),当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是______。
(5)预测元素周期表中,x值最小的元素位置:_________
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化法是测定葡萄酒中SO2含量的常用方法,其原理是在低温条件下,用过量的过氧化氢溶液氧化从样品中挥发出的SO2,再用碱标准溶液滴定生成的酸。
按图组装好装置,检查装置气密性,由c向A中注入20.00mL葡萄酒,10mL25%磷酸溶液,C、D中分别注入20.00mL,5.00mL稀H2O2溶液。回答下列问题:
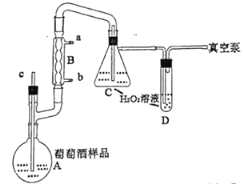
(1)装置B的名称是___________,冷凝水从___________(填“a”或“b”)口进入。
(2)C中发生反应的化学方程式为___________,使用D的目的是___________________。
(3)真空泵抽气速率不宜过快,原因是______________________。
(4)抽气十分钟后,合并C、D中的溶液,加入指示剂,用浓度为c(单位为![]() )的NaOH标准溶液滴定,消耗
)的NaOH标准溶液滴定,消耗![]() ;另取装置,向A中注人20.00mL蒸馏水,按同样的方法做空白实验,消耗NaOH溶液
;另取装置,向A中注人20.00mL蒸馏水,按同样的方法做空白实验,消耗NaOH溶液![]() ,则该葡萄酒中SO2的含量为___________mg/L.(用c、
,则该葡萄酒中SO2的含量为___________mg/L.(用c、![]() 、
、![]() 表示)
表示)
(5)葡萄酒中含有的SO2的作用是______________________。(答一点)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com