
科目: 来源: 题型:
【题目】普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型)。

下列关于普伐他汀的性质描述正确的是 ( )
A. 能与FeCl3溶液发生显色反应
B. 该物质的分子式为C23H38O7
C. 能发生加成、取代、消去反应,能使酸性KMnO4溶液褪色
D. 1mol该物质最多可与1molNaOH反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某2.0L硫酸溶液中含有1.0molH2SO4。试计算:
(1)溶液中H2SO4的物质的量浓度。___________
(2)向上述溶液中加入足量的铁粉,产生气体的体积(标准状况下)。____________
(3)假设反应前后溶液体积不变,则所得溶液中FeSO4的物质的量浓度。____________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应的产物中,存在同分异构体的是( )
A. CH3CH2CH2Br在碱性溶液中水解
B. 甲苯在催化剂作用下与Cl2发生苯环上的取代反应
C. ![]() 与NaOH的醇溶液共热反应
与NaOH的醇溶液共热反应
D. ![]() 在催化剂存在下与H2完全加成
在催化剂存在下与H2完全加成
查看答案和解析>>
科目: 来源: 题型:
【题目】甲胺(CH3NH2)是一种一元弱碱,其电离方程式为:CH3NH2 + H2O ![]() CH3NH3+ + OH-。常温下,向20.0 mL 0.10 mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是
CH3NH3+ + OH-。常温下,向20.0 mL 0.10 mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是
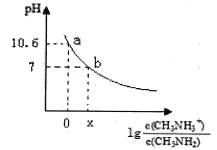
A. b点对应加入盐酸的体积V<20.00mL
B. 常温下,根据a点可知甲胺的电离平衡常数Kb=10 -3.4
C. b点可能存在关系:c(Cl-) > c(CH3NH3+) > c(H+) = c(OH-)
D. V=20.00mL时,溶液呈弱酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)![]() CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )

A. 该反应的ΔH=+91 kJ·mol-1
B. 加入催化剂,该反应的ΔH变小
C. 反应物的总能量小于生成物的总能量
D. 如果该反应生成液态CH3OH,则ΔH减小
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:![]() ,下列有机物能够合成
,下列有机物能够合成![]() 的组合是( )
的组合是( )
①1,3-丁二烯 ②2-甲基-l,3-丁二烯 ③1,3-戊二烯 ④2,3-二甲基-l,3-丁二烯
⑤2,3-二甲基-l,3-戊二烯 ⑥乙炔 ⑦丙炔 ⑧2-丁炔
A. ①、⑦及④、⑧ B. ⑤、⑥及③、⑧
C. ①、③及②、⑧ D. ②、⑧及④、⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】有甲、乙两种物质:

(1)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
![]()
其中反应I的反应类型是___________,反应II的条件是_______________,反应III的化学方程式为___________________________________(不需注明反应条件)。
(2)下列物质不能与乙反应的是 (选填序号)。
a.金属钠 b.溴水 c.碳酸钠溶液 d.乙酸
(3)乙有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体结构简式 。
a.苯环上的一氯代物有两种
b.遇FeCl3溶液显示紫色
查看答案和解析>>
科目: 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料.工业上提取铝的工艺流程如下:
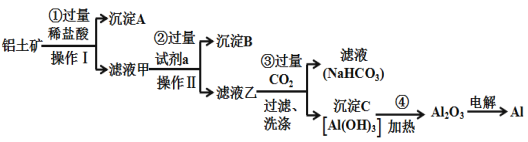
(1)沉淀A的化学式是_________,试剂a的化学式为______________;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为______________________________________;
(3)Al2O3中所含的化学键的类型为___________________;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其阳极反应式为______________________________;
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是(___________)
a MgO b V2O 5 c Fe3O4 d MnO2
查看答案和解析>>
科目: 来源: 题型:
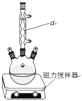
【题目】二苯基乙二酮常用作医药中间体及紫外线固化剂,可由二苯基羟乙酮氧化制得,相关物质的物理参数、化学方程式及装置图(加热和夹持装置已略去)如下:
相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 | ||
二苯基羟乙酮 | 212 | 133 | 344 | 1.310 | 不溶于冷水,溶于乙醇 | |
二苯基乙二酮 | 210 | 97 | 348 | 1.084 | 不溶于水,能溶于乙醇 |
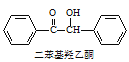 +2FeCl3
+2FeCl3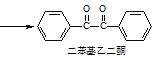 +2FeCl2+2HCl
+2FeCl2+2HCl
在反应装置中,加入10mL冰醋酸、5.50g FeCl3固体、10mL水及少量碎瓷片,加热至沸腾,停止加热,待沸腾平息后加入2.12g二苯基羟乙酮,继续加热回流至二苯基羟乙酮完全反应。反应结束后加水煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯,得到1.80g产品。
重结晶过程如下:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答以下问题:
(1)装置图中仪器a的名称是____,其作用是____。
(2)加入碎瓷片的作用是____。若加热后发现未加碎瓷片,应采取的正确方法是___。
(3)实验中可采用薄层色谱跟踪反应进程,其原理和操作与纸上层析类同,通过观察薄层色谱展开后的斑点(在实验条件下,只有二苯基羟乙酮和二苯基乙二酮能够产生斑点)判断样品中的成分。如图分别为加入二苯基羟乙酮后反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样,薄层色谱展开后的斑点:

该实验条件下加热____后可认为反应结束。
A.15min B.30min C.45min D.60min
(4)上述重结晶过程中,____(填步骤名称)操作除去了不溶性杂质。
(5)在重结晶过程中,不可选用明火直接加热,原因是____。
(6)不选择蒸馏的方法提纯二苯基乙二酮粗产品的原因是_____。
(7)本实验的产率是____%。(保留3位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com