
科目: 来源: 题型:
【题目】某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含![]() 、
、![]() 及Pb、Ca等元素)和轧钢废酸液制取工业级碳酸锰(
及Pb、Ca等元素)和轧钢废酸液制取工业级碳酸锰(![]() ),其流程如下:
),其流程如下:
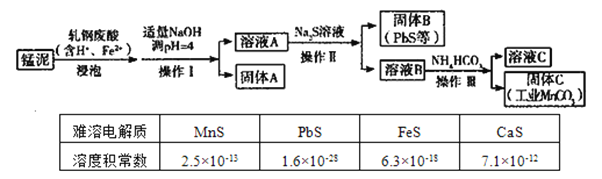
(1)操作Ⅰ、操作Ⅱ、操作Ⅲ的名称是____。
(2)轧钢废酸中![]() 的作用是_________________。
的作用是_________________。
(3)固体A是_____________。(填化学式,下同)
(4)溶液B中含有____阳离子,通过表格中数据简单说明固体B与以上离子分离的原因_____。
(5)若固体C中不含![]() ,则溶液C中
,则溶液C中![]() __。(已知:
__。(已知:![]()
![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】欲测定某NaOH溶液的物质的量浓度,可用0.100mol/L的HCl标准溶液进行中和滴定(用甲基橙作指示剂)。 请回答下列问题:
(1)滴定前,用移液管量取待测NaOH溶液于 _____中( 填仪器名称),并加入2~3滴指示剂;
(2)盛装标准盐酸的仪器名称为 _____ ;
(3)如何判断滴定终点(需写出颜色变化) __________ ;
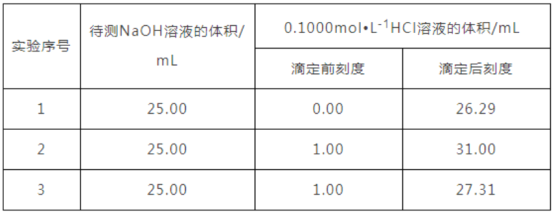
某学生做了三组平行实验,数据记录如下:
选取下述合理数据,算出待测NaOH溶液的物质的量浓度为 _______________;
(保留四位有效数字)
(4)下列哪些操作会使测定结果偏低____________
a.反应容器用蒸馏水洗净后,未用待测液润洗
b.滴定前,平视读数;滴定后,仰视读数
c.滴定前,尖嘴无气泡;滴定后,尖嘴出现气泡
查看答案和解析>>
科目: 来源: 题型:
【题目】10℃时加热![]() 饱和溶液,测得该溶液的pH发生如下变化:
饱和溶液,测得该溶液的pH发生如下变化:

(1)![]() 饱和溶液中存在三个平衡关系,写出三个平衡表达式 :________;_______;______。
饱和溶液中存在三个平衡关系,写出三个平衡表达式 :________;_______;______。
(2)甲同学认为,该溶液的pH升高的原因是![]() 的水解程度增大,故碱性增强。乙同学认为,溶液的pH升高的原因是
的水解程度增大,故碱性增强。乙同学认为,溶液的pH升高的原因是![]() 受热分解,生成了
受热分解,生成了![]() ,并推断
,并推断![]() 的水解程度________(填“大于”或“小于”)
的水解程度________(填“大于”或“小于”)![]() 。丙同学认为将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 ____________(填“甲”或“乙”)判断正确。
。丙同学认为将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 ____________(填“甲”或“乙”)判断正确。
(3)丁同学向饱和![]() 溶液中加入饱和
溶液中加入饱和![]() 溶液,观察到有白色沉淀和无色气体,经检验该白色沉淀为碳酸钙沉淀,试利用沉淀溶解平衡表达式和K、Q关系分析产生该沉淀的原因 ____________。
溶液,观察到有白色沉淀和无色气体,经检验该白色沉淀为碳酸钙沉淀,试利用沉淀溶解平衡表达式和K、Q关系分析产生该沉淀的原因 ____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用离子方程式回答下列问题:
(1)泡沫灭火器中灭火原理(内装小苏打溶液和![]() 溶液____________。
溶液____________。
(2)已知AgCl为难溶于水和酸的白色固体,![]() 为难溶于水和酸的黑色固体。向AgCl的悬浊液中加入足量的
为难溶于水和酸的黑色固体。向AgCl的悬浊液中加入足量的![]() 溶液并振荡,白色固体完全转化为黑色固体:________________。
溶液并振荡,白色固体完全转化为黑色固体:________________。
(3)③实验室配制![]() 溶液,溶解时先要加入少量的稀硫酸,其原因________;配制完毕后要加入少量铁屑,其目的是_____________。
溶液,溶解时先要加入少量的稀硫酸,其原因________;配制完毕后要加入少量铁屑,其目的是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我们祖先的四大发明之一黑火药的爆炸反应为:S+2KNO3+3C![]() A+N2↑+3CO2↑(已配平)。请回答下列问题:
A+N2↑+3CO2↑(已配平)。请回答下列问题:
(1)生成物固体A属于___________晶体,上述化学反应的氧化剂是__________(写化学式);
(2)硫元素在周期表中的位置为_________能说明氯的非金属性比硫强的实验是_______(任写一条即可);
(3)C原子最外层电子的电子排布式是_____,CCl4是一种常见的有机溶剂,写出其电子式_____,判断其属于_________(填“极性”、“非极性”)共价键_____分子(填“极性”或“非极性”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是( )
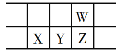
A.原子半径:W<X
B.Y单质是良好的半导体材料
C.气态氢化物热稳定性:W>Z
D.X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目: 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A是一种金属单质,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系:

(1)写出A、B、C、E的化学式:
A__________,B__________,C__________,E__________。
(2)写出E→F反应的化学方程式_________;写出B→D反应的化学方程式_________。
(3)F在空气中遇水蒸气产生白雾现象,这白雾实际上是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
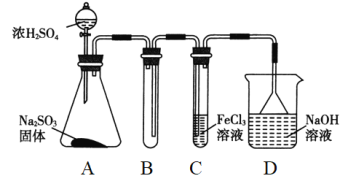
(1)通入足量SO2时C中观察到的现象是______________________。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:_______________________;
②请设计实验方案检验有Fe2+生成:_________________________;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法_____(填“合理”或“不合理”),理由是______。
(3)D装置中倒置漏斗的作用是__________________________。
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________(填字母)。
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,0.1mol·L-1 的 FeCl3 溶液呈___________性(填“酸”、“碱”或“中”),原因是___(请用离子方程式表示)。电子工业曾用 30%的 FeCl3溶液腐蚀敷有铜箔的绝缘板制印刷电路板,为了从使用过的废腐蚀液中回收铜,并重新得到 FeCl3 溶液,设计如下实验流程:
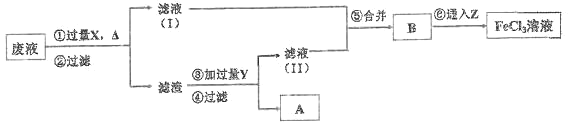
上述流程中,所加试剂的化学式为:X_____,Y_________,Z_____;第⑥步反应的离子方程 式为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com