
科目: 来源: 题型:
【题目】乙醇分子中不同化学键的表示,回答下列问题:
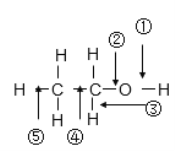
(1)乙醇与金属钠反应,___________键断裂
(2)将乙醇与浓硫酸的混合液,温度升高到170℃时,_________键断裂
(3)将乙醇与浓硫酸的混合液,温度升高到140℃时,_________键断裂
(4)在加热条件下,用铜作催化剂与氧气反应时,______断裂。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的有机产物,肯定是一种的是( )
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2—氯丁烷(![]() )与NaOH溶液共热发生反应
)与NaOH溶液共热发生反应
C. 甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D. 等物质的量的甲烷和氯气的混和气体长时间光照后的产物
查看答案和解析>>
科目: 来源: 题型:
【题目】已知3CuO+2NH3![]() 3Cu+N2+3H2O。下列判断正确的是
3Cu+N2+3H2O。下列判断正确的是
A.N元素的化合价降低B.NH3被还原
C.消耗0.3 mol CuO转移0.6 NA个电子D.CuO是还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是H2(g)与I2(g)反应生成HI(g)的能量示意图。由图可知

A.该反应是吸热反应
B.1 mol HI(g)分解吸收的热量为Q
C.热化学方程式:H2+I2![]() 2HI+Q
2HI+Q
D.反应物总能量高于生成物总能量
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 28g乙烯、丙烯的混合气体中所含原子数为6NA
B. 28g乙烯所含共用电子对数目为4NA
C. 标准状况下,11.2 L氯仿(CHCl3)所含分子数为0.5 NA
D. 78g苯中含有C—C键数目为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取乙烯的发生装置如图所示。下列说法正确的是

A.烧瓶中加入乙醇、浓硫酸和碎瓷片
B.反应温度控制在140℃
C.导出的气体中只有乙烯
D.可用向上排气法收集乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:
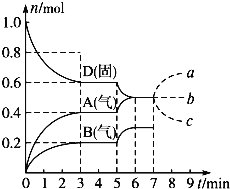
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为______mol/(L·min)。
(2)根据上图写出该反应的化学方程式________,该反应的平衡常数表达式为K=________。
(3)①第5min时,升高温度,A、B、D的物质的量变化如上图,则该反应的正反应是___(填“放热”或“吸热”)反应,反应的平衡常数______(填“增大”“减小”或“不变”,下同)。
②若在第7min时增加D的物质的量,A的物质的量变化正确的是____(用图中a、b、c的编号回答)。
查看答案和解析>>
科目: 来源: 题型:
【题目】仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置就能实现相应实验目的的是( )
选项 | A | B | C | D |
实验目的 | 除去KCl中少量的MnO2 | 用10mol·L-1的盐酸配制100mL0.1 mol·L-1的盐酸 | 用氯化钠溶液制备氯化钠晶体 | 除去CO2气体中的HCl |
实验仪器或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 |
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】肼(N2H4)是一种应用广泛的化工原料。工业上先合成氨气:N2(g)+3H2(g) ![]() 2NH3(g)+Q(Q>0),再进一步制备肼。完成下列填空:
2NH3(g)+Q(Q>0),再进一步制备肼。完成下列填空:

(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条件相同),则生产中适宜选择的催化剂是___(填“A”或“B”或“C”),理由是:________________。
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“无法确定”)
反应速率 | 平衡常数K | 氨的体积分数 | |
变化情况 | __ | ____ | ____ |
(3)肼可作为火箭燃料,4gN2H4(g)在NO2气体中燃烧生成氮气和气态水,放出71kJ的热量。写出该反应的化学方程式:________。
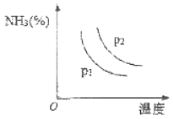
(4)氨主要用于生产化肥和硝酸。“十三五”期间,预计我国合成氨产量将保持稳中略增。下图是不同温度和不同压强下,反应达到平衡后,混合物中NH3含量(体积%)的变化情况,己知初始时n(N2):n(H2)=1:3。判断pl、p2压强的大小关系,pl___p2(选填“>”、“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】用Cl2生产含氯有机物时会产生HCl,利用反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)可实现氯的循环利用。完成下列填空:
2Cl2(g)+2H2O(g)可实现氯的循环利用。完成下列填空:
(1)上述反应若在固定体积的密闭容器中发生,能说明反应已达平衡的是_________(选填序号)。
a.2ν(HCl)正=ν(Cl2)逆 b.体系压强不再改变
c.混合气体密度不变 d.K=![]()
(2)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似。下列有关说法不正确的是___(选填序号)。
a.S2C12分子中有4对共用电子对 b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为-1价 d.S2C12分子中各原子均为8电子稳定结构。
(3)已知X2(g)+H2(g)![]() 2HX(g)+Q(X2表示Cl2、Br2)如图表示上述反应的平衡常数K与温度T的关系。
2HX(g)+Q(X2表示Cl2、Br2)如图表示上述反应的平衡常数K与温度T的关系。
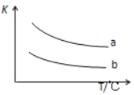
①Q表示X2(g)与H2(g)反应的反应热,Q____0(填“>”、“<”或“=”)。
②写出曲线b表示的平衡常数K的表达式,K=_________________(表达式中写物质的化学式)。
(4)向新制的氯水中加入少量下列物质,能增强溶液漂白能力的是(_______)
A.氯化钙 B.碳酸钙粉末 C.二氧化硫溶液 D.稀硫酸
(5)若向氯化银沉淀中逐渐滴加HBr,会看到白色沉淀逐渐变为淡黄色沉淀现象,请用溶解平衡原理解释此现象____。
(6)已知BBr3与BI3的空间构型是平面三角形结构,则它们是____分子(填极性或非极性),且BBr3的沸点低于BI3,原因是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com