
科目: 来源: 题型:
【题目】今有下列物质:①1molNH3②标准状况下11.2LN2③4℃时10mL水④标准状况下22.4LCH4原子数由多到少的顺序是( )
A.④③①②B.④②①③C.②④①③D.④①③②
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积均为1.0 L 的恒容密闭容器中发生反应:2A(g)![]() B(g)+C(g) ΔH
B(g)+C(g) ΔH
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
A(g) | B(g) | C(g) | ||
Ⅰ | 387 | 0. 20 | 0. 080 | 0. 080 |
Ⅱ | 387 | 0. 40 | ||
Ⅲ | 207 | 0. 20 | 0. 090 | 0. 090 |
下列说法不正确的是
A. 该反应的正反应为ΔH<0
B. 207℃,K=4
C. 达到平衡时,容器Ⅰ中的A体积分数与容器Ⅱ中的相同
D. 容器Ⅰ中反应到达平衡所需时间比容器Ⅲ中的短
查看答案和解析>>
科目: 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在:钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)工艺流程如下:
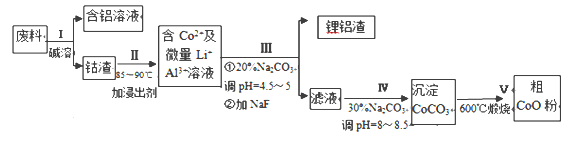
(1)过程Ⅰ中采用NaOH溶液溶出废料中的Al,反应的离子方程式为_________________。
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为 (产物中只有一种酸根)_________。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从氧化还原和环境保护的角度分析不用盐酸浸出钴的主要原因____。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式_____ 。
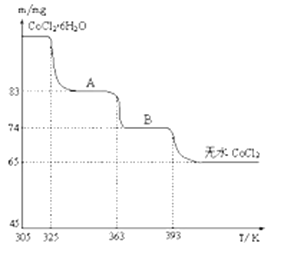
(4)如图是CoCl2.6H2O晶体受热分解时,剩余固体的质量随温度变化的曲线,B物质的化学式是______________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】等质量的CH4和NH3相比较,下列结论正确的是( )
A.它们的分子个数比为17∶16B.它们的原子个数比为17∶16
C.它们的氢原子个数比为17∶16D.它们所含氢的质量比为17∶16
查看答案和解析>>
科目: 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐![]()
![]()
![]()
![]()
![]() 滤液
滤液![]()
![]() 精盐
精盐
(1)如何检验该粗盐中含有SO42-___。
(2)第④步中加入过量的Na2CO3的目的是___。
(3)蒸发结晶需要的玻璃仪器___。
(4)若先加适量盐酸再过滤,将对实验结果产生影响,其原因是______。(用离子方程式结合文字解释)
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素A、B、C、D、E的原子序数依次增大,其中A、D同主族,B、C、D、E同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素,C原子的质子数比B原子的质子数多2个。请回答下列问题:
(1)B元素的名称为___________,E的元素符号为___________
(2)A、B两种元素可形成化学式为B2A、B2A2等化合物,则B2A2的电子式为_____。
(3)将B2A2投入到B2D的水溶液中可生成D的单质,发生反应的离子方程式为:______________________
(4)DA2与E元素的单质在水中反应的离子方程式为:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:A(s)+3B(g)![]() 2C(g) ΔH<0,在体积为10L的密闭容器中发生反应的过程如图所示。下列说法正确的是( )
2C(g) ΔH<0,在体积为10L的密闭容器中发生反应的过程如图所示。下列说法正确的是( )
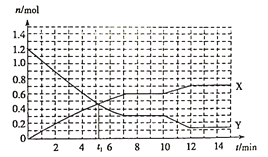
A. X曲线表示B的物质的量随时间变化的关系
B. 第t1 min时说明反应达到了平衡
C. 前4 min,用C表示反应速率为v(C)=0.1 mol·L-1·min-1
D. 第10 min时,可能采取了降温
查看答案和解析>>
科目: 来源: 题型:
【题目】溴化钙具有易溶于水、易吸潮等性质。溴化钙可用作阻燃剂、制冷剂,实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:
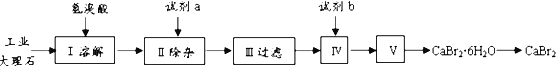
回答下列问题:
(1)已知步骤III的滤液中不含NH4+。步骤II加入的试剂a是___________,控制溶液的pH约为8.0的目的是___________、___________。
(2)试剂b是___________,步骤IV的目的是_______。
(3)步骤V所含的操作依次是________________、过滤。
(4)制得的溴化钙可以通过如下步骤测定其纯度:
称取4.00g无水溴化钙样品;溶解;滴入足量Na2CO3溶液,充分反应;过滤;烘干;冷却。若得到1.88g碳酸钙,则溴化钙的质量分数为_________。 若实验操作规范而测定结果偏低,其原因是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题
(1)已知在常温常压下:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) H=-1275.6kJ·mol-1
②H2O(l)=H2O(g) H=+44.0 kJ·mol-1 写出表示甲醇燃烧热的热化学方程式___________________________。
(2)已知:CH3OH(g)+ ![]() O2(g)
O2(g)![]() CO2(g)+2H2(g) H1=-192.9kJ·mol-1
CO2(g)+2H2(g) H1=-192.9kJ·mol-1
H2(g)+ ![]() O2 (g)
O2 (g) ![]() H2O(g) H2=-120.9kJ·mol-1
H2O(g) H2=-120.9kJ·mol-1
则甲醇与水蒸气催化重整反应的焓变H3________________。
(3)苯乙烯是重要的基础有机原料。工业中用乙苯(C6H5—CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5—CH=CH2)的反应方程式为:C6H5—CH2CH3(g)![]() C6H5—CH=CH2(g)+H2(g) H1
C6H5—CH=CH2(g)+H2(g) H1
已知:3C2H2(g)![]() C6H6(g) H2;C6H6(g)+C2H4(g)
C6H6(g) H2;C6H6(g)+C2H4(g)![]() C6H5—CH2CH3(g) H3
C6H5—CH2CH3(g) H3
则反应3C2H2(g)+C2H4(g)![]() C6H5—CH=CH2(g) +H2(g)的H =________。
C6H5—CH=CH2(g) +H2(g)的H =________。
(4)氨的合成是最重要的化工生产之一。工业上合成氨用的H2有多种制取的方法:
①用焦炭跟水反应: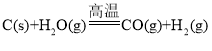 ;
;
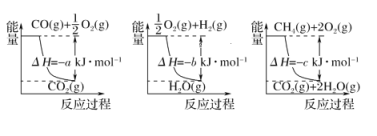
②用天然气跟水蒸气反应: 已知有关反应的能量变化如图所示,则方法②中反应的H =________。
已知有关反应的能量变化如图所示,则方法②中反应的H =________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知短周期主族元素Q、T、U、V、W、X、Y、Z原子序数依次增大。已知:T与U、V同周期,W与X、Y、Z同周期,U和Y同族;元素Q的某种核素没有中子;元素T的最高正价与最低负价的代数和为0;Q与U形成的气态化合物相对分子质量为17;工业上通过分离液态空气获得V的单质,且该单质的某种同素异形体是保护地球地表环境的重要屏障;W、X、Z的最高价氧化物对应的水化物两两之间都能反应,且W、X、Z原子最外层电子数之和等于W的原子序数。
(1)Z元素原子的 L层电子数为______,元素 Y的原子结构示意图___________,T的一种核素在考古时常用来鉴定一些文物的年代,用的核素是___________(填核素符号)。
(2)元素Q与V可以形成18电子化合物的其电子式为_________,元素W与Q形成的化合物的类型_____________(填‘离子化合物’或‘共价化合物’)。
(3)V的氢化物比同主族其他元素的氢化物的熔沸点明显偏高,原因是___________。
(4)写出X、W 两种元素最高价氧化物对应的水化物相互反应的离子方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com