
科目: 来源: 题型:
【题目】图中装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于 ( )

A. 锌和盐酸生成氢气
B. 二氧化锰和浓盐酸生成氯气
C. 碳酸钙和盐酸生成二氧化碳
D. 浓氨水和烧碱制取氨气
查看答案和解析>>
科目: 来源: 题型:
【题目】向甲溶液加入(或通入)物质乙(乙物质为气体或溶液),生成沉淀的质量与消耗乙的质量关系曲线符合图的是

A.向Na[Al(OH)4]溶液中通入二氧化碳
B.向Na[Al(OH)4]溶液中滴加盐酸
C.向澄清石灰水中通入二氧化碳
D.向Al2(SO4)3溶液中滴加NaOH溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,物质之间通过一步反应不能实现如图所示转化的是
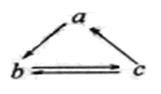
a | b | c | |
A | Al2O3 | Na[Al(OH)4] | Al(OH)3 |
B | HNO3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | Fe | FeCl3 | FeCl2 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是
A.V(H2)==0.1 mol/(L·min)B.V(N2)==0.1mol/(L·min)
C.V(NH3)==0.15mol/(L·min)D.V(N2)==0.02mol/(L·s)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,容器内某一反应种M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是
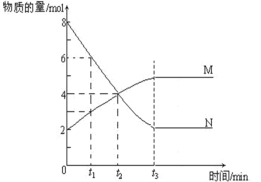
A.t2时,正逆反应速率相等,达到平衡
B.t3时间以后,正反应速率大于逆反应速率
C.t1时N的浓度是M的两倍
D.达到平衡时,N的浓度与M的浓度相等且不变
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组同学取V L浓缩的海水,用下图所示装置模拟工业法提溴。回答下列问题:
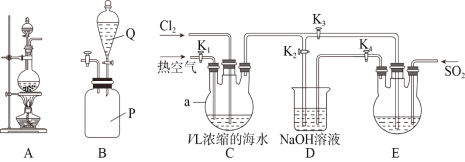
(1)装置A可用于实验室制备氯气,其反应原理为________________________________(用离子方程式表示),装置B是SO2贮气瓶,则Q中的溶液为________________。
(2)溴的富集过程:
①通入氯气与通入热空气的顺序是先通______________,通入氯气时K1、K2、K3的关、开方式是___________________。
②装置D的作用是_______________________________,通入SO2时装置E中发生反应的化学方程式为______________________________________。
(3)溴的精制:
①待装置E中Br-全部转化为单质后,再利用下图中的____________(填字母)装置进行蒸馏即可得到纯溴。
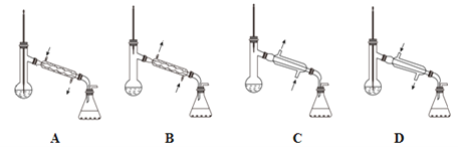
②假设最终得到m g纯溴,实验中溴的利用率为b%,则浓缩海水中c(Br-)=______________.
查看答案和解析>>
科目: 来源: 题型:
【题目】利用化学原理对废气、废水进行脱硝、脱碳处理,可实现绿色环保、废物利用,对构建生态文明有重要意义。
Ⅰ.脱硝:
(1)H2还原法消除氮氧化物
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+133 kJ/mol
H2O(g)=H2O(l) ΔH2=-44 kJ/mol
H2的燃烧热ΔH3=-285.8 kJ/mol
在催化剂存在下,H2还原NO2生成水蒸气和氮气的热化学方程式为__________。
(2)用NH3催化还原法消除氮氧化物,发生反应:
4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) ΔH<0
5N2(g)+6H2O(l) ΔH<0
相同条件下,在2L恒容密闭容器中,选用不同催化剂,产生N2的量随时间变化如图所示。
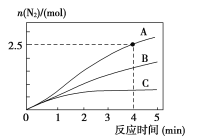
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=____。
②下列说法正确的是____。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已达到平衡
D.若反应在恒容绝热的密闭容器中进行,当K值不变时,说明已达到平衡
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH_____(填“增大”“减小”或“不变”),负极的电极反应式为________。
Ⅱ.脱碳:
(4)用甲醇与CO反应生成醋酸可消除CO污染。常温下,将a mol/L醋酸与b mol/L Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),忽略溶液体积变化,计算醋酸的电离常数Ka=________(用含a、b的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】
研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________,原因是______________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。

查看答案和解析>>
科目: 来源: 题型:
【题目】钴铁氧体(CoFe2O4)不仅是重要的磁性材料、磁致伸缩材料,还是重要的锂离子电池负极材料。工业上,可以由废旧锂钴电池正极材料(主要含Fe、Al、硅等杂质)回收钴,再用电化学法制得CoFe2O4。其流程如图所示(过程中所加试剂均足量)
Ⅰ.废旧电池中钴的回收

(1)含铝滤液中,铝元素的存在形式为________(写化学式);硅在过程_____(填序号)与钴分离。
(2)写出过程②中LiCoO2与H2O2发生反应的化学方程式____________________________。
(3)过程③Na2CO3的主要作用为________________________________________。
Ⅱ.电解法制得钴铁合金
(4)配制 0.050molL-1 FeSO4和0.025molL-1 CoSO4的混合溶液,用铜作阴极、石墨作阳极进行电解,获得CoFe2合金。阴极的电极方程式为____________________________________。
Ⅲ.阳极氧化法制得钴铁氧体
(5)以1.500molL1NaOH溶液作电解液,纯净的钴铁合金(CoFe2)作阳极进行电解,在阳极上获得CoFe2O4薄膜。该电解过程的化学方程式为_________________________。
(6)当电路上有0.4mol电子转移时,阳极电极材料增重质量为3.4g,与理论值不符,其原因可能为______________________________________________。
(7)由废旧锂钴电池制CoFe2O4的现实意义在于:______________________(写一条即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知 4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH= -1200kJ·mol-1
4CO2(g)+N2(g) ΔH= -1200kJ·mol-1
①该反应在________________(填“高温、低温或任何温度”)下能自发进行。
②对于该反应,改变某一反应条件(温度T1>T2),下列图像正确的是_______(填序号)。
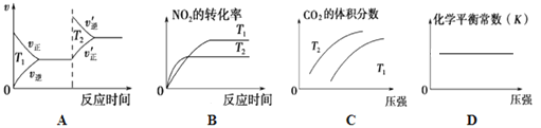
③某实验小组模拟上述净化过程,一定温度下,在 2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________;两种方式达平衡时,N2的体积分数:甲______乙( 填“>、=、<或不确定”,下同),NO2的浓度:甲______乙。
甲 | 乙 |
0.2mol NO2 | 0.1mol NO2 |
0.4mol CO | 0.2mol CO |
(2)柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
模拟尾气 | 气体(10mol) | 碳烟 | ||
NO | O2 | He | ||
物质的量(mol) | 0.025 | 0.5 | 9.475 | a |
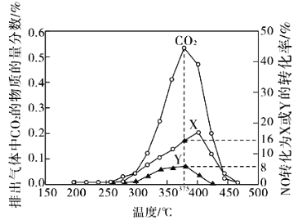
①375℃时,测得排出的气体中含0.45mol O2和0.0525mol CO2,则Y的化学式为________。
②实验过程中采用NO模拟NOx,而不采用NO2的原因是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com