
科目: 来源: 题型:
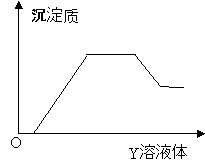
【题目】向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,符合图像的一组是
X | Y | |
A | AlCl3、Mg(NO3)2、HNO3 | NaOH |
B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 |
C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH |
D | NaAlO2、氨水、NaOH | H2SO4 |
查看答案和解析>>
科目: 来源: 题型:
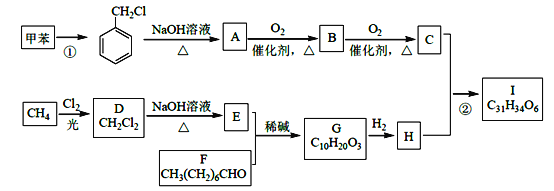
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下:
已知:a、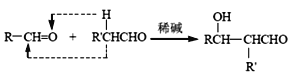
b、
回答下列问题:
(1)反应①所需试剂、条件分别是____________;F 的化学名称为____________。
(2)②的反应类型是______________;A→B 的化学方程式为_________________。
(3)E的结构简式为______________;H 中所含官能团的名称是____________。
(4)化合物W 的相对分子质量比化合物C 大14,且满足下列条件,W 的可能结构有____种。①遇FeCl3 溶液显紫色;②能发生银镜反应,其中核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出符合要求的W 的结构简式____________。
(5)设计用甲苯和乙醛为原料制备![]() 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A
的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A![]() B。。。
B。。。![]() 目标产物。____________。
目标产物。____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验过程中产生的现象与对应的图形相符的是( )
A.  NaHSO3 粉末加入HNO3溶液中B.
NaHSO3 粉末加入HNO3溶液中B.  SO2气体通入新制氯水中
SO2气体通入新制氯水中
C.  NaOH溶液滴入 Ba(HCO3)2溶液中D.
NaOH溶液滴入 Ba(HCO3)2溶液中D. 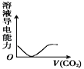 CO2气体通入澄清石灰水中
CO2气体通入澄清石灰水中
查看答案和解析>>
科目: 来源: 题型:
【题目】C、N、O、P、S、Cl、Cu、Zn八种元素的单质及化合物在现代工业生产中有着广泛的应用,请回答下列问题:
(1)第一电离能:Zn_______Cu(填“>”或“<”下同)电负性S ______Cl。
(2)写出基态Cu原子的价电子排布式_________________
(3)SO3的空间构型是________________ ,白磷P4分子呈正四面体结构,P原子位于正四面体的四个顶点,则P原子的杂化形式为_________________。
(4)与SCN—互为等电子体的微粒有_________________________(任写两种)。
(5)NH3、PH3、AsH3三者的沸点由高到低的顺序是___________,原因是______________。
(6)Cu与Cl形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
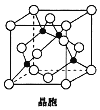
①该晶体的化学式为_________。
②已知该晶体中Cu原子和Cl氯原子之间的最短距离apm且恰好为体对角线的![]() ,阿伏伽德罗常数为NA,则该晶体的密度为__________________g/cm3(列出计算式即可)。
,阿伏伽德罗常数为NA,则该晶体的密度为__________________g/cm3(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,B是最活泼的非金属元素,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是周期表中最强的含氧酸。
(1)元素B在周期表中的位置是_________,甲的电子式是_______。
(2)单质D与C的最高价氧化物对应水化物的水溶液反应的离子方程式是___________。
(3)单质E与C的最高价氧化物对应水化物的水溶液反应的化学方程式是________。
(4)物质乙与水反应的化学方程式____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上以菱铁矿(主要成分是FeCO3及少量SiO2)为原料制备高铁酸钠生产过程如下:
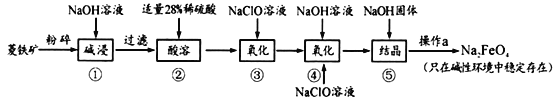
(1)Na2FeO4中铁元素的化合价为_____________,高铁酸钠用于杀菌消毒时的化学反应类型为_______________(填“氧化还原反应”、“复分解反应”或“化合反应”)。
(2)按照上述流程,步骤①中碱浸时能否用较便宜的Ca(OH)2替代NaOH___________ (填“能”或“不能”),理由是________________________。
(3)步骤③中检验Fe2+全部转化成Fe3+的方法是:___________________________。
(4)步骤④中除生成Na2FeO4外,还有NaCl生成,其离子方程式为_____________。己知步骤⑤是向Na2FeO4溶液中继续加入氢氧化钠固体得到悬浊液,则操作a的名称为_____。
(5)生产过程中,理论上每获得0.5mol的FeO42-消耗 NaClO的总质量为_______________。
(6)已知几种物质在20℃时的Ksp如下表:
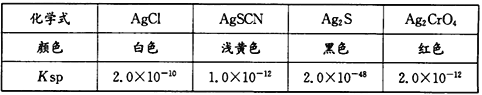
某同学用滴定法测定晶体CoCl2·xH2O中的x,常用标准硝酸银法进行滴定,滴定时选择的指示剂是_____(填编号)。
A.KCl B.KSCN C.K2S D.K2CrO4
若取晶体样品ag溶于蒸馏水中配制100mL溶液取20mL配制溶液于锥形瓶中,加入所选指示剂,用cmol/LAgNO3溶液滴定至终点消耗标准溶液bmL。则x的表达式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是物质间发生化学反应的颜色变化,其中物质a、b、c、d对应的物质正确的是( )
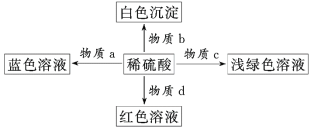
选项 | 物质a | 物质b | 物质c | 物质d |
A | Cu2(OH)2CO3 | Ba(OH)2 | Fe(OH)3 | 酚酞溶液 |
B | CuO | NaAlO2 | Fe2O3 | 紫色石蕊溶液 |
C | CuO | BaCl2 | FeO | 酚酞溶液 |
D | Cu(OH)2 | Ba(NO3)2 | FeO | 紫色石蕊溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。下列是有机物A~G之间的转化关系:

请回答下列问题:
(1)A的官能团的名称是____________;C的结构简式是__________;
(2)E是一种具有香味的液体,由B+D→E的反应类型是_______,该反应方程式为_________;
(3)G是一种高分子化合物,其结构简式是__________;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F进行应急处理。写出由A制F的化学反应方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2在活性炭作用下反应制取少量的SO2Cl2,装置如图所示(部分夹持装置省略)。已知SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生剧烈的水解反应,并产生白雾。
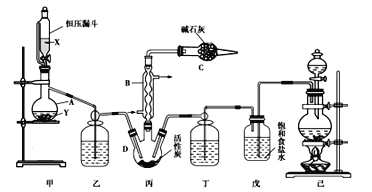
(1)仪器B的名称为_____,由仪器B的使用可知SO2与Cl2反应的ΔH____(填“>”或“<”)0。
(2)仪器C的作用是________________________________。
(3)试剂X、Y的组合最适宜的是______。
a.18.4mol/LH2SO4溶液+Cu b.4mol/LHNO3溶液+Na2SO3 c.75%H2SO4溶液+K2SO3
(4)反应结束后,将丙中产物分离的实验操作的名称是______。
(5)分离产物后,向获得的SO2Cl2中加入足量NaOH溶液,振荡、静置得到无色溶液w。
①写出该反应的离子方程式:___________。
②检验溶液w中存在SO42-的方法是________。
(6)若反应中消耗的氯气的体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为_________(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
A. C生成的速率是A反应速率的2倍
B. A、B、C的浓度不再变化
C. 单位时间内生成nmol A,同时生成3nmol B
D. A、B、C的分子数之比为1∶3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com