
科目: 来源: 题型:
【题目】白黎芦醇具有抗氧化和预防心血管疾病的作用。可通过以下方法合成:
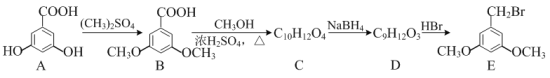

⑴化合物A中所含官能团的名称为______和______。
⑵由F→G的反应类型是______。
⑶D的结构简式为______。
⑷写出同时满足下列条件的C的一种同分异构体的结构简式:______。
①能发生银镜反应,与FeCl3溶液不显色;
②能发生水解反应,水解产物之一能与FeCl3溶液显色;
③分子中含有4种不同化学环境的氢。
⑸请写出以苯甲酸、甲醇为原料制备![]() 的合成路线流程图,无机试剂可任选,合成示例见本题题干。_________________
的合成路线流程图,无机试剂可任选,合成示例见本题题干。_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应在含氯物质的制取、含量测定等方面有重要的作用。
⑴将一定量的氯气通入过量NaOH溶液中,由于副反应的存在,溶液中同时存在Cl-、ClO-和ClO3-。若Cl-、ClO-和ClO3-的物质的量分别为a mol、b mol和c mol,根据电子得失守恒可知a、b、c之间一定存在的等量关系是______。
⑵工业次氯酸钠溶液中含有氯酸钠会影响产品质量。测定次氯酸钠样品中的氯酸钠含量的过程如下:
步骤Ⅰ:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将ClO-完全还原成Cl-(ClO3-在该条件不与H2O2反应),加热煮沸,冷却至室温,加入硫酸至酸性,
步骤Ⅱ:向步骤Ⅰ所得溶液中加入0.1000 mol·L-1硫酸亚铁溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。
已知步骤Ⅱ中涉及的相关反应转化为:ClO3-![]() Cl-,Cr2O72-
Cl-,Cr2O72-![]() Cr3+,则碱性NaClO溶液试样中所含NaClO3的物质的量浓度为______mol·L-1。
Cr3+,则碱性NaClO溶液试样中所含NaClO3的物质的量浓度为______mol·L-1。
⑶NaClO2广泛用于造纸工业、污水处理等,可由ClO2为原料反应制得。某溶液X中同时含有ClO2和NaClO2,为测定其中ClO2-的浓度,现进行如下实验:
步骤1:量取25.00 mL溶液X,调节溶液的pH为8.0,加入足量的KI晶体(发生反应:2ClO2+2I-=2ClO2-+I2)。滴入2滴淀粉溶液,滴加0.02000 mol·L-1Na2S2O3溶液(发生反应:2Na2S2O3+I2=Na2S4O6+2NaI)。恰好完全反应时,消耗Na2S2O3溶液12.50 mL。
步骤2:调节上述反应后溶液的pH为1.0(发生反应:ClO2-+4H++4I-=Cl-+2I2+2H2O),滴加0.2500 mol·L-1Na2S2O3溶液。恰好完全反应时,消耗Na2S2O3溶液40.00 mL。请计算溶液X中ClO2-的物质的量浓度(写出计算过程)。_______
查看答案和解析>>
科目: 来源: 题型:
【题目】五种主族元素X、Y、Z、M和N在周期表中的位置如图所示。下列说法正确的是

A. M的原子半径比N小
B. Y和Z既可形成Z2Y,也可形成Z2Y2
C. X2M的热稳定性比X2Y强
D. M和N的氧化物的水化物均为强酸
查看答案和解析>>
科目: 来源: 题型:
【题目】双氧水是常见的氧化剂、消毒剂,一种制取双氧水的流程如下:
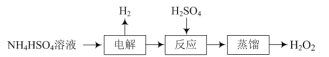
(1)“电解”后生成(NH4)2S2O8,该反应的化学方程式为______。
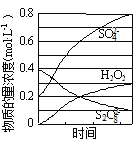
(2)“反应”中部分物质的浓度变化如图所示,该反应的离子方程式为______。
(3)双氧水中H2O2的含量可以用酸性KMnO4溶液来测定,测定时MnO![]() 被还原成Mn2+,测定反应的离子方程式为______。
被还原成Mn2+,测定反应的离子方程式为______。
(4)pH=6时,(NH4)2S2O8溶液与足量MnSO4反应有MnO2沉淀生成,过滤后所得滤液中含硫微粒均为SO42-,该反应的离子方程式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】很多非金属元素是地球上组成生命的基本元素,特别是碳元素、氧元素与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。请回答下列问题:
(1)基态碳原子最外层有______种空间运动状态不同的电子,其价电子排布图(即价电子轨道表示式)为______。
(2)写出COS的电子式:_______,中心原子的杂化轨道类型为_______杂化,写出与COS互为等电子体的粒子化学式(分子与离子各一种):________、_______。
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
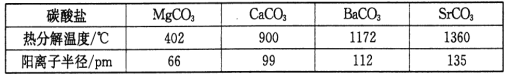
试从生成物角度分析为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?___________。
(4)碳的一种同素异形体—C60,又名足球烯,是一种高度对称的球碳分子(C60分子结构和C60晶体的晶胞结构如下图所示)。立方烷(分子式:C8H8,结构是立方体:![]() )是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体中组成的C8H8与C60分子个数比为__________。
)是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体中组成的C8H8与C60分子个数比为__________。
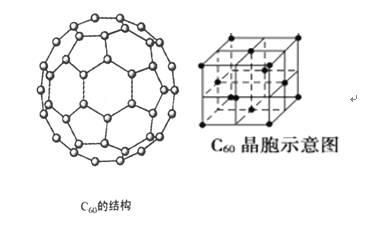
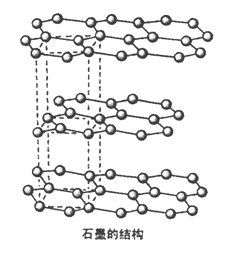
(5)碳的另一种同素异形体——石墨,其晶体结构如图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为________个。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其周期数相同;B的价电子排布式为nsnnpn+2;短周期元素C和D为同周期不相邻的元素,C是同周期元素中离子半径最小的元素,D元素最外层有两个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ECl4(氯化物)溶液的方法制备纳米材料。回答下列问题:
(1)D元素在周期表中的位置为______,E原子核外有_____个未成对电子,五种元素中电负性最大的是_____(填元素名称)。
(2)由A、B、D三种元素形成的常见三元化合物中具有强氧化性的是______(填化学式)。
(3)氯元素能与C(非碳元素符号)形成某化合物Q。在1.01×105Pa、T1℃时,气体摩尔体积为53.4L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的结构式为___________。(如有配位键须用“→”标出)
(4)A、B、D元素形成的化合物有A2B、DB3,下列关于A2B和DB3的说法中,正确的是________(填标号)。
A.中心原子的价层电子对数目相等 B.都是非极性分子
C.中心原子的孤电子对数目相等 D.都含有极性键
E.都能与Na2O反应 F.固态时晶体类型不同
(5)D在空气中燃烧的产物分子构型为_________。固体DB3中存在如图所示的三聚分子,该分子中D原子的杂化轨道类型为________。

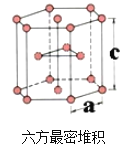
(6)E单质有两种同素异形体,高温下是体心立方堆积;但在常温下的晶体结构为如下图所示的六方最密堆积(底面是正六边形)。已知常温下晶体晶胞参数分别为a cm和c cm,则该晶体的密度可表示为________g·cm-3。(用含a和c的式子表示,用NA表示阿伏伽德罗常数的值)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质结构的命题中,错误的项数有( )
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2中阴阳离子个数比不同
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为: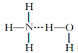
⑦HF晶体沸点高于HCl,是因为 HCl共价键键能小于HF
A. 4项B. 5项C. 6项D. 7项
查看答案和解析>>
科目: 来源: 题型:
【题目】向体积均为2 L的两个恒容密闭容器中分别充入1molSiHCl3,维持容器的温度分别为T1℃和T2℃不变,发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
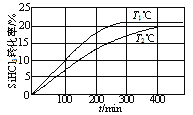
A.T1>T2
B.T1℃时,0~100min反应的平均速率v(SiHCl3)=0.001mol·(L·min)-1
C.T2℃时,反应的平衡常数:K=1/64
D.T2℃时,使用合适的催化剂,可使SiHCl3的平衡转化率与T1℃时相同
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
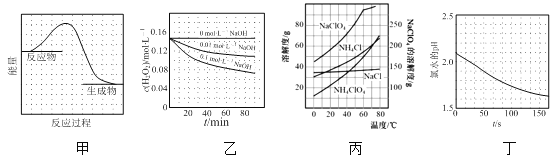
A.图甲表示某反应过程中的能量变化曲线,可推知该反应是吸热反应
B.图乙表示70℃时不同碱性条件下H2O2的浓度随时间变化的曲线,可推知溶液碱性越强,H2O2分解速率越慢
C.图丙表示部分物质的溶解度随温度变化的曲线,可推知20℃时向含a mol NaClO4的饱和溶液中加入a mol NH4Cl固体会有NH4ClO4固体析出
D.图丁表示光照下氯水的pH随时间的变化曲线,可推知光照后溶液中Cl2浓度增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.反应2CO(g)+O2(g)=2CO2(g)在一定条件下能自发进行的原因是ΔS>0
B.由Ksp[Mg(OH)2]=1.8×10-11可知常温下pH=8的溶液中,c(Mg2+)≤1.8×10-5mol·L1
C.反应H2(g)+Cl2(g)=2HCl(g)的ΔH可用下式换算:ΔH=反应中断裂的旧化学键键能之和-反应中形成的新化学键键能之和
D.由反应C(s)+1/2O2 (g)=CO(g)ΔH=-111 kJ·mol1可知C的燃烧热是111 kJ·mol1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com