
科目: 来源: 题型:
【题目】近年研究表明离子液体型催化剂GIL可对某些特定加成反应有很好的催化作用,有机化合物H的合成路线如下:

(1)C中含有的官能团名称为_____。
(2)C→D的反应类型为_____。
(3)已知:G和H的分子式相同,F→G和B→C反应类型也相同,那么G的结构简式为_____。
(4)写出满足下列条件的B的一种同分异构体X的结构简式:_____。
①1molX完全水解消耗2molNaOH;
②水解酸化后两种产物核磁共振氢谱均有4个峰,峰高比为3∶2∶2∶1。
(5)以乙醇为原料利用GIL合成聚酯![]() 写出合成路线流程图(无机试剂可任选,合成路线流程图示例见本题题干)。______
写出合成路线流程图(无机试剂可任选,合成路线流程图示例见本题题干)。______
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,不正确的是( )
A.实验室用H2O2分解制O2,加入MnO2作催化剂后,反应速率明显加快
B.2SO2+O2![]() 2SO3反应中,SO2的转化率能达到100%
2SO3反应中,SO2的转化率能达到100%
C.日常生活中用冰箱冷藏食物可降低食物变质的反应速率
D.可逆反应在一定条件下达到化学反应限度时正反应速率和逆反应速率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】(17分)顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:
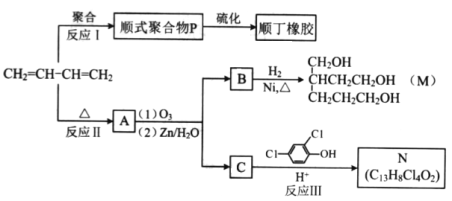
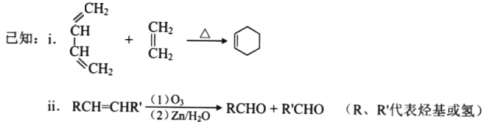
(1)CH2=CH-CH=CH2的名称是_______;
(2)反应I的反应类型是(选填字母)_______;
a.加聚反应 b.缩聚反应
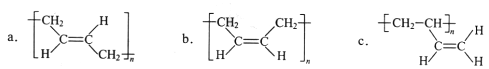
(3)顺式聚合物P的结构式是(选填字母)_______;
(4)A的相对分子质量为108.
①反应II的化学方程式是_____________________
②1molB完全转化为M所消耗的H2的质量是______g。
(5)反应III的化学方程式是______________________________。
(6)A的某些同分异构体在相同反应条件下也能生成B和C,写出其中一种同分异构体的结构简式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关下列装置或操作说法正确的是
A.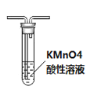 中:可以除去甲烷中混有的乙烯
中:可以除去甲烷中混有的乙烯
B. 中:装置可用于证明非金属性强弱:Si<C<Cl
中:装置可用于证明非金属性强弱:Si<C<Cl
C. 中:可用于制备、收集乙酸乙酯
中:可用于制备、收集乙酸乙酯
D.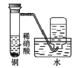 中:制备并收集少量NO2气体
中:制备并收集少量NO2气体
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____。
②与BH4-互为等电子体的阳离子的化学式为_____。
③H、B、Ti原子的第一电离能由小到大的顺序为_____。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
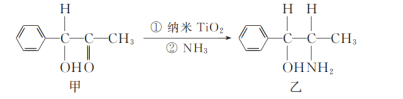
化合物乙的分子中采取sp3杂化方式的原子个数为_____。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____。
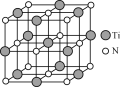
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】烟气中的氮氧化物是造成大气污染的重要因素。
(1)NOx是汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
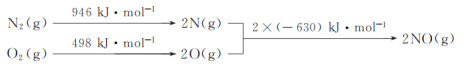
则N2(g)和O2(g)反应生成NO(g)的热化学反应方程式为___。
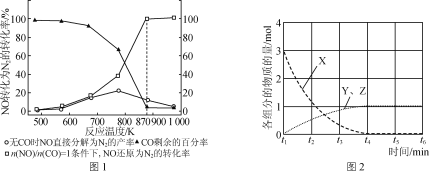
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag—ZSM—5为催化剂,测得NO转化为N2的转化率随温度变化情况如图1所示。
①若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为_____。
②NO直接催化分解(生成N2与O2)也是一种脱硝途径。在不同条件下,NO的分解产物不同。在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图2所示。请写出NO分解的化学方程式:______。
(3)一定条件下,向NOx/O3混合物中加入一定浓度的SO2气体,进行同时脱硫脱硝实验,实验结果如图3。
①同时脱硫脱硝时NO的氧化率略低的原因是____。
②由图3可知SO2对NO的氧化率影响很小的原因是_____。
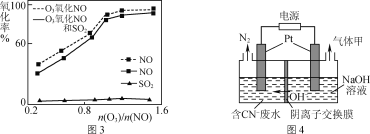
(4)有人设想采用下列方法减少烟气中的氮氧化物对环境的污染:用天然气中的CH4、H2等还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NOx。请写出这种含硫化合物和NOx反应的化学方程式:_____。
(5)某工业废水中含有毒性较大的CN-,可用电解法将其转变为N2,装置如图4所示。电解池中生成N2的电极反应式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】食盐是一种重要的化工原料。请回答下列问题。
⑴请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
![]()
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和__________________。
②在蒸发过程中,待________时,停止加热,利用余热将滤液蒸干。
⑵由于粗盐中含有MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如下图。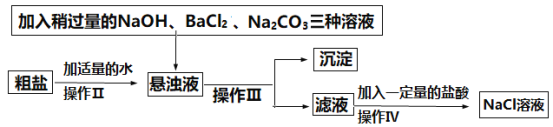
除杂质过程中用到下列操作: a.加入适量稀盐酸 b.加入过量BaCl2溶液 c.加入过量Na2CO3溶液 d.加入过量NaOH溶液
①除去可溶性杂质加入试剂的正确顺序是_____________(填序号)
②证明SO42-已经沉淀完全的方法是__________。
③加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是_____(用化学方程式表示)。
④操作Ⅳ所得滤液中加入一定量的盐酸,用玻璃棒搅拌直到没有气泡冒出,还要进行____(操作)。然后将滤液倒入蒸发皿蒸发。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:

这种材料可采用如图所示的合成路线
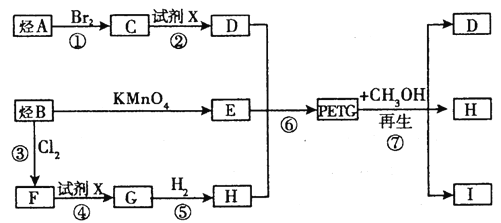
(1)![]()
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1) ⑦的反应类型是________________。
(2) 写出I的结构简式:___________________。
(3) 合成时应控制的单体的物质的量:n(H)∶n(E)∶n (D)=____________(用m、n表示)。
(4) 写出反应②的化学方程式:______________________
(5) 写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①该同分异构体的苯环上相邻的三个碳原子上都连有取代基。
②该同分异构体在一定条件下能发生银镜反应和水解反应,遇到FeCl3溶液显紫色。
______________、_________________、____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有Ⅰ~Ⅳ四个体积均为0.5 L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
容器 | 起始时 | ||
t/℃ | n(HCl)/mol | Z | |
Ⅰ | 300 | 0.25 | a |
Ⅱ | 300 | 0.25 | b |
Ⅲ | 300 | 0.25 | 4 |
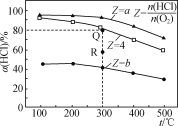
A. ΔH<0,a<4<b
B. 300℃该反应的平衡常数的值为64
C. 容器Ⅲ某时刻处在R点,则R点的υ正>υ逆,压强:p(R)>p(Q)
D. 若起始时,在容器Ⅳ中充入0.25molCl2和0.25molH2O(g),300℃达平衡时容器中c(HCl)=0.1mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中的实线表示元素周期表的边界。①~⑧分别表示元素周期表中对应位置的元素。

(1)上述元素所能形成的简单离子中半径最小的是________(填离子符号),最高价氧化物对应水化物酸性最强的是________(填分子式)。
(2)写出④与⑥形成的化合物的形成过程____________________
(3)元素①的氢化物电子式为______________。
(4)④、⑤、⑥各自的最高价氧化物对应的水化物两两皆能反应,它们反应的离子方程式为____________,______________,_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com