
科目: 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ/mol):P-P:198,P-O:360,O=O:498,则反应P4(白磷)+3O2=P4O6中消耗3 mol O2放出的热量为
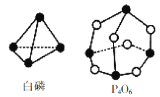
A.1368kJB.1498kJC.1638kJD.1683kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】如图两种化合物的结构或性质描述正确的是( )
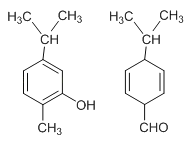
A. 两种化合物均是芳香烃
B. 两种化合物互为同分异构体,均能与溴水反应
C. 两种化合物分子中共平面的碳原子数相同
D. 两种化合物可用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
科目: 来源: 题型:
【题目】下列方程式不能正确表示某沉淀溶解过程的是
A.热的浓盐酸洗涤试管内壁的MnO2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B.热的NaOH溶液洗涤试管内壁的S:3S+6NaOH![]() 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O
C.向石灰石粉的悬浊液中持续通CO2:Ca(OH)2+2CO2=Ca(HCO3)2
D.稀硫酸可除去铁锈:Fe2O3+6H+=2Fe3++3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】某液态肼(N2H4)燃料电池被广泛应用于发射通讯卫星、战略导弹等运载火箭中。其中以固体氧化物为电解质,生成物为无毒无害的物质。下列有关该电池的说法正确的是
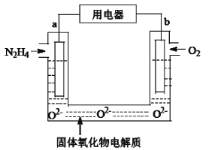
A.b极是正极,发生还原反应
B.电池电路中,电流方向:电极a→用电器→电极b
C.当电极a.上消耗1 mol N2H4时,电极b上被氧化的O2在标准状况下体积为11.2 L
D.b极附近的pH值变大
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F的核电荷数依次增大,且均为核电荷数小于18的非稀有气体元素。A的单质是自然界中密度最小的气体,A和C可形成A2C和A2C2两种常见的液态化合物,B、C原子的最外层电子数之和等于11,D+与C的简单离子的核外电子排布相同,C、E原子的最外层电子数相同。请回答下列问题:
(1)写出元素符号:B__,D__。
(2)A元素具有两个中子的核素的表示符号为__,E的简单离子的结构示意图是__。
(3)A2C2的分子式为__。
(4)将少量F的单质通入足量NaOH溶液中,发生反应的离子方程式是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A. 仅用水不能区分已烷、溴乙烷、乙醇三种液态有机物
B. 碳原子数小于或等于6的单烯烃,与HBr加成反应的产物只有1种结构,符合条件的单烯烃有3种
C. 苯、乙烷、乙烯、乙炔分子中碳碳键的键长分别为a、b、c、d,则![]() >d
>d
D. 等质量的烃完全燃烧,耗氧量最多的是甲烷
查看答案和解析>>
科目: 来源: 题型:
【题目】证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
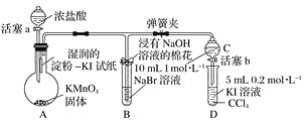
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是________________________________________。
(2)B中溶液发生反应的离子方程式是____________________________________________。
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是____________________________。
(4)过程Ⅲ实验的目的是________________________________________________________。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐________,得电子能力逐渐________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是
A.做中和热测定实验时,在大小烧杯之间填满碎泡沫塑料以防止热量散失
B.海上石油钢铁钻井平台可用外加电流的阴极保护法以防腐
C.H2O2催化分解每产生1molO2,转移电子的数目为2×6.02×1023
D.25℃时,加水稀释0.1molL﹣1NH4Cl,溶液中![]() 不断增大
不断增大
查看答案和解析>>
科目: 来源: 题型:
【题目】热还原法制备MgO材料的原理为MgSO4(s)+CO(g)![]() MgO(s)+SO2(g)+CO2(g) △H>0,T℃时,在一恒容密闭容器中加入一定量的MgSO4(s)和CO(g),一段时间后达到平衡状态。下列说法正确的是( )
MgO(s)+SO2(g)+CO2(g) △H>0,T℃时,在一恒容密闭容器中加入一定量的MgSO4(s)和CO(g),一段时间后达到平衡状态。下列说法正确的是( )
A. 活化能:E正>E逆
B. 其他条件不变,加入催化剂,△H减小
C. 其他条件不变,降低温度,化学平衡常数增大
D. 其他条件不变,向容器中通入Ar(g),平衡逆向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,回答相关的问题。
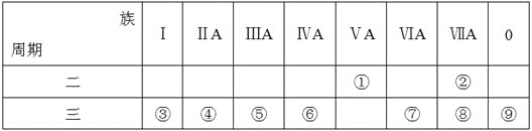
(1)写出④的元素符号__。
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:__。
(3)在这些元素中,最高价氧化物的水化物酸性最强的是__(填相应化学式,下同),碱性最强的是__。
(4)这些元素中(除⑨外),原子半径最小的是__(填元素符号,下同),原子半径最大的是__。
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为(方程式中用具体元素符号表示)__。
(6)⑦的低价氧化物通入足量Ba(NO3)2溶液中的离子方程式__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com