
科目: 来源: 题型:
【题目】下列说法正确的是
A. Si、P、S、Cl相应的最高价氧化物对应水化物的酸性依次增强
B. 自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片
C. 工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质[
D. 钠与氧气反应的产物与反应条件无关
查看答案和解析>>
科目: 来源: 题型:
【题目】书写化学方程式:
(1)乙醛的银镜反应___________________
(2)1-溴丙烷的消去反应_______
(3)乙醇的催化氧化反应_______________________
(4)制取聚乙二酸乙二酯的反应方程式____________
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石中不含其他与CO反应的成分),并除去尾气。CO气体用H2C2O4![]() CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
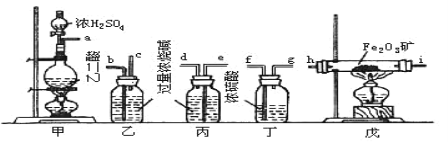
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a、b…表示) 接 , 接 , 接 , 接 。___________________
(2)装置乙的作用是___________________;装置丙的目的是____________________。
(3)实验结束后,先熄灭戊处的酒精灯,再熄灭甲处的酒精灯,其主要原因是____________________。
(4)实验前氧化铁矿粉末为xg,实验后测得乙、丙质量分别增加yg和zg,则氧化铁的质量分数为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B都是芳香族化合物,1摩尔A水解得到1摩尔B和1摩尔醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O,且B分子中碳和氢元素总的质量百分含量为65.2%。A的溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B的分子量之差为____________
(2)A的分子式是___________________
(3)B可能的三种结构简式是____________ 、_____________ 、__________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸的消费量是衡量一个国家化工生产水平的重要标志。而在硫酸的生产中,最关键的一步反应为:2SO2(g)+O2(g)![]() 2SO3(g)。
2SO3(g)。
(1)一定条件下,SO2与O2反应10min后,若SO2和SO3物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为___________________;10min生成SO3的化学反应速率为___________________。
(2)下列关于该反应的说法正确的是___________________。
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
(3)工业制硫酸,用过量的氨水对SO2尾气处理,请写出相关的离子方程式:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2为一种黄绿色气体,是目前国际上公认的高效、广谱、快速安全的杀菌剂,制备ClO2的新工艺是电解法。
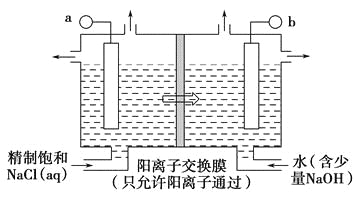
(1)如图表示用石墨做电极,在一定条件下电解饱和食盐水制取ClO2,写出阳极产生ClO2的电极方程式:__________________________________;图中b电极为_____________(填“阳极”或“阴极”)。
(2)电解一段时间,当阴极产生标准状况下气体112 mL时,停止电解,则通过阳离子交换膜的阳离子物质的量为________mol,阴极区pH________(填“变大”“变小”或“不变”)。
(3)ClO2对污水中Fe2+、Mn2+、S2-、CN-等有明显去除效果,某工厂中污水含CN-(a mol·L-1),现将ClO2把CN-氧化成两种无毒气体,写出该反应的离子方程式:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将4molA气体和2molB气体置于1L的密闭容器中,混合后发生如下反应:![]() 。若经2s后测得C的浓度为1.2mol/L,则下列说法正确的是( )
。若经2s后测得C的浓度为1.2mol/L,则下列说法正确的是( )
A.用物质A表示的反应速率为![]()
B.用物质B表示的反应速率为![]()
C.2s内物质A的转化率为30%
D.2s时物质B的浓度为0.6mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为相互串联的三个装置,试回答:
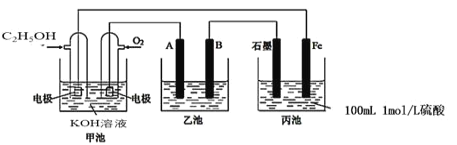
(1)写出甲池负极的电极反应式:________。
(2)若甲池消耗4.6gC2H5OH气体,则丙池中石墨极上生成气体的物质的量为______,反应一段时间后丙池溶液pH_______(填“增大”、“减小”、“不变”)。
(3)若利用乙池在铁片上镀银,则B是_______(填电极材料),电极反应式是______。
(4)若乙池中A、B为石墨电极,电解质溶液为CuCl2。当丙池共产生6.72L(标况)气体时,乙池A极产物_____mol,检验该产物的方法为:______(简述操作)。
查看答案和解析>>
科目: 来源: 题型:
【题目】今有化合物,甲:![]() 乙:
乙:![]() 丙:
丙:![]()
(1)甲、乙、丙之间是否互为同分异构体 ____(填“是”、“否”)请写出丙中含氧官能团的称:_______。
(2)写出只有一个侧链并且能水解的甲的同分异构体:___________
(3)请分别写出鉴别甲、乙、丙化合物的方法(指明所选试剂及主要现象即可)。
鉴别甲的方法:______________。
鉴别乙的方法:_____________________。
鉴别丙的方法:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:
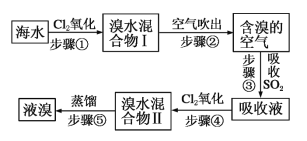
(1)步骤①反应的离子方程式是___________________。
(2)步骤③反应的化学方程式是___________________,从理论上考虑,下列也能吸收Br2的是___________________。
A.FeCl2 B.Na2SO3 C.H2O
(3)步骤①中已获得Br2,步骤③中又将Br2还原为Br-,步骤④又生成Br2,这样做的目的为___________________。
(4)已知海水中Br-含量为64mg/L,依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为___________________L(忽略Cl2的溶解)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com