
科目: 来源: 题型:
【题目】工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:

已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是___________________。
(2)反应器Ⅱ中发生反应的离子方程式为__________________________。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是___________________。
(4) Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有__________,请写出工业上用氯气和消石灰生产漂粉精的化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
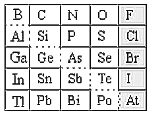
(1)元素Ga在元素周期表中的位置为:__________(写明周期和族)。
(2)Sn的最高正价为______,Cl的最高价氧化物对应水化物的化学式为_____,As的气态氢化物为_____。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_____(填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_____H2SeO4(填“>”、“<”或“=”)。
③氢化物的还原性:H2O_____H2S(填“>”、“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找_____(填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(5)①Se2Cl2常用作分析试剂,其电子式为_________。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。 下列说法正确的是_____(填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(6)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
实验步骤 | 实验现象与结论 |
在试管中加入_____,再加入_____,将生成气体通过_____洗气后,通入_____; | 现象:__________; 结论:非金属性C>Si |
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列物质转化中,A是一种酸式盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是________, Z是________。
(2)当X是强酸时,写出B生成C的化学方程式:___________________。
(3)当X是强碱时,E是________,写出E和铜反应生成C的化学方程式:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I、实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图所示:
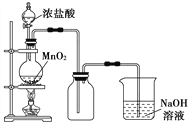
(1)圆底烧瓶中发生反应的化学反应方程式是__________________。
(2)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热(忽略盐酸的挥发),充分反应后生成的氯气明显_________(填大于、等于、小于)0.06 mol。其主要原因有_____________________________;
(3)写出尾气处理的离子方程式是_______________________。
II、用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量:____________。定容时,向容量瓶中加水,至1~2cm时,改用_________加水至刻度,加盖摇匀;
(2)下列操作对所配溶液的浓度可能产生影响
①Na2CO3·10H2O晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体(使用游码) ③碳酸钠晶体不纯,其中混有氯化钠 ④容量瓶未经干燥使用。 其中引起所配溶液浓度偏高的有______________(填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是

A. 放电时,多孔碳材料电极为负极
B. 放电时,外电路电子由多孔碳材料电极流向锂电极
C. 充电时,电解质溶液中Li+向多孔碳材料区迁移
D. 充电时,电池总反应为Li2O2-x=2Li+(1-![]() )O2
)O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 碳燃烧的热化学方程式为C(s)+1/2O2(g)=CO(g) ΔH=+110.5kJ·mol-1
B. 镀锌铁皮发生电化学腐蚀时,负极反应式为:Zn-2e–= Zn2+
C. NaHS水解的离子方程式是:HS﹣+H2O![]() S2﹣+H3O+
S2﹣+H3O+
D. 溶液中碳酸的电离方程式为:H2CO3![]() 2H++ CO32–
2H++ CO32–
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2SO3+I2+H2O=H2SO4+2HI,将0.1molCl2通入100ml含等物质的量的HI与H2SO3的混合溶液中,有一半的HI被氧化,则下列说法正确的是
A.物质的还原性:HI>H2SO3>HCl
B.HI与H2SO3的物质的量浓度为0.6 mol·L-1
C.通入0.1molCl2发生反应的离子方程式为:5Cl2+4H2SO3+2I-+4H2O=4SO42-+I2+10Cl-+16H+
D.若再通入0.05molCl2,恰好能将HI和H2SO3完全氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如下:
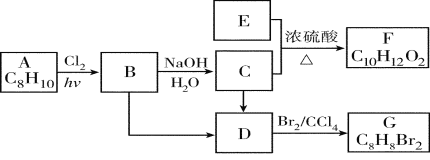
请回答下列问题:
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为________;
(2)A为一取代芳烃,B中含有一个甲基。由B生成C的化学方程式为:________________;
(3)由B生成D的反应条件是________________;
(4)在G的同分异构体中,苯环上一硝化的产物只有一种的共有________个,其中核磁共振氢谱有两组峰,且峰面积比为1∶1的是_________(填结构简式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用。
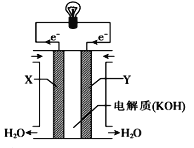
(1)下图为氢氧燃料电池的构造示意图,由此判断X极为电池的_____极,OH—向______(填“正”或“负”)极作定向移动,Y极的电极反应方程式为________,电路中每转移0.2mol电子,标准状况下正极上消耗气体的体积是_______ L。
(2)为了验证Fe3 +与Cu2+氧化性强弱,设计一个装置,下列装置既能产生电流又能达到实验目的的是__________。

(3)铅蓄电池是常见的化学电源之一,其充电、放电的总反应是:2PbSO4 + 2H2O![]() Pb + PbO2 + 2H2SO4。铅蓄电池放电时正极是______(填物质化学式),该电极质量_____(填“增加”或“减少)。若电解液体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到________mol/L。
Pb + PbO2 + 2H2SO4。铅蓄电池放电时正极是______(填物质化学式),该电极质量_____(填“增加”或“减少)。若电解液体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C三种物质的分子式都是C7H8O,若滴入FeCl3溶液,只有C呈紫色。若投入金属钠,只有B没有变化。
(1)若C的分子中苯环上的原子团处于邻位,写出A、B、C的结构简式:
A____________,B____________,C_____________ 。
(2)C的另外两种同分异构体的结构简式是:①__________,②________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com