
科目: 来源: 题型:
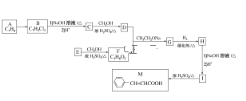
【题目】肉桂酸(M)是医药、香料的中间体,实验室由芳香化合物A制备M的一种合成路线如下:
已知:①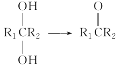 (R1、R2表示氢原子或烃基)
(R1、R2表示氢原子或烃基)
②R1COOR2+R3CH2COOR4![]()
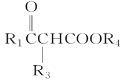 +R2OH
+R2OH
(R1、R3表示氢原子或烃基,R2、R4表示烃基)
请回答下列问题:(1)A→B的条件为________。
(2)E中所含官能团的名称为________。
(3)H的结构简式为________。(4)I→M的反应类型为________。
(5)D+F→G的化学方程式为________________________。
(6)同时满足下列条件的I的同分异构体有________种(不考虑立体异构),任写一种核磁共振氢谱中有6组吸收峰且峰面积之比为1:2:2:2:2:1的结构简式为_______。
①能发生显色反应和银镜反应 ②苯环上连有两个取代基
(7)参照上述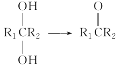 信息,以甲烷和苯酚为原料(其他无机试剂任选),设计制备
信息,以甲烷和苯酚为原料(其他无机试剂任选),设计制备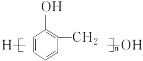 的合成路线_______________________。
的合成路线_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案中,不能达到相应实验目的的是
A | B | C | D | |
方案 |
|
|
|
|
目的 | 验证不同催化剂对化学反应速率的影响 | 验证石蜡油分解的产物中含有与烷烃性质不同的烃 | 制备乙酸乙酯 | 比较Cl2、I2的氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法不正确的是
A.1 mol苯分子中含有C=C双键数目为3NA
B.标准状况下,11.2L CH3Cl中含有的共价键数目为2NA
C.常温常压下,2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2 NA
D.17 g甲基(﹣14CH3)所含中子数为8NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 纤维素![]() 葡萄糖
葡萄糖 ![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 淀粉![]() 葡萄糖
葡萄糖 ![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
D. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,固定容积的密闭容器中发生下列反应:![]() 反应过程中,各物质浓度与时间的关系如图:
反应过程中,各物质浓度与时间的关系如图:
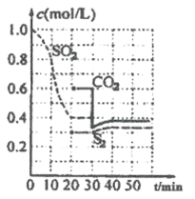
(1)该反应平衡常数表达式为![]() ____________。
____________。
(2)![]() 化学反应速率表示
化学反应速率表示![]() ______;建立平衡过程中,混合气体的密度______(选填“增大”、“减小”或“不变”)。
______;建立平衡过程中,混合气体的密度______(选填“增大”、“减小”或“不变”)。
(3)![]() 时改变外界条件,使
时改变外界条件,使![]() ______
______![]() (选填“大于”、“小于”或“等于”)。
(选填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。裂解的副反应为C4H10(g,正丁烷)![]() CH4(g)+C3H6(g),请回答下列问题:
CH4(g)+C3H6(g),请回答下列问题:
(1)化学上,将稳定单质的能量定为0,由元素的单质化合成单一化合物时的反应热叫该化合物的生成热,生成热可表示该物质相对能量。25 ℃、101 kPa几种有机物的生成热如下表所示:
物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/kJ· mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
由正丁烷裂解生成乙烯的热化学方程式为_____________________________。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。
下列情况能说明该反应达到平衡状态的是________(填标号)。
A.气体密度保持不变 B.c(C2H4)·c(C2H6)/c(C4H10)保持不变
C.反应热保持不变 D.正丁烷分解速率和乙烷消耗速率相等
(3)向密闭容器中充入正丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,随着温度升高,乙烯产率降低,可能的原因是____________。
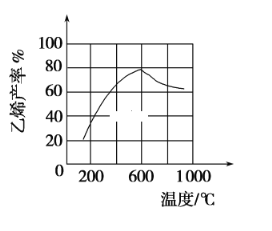
(4)在一定温度下向10 L恒容密闭容器中充入2 mol正丁烷,反应生成乙烯和乙烷,经过10 min达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10 min内乙烷的生成速率v(C2H6)=________ mol·L-1·min-1。
②上述条件下,正丁烷的平衡转化率为_______,该反应的平衡常数K为_____。
(5)丁烷空气燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的正极反应式为26CO2+13O2+52e-===26CO32-,则负极反应式为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中化学资源的综合开发利用,已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,如图为提取它们的主要步骤:
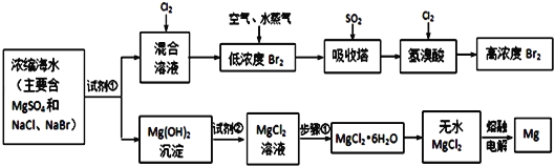
请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是_________。
(2)吸收塔中反应的离子方程式是_______,工业生产1mol Br2,理论上需要Cl2的物质的量为______ 。
(3)取10L海水经过提纯浓缩,向吸收塔吸收后的溶液中加入0.100mol/L AgNO3溶液8.0mL恰好完全反应,则海水中含溴的含量为______ mg/L(不考虑提纯过程中溴的损失)。
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用__________ (写化学式)。
(2)步骤①包括加热、蒸发、冷却、结晶、____________。
(3)通电时无水MgCl2在熔融状态下反应的化学方程式是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用下图所示装置从海水中提取CO2,有利于减少环境中温室气体的含量。下列说法正确的是
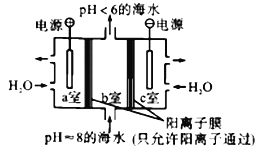
A. 通电后,a室的pH增大
B. 中间隔室发生的反应:HCO3-+H+==CO2↑+H2O,从而提取CO2
C. 阴极反应式为2H+-2e-==H2↑
D. 当电路中通过1mol电子的电量时,会有22.4LCO2气体产生
查看答案和解析>>
科目: 来源: 题型:
【题目】聚合硫酸铝铁(PAFS)是一种高效净水剂,其组成表示为[AlFe(OH)x(SO4)(3-![]() )]y。为检测PAFS中Al的含量,设计如下流程。
)]y。为检测PAFS中Al的含量,设计如下流程。

回答下列问题:
(1)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为__。
(2)PAFS中铁元素的化合价为_______;沉淀A的化学式为_________。
(3)如图所示,过滤操作中的一处错误是__________。
(4)生成沉淀B的离子方程式为______。
(5)PAFS中Al元素的质量分数为_______(用同m、n的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在空气中泄露的二氧化硫,会被氧化而形成硫酸雾或硫酸盐气溶胶,污染环境。工业上常用![]() 溶液吸收、活性炭还原等方法处理二氧化硫,以减小对空气的污染。
溶液吸收、活性炭还原等方法处理二氧化硫,以减小对空气的污染。
(1)写出用![]() 溶液吸收
溶液吸收![]() 的离子方程式____________。
的离子方程式____________。
(2)钠原子核外有______种能量不同的电子。写出硫原子最外层电子的轨道表示式____________。
(3)![]() 比
比![]() 稳定,请用分子结构的知识简述其理由。__________________
稳定,请用分子结构的知识简述其理由。__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com