
科目: 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是
A. 实验I、II、III中均涉及Fe3+被还原
B. 对比实验I、II说明白色沉淀的产生与铜粉的量有关
C. 实验II、III中加入蒸馏水后c(Cu2+)相同
D. 向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】H2在工农业生产过程中有着重要的作用。
I.(1)工业上用电解饱和食盐水的方法制取H2,该反应的离子方程式为___________。
(2)下图是为LiBH4/MgH2体系放氢焓变示意图,
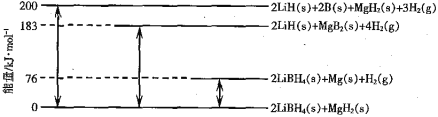
则由LiH、B与H2反应得到LiBH4的热化学方程式为_________。
Ⅱ.高铁酸钠(Na2FeO4)是一种新型多功能材料,工业上Na2FeO4制备方法是以纯铁棒与石墨电极为工作电极,用有隔膜的电解槽(如图所示),电解浓NaOH溶液制备高铁酸钠,化学方程式为:Fe+2NaOH+2H2O= Na2FeO4+2H2↑
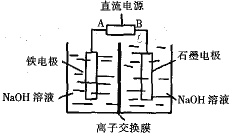
(3)A为电源_______极(填“正”或“负”),铁电极_____(填“能”或“不能”)换成石墨电极。
(4)石墨电极上发生的电极反应式为______。
(5)电解过程中可能存在副产物,左池有时会生成红褐色沉淀,此时只要加大电流强度,就可以使红褐色沉淀继续电解,转化为FeO42-,该过程的电极反应式为____
Ⅲ.(6)利用甲醇燃料电池进行电解的装置如图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后断开K,此时A、B两极上生成等物质的量的气体。
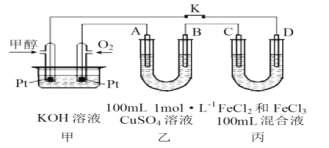
乙中B电极为_____(填“阴极”或“阳极”),该电极上生成的气体在标准状况下的体积为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Fe、Ni均为Ⅷ族元素,与C、N、O、P等组成的化合物有广泛的用途。回答下列问题:
(1)基态Ni2+的价层电子轨道表达式为________,C、N、O的第一电离能从小到大的顺序为________。
(2)N、P可形成一些复杂离子,如(CH3)3NH+、NO2+、PCl6-等。
①(CH3)3NH+ 中N原子的杂化类型为___,NO2+的空间构型为______________。
②PCl5是一种白色固体,在加压下于148℃时液化,形成一种能导电的熔体。熔体能导电的原因是___________。
(3)Fe、Ni易与CO形成配合物,Fe(CO)5中σ键与π键个数比为______,Ni(CO)4熔点-25℃,沸点43℃,不溶于水,溶于乙醇、苯等有机溶剂,Ni(CO)4为______晶体。
(4)FeO、NiO的晶体类型与结构和NaCl相同。
① 熔点FeO_____NiO(填“>”、“<”或“=”)。
② FeO 晶胞如下图,Fe2+的配位数为_______。
③ FeO在氧气中加热,部分Fe2+被氧化为Fe3+,晶体结构产生铁离子缺位的缺陷,其组成变为FexO(x<1),测得晶胞边长为a cm,密度为g·cm-3,则x=_______。
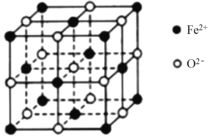
查看答案和解析>>
科目: 来源: 题型:
【题目】物质结构揭示物质构成的奥秘,请回答以下问题:
(1)元素A含有8个质子,10个中子的核素,用核素符号表示为______。元素B被科学家称“防癌之王”,与元素A同主族位于第四周期,元素B的名称为______,A和B的氢化物,沸点较高的是_____(填化学式)。
(2)CH4中共用电子对偏向C,SiH4中硅元素为+4价,则C、Si、H的电负性由大到小的顺序为______。
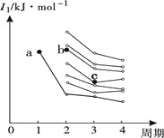
(3)如图是前四周期主族元素第一电离能梯度图,图中a点对应的元素为氢,则b点对应元素的未成对电子数为______,c点对应元素基态原子价电子排布式为_______。
(4)FeC13晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因是____。
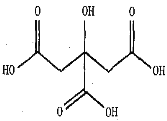
(5)水果中含有不同的果酸,其中柠檬、柑橘等水果中含有柠檬酸,柠檬酸的结构如下图。柠檬酸的晶体类型为_____,碳原子的杂化轨道类型为_____;柠檬酸晶体中含有的作用力有___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛合金材料已经广泛应用于国防、航天、医疗等领域。已知常温下钛(Ti)与酸、碱均不反应,高温下能被空气氧化。由钛铁矿(主要成分为FeO·TiO2)提取金属钛的主要流程如图所示。有关叙述错误的是( )
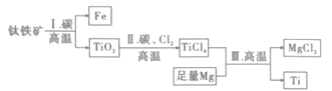
A.步骤Ⅰ、Ⅱ中的碳均作还原剂B.可用稀硫酸或稀盐酸除去金属钛中的少量镁
C.钛元素位于元素周期表中第ⅡB族 D.步骤Ⅲ需在氩气氛围中进行,防止金属被空气氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是
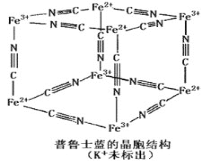
A. 化学式可以表示为KFe2(CN)6
B. 每一个立方体中平均含有24个π键
C. 普鲁士蓝不属于配位化合物
D. 每个Fe3+周围与之相邻的Fe2+离子有12个
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列三个化学反应均能发生:
X2+2W2+![]() 2X-+2W3+
2X-+2W3+
Z2+2X-![]() 2Z-+X2
2Z-+X2
2W3++2Y-![]() 2W2++Y2
2W2++Y2
则在相同条件下,下列三个反应也能发生的是( )
①Y2+2X-![]() 2Y-+X2 ②Z2+2Y-
2Y-+X2 ②Z2+2Y-![]() 2Z-+Y2 ③2W3++2Z-
2Z-+Y2 ③2W3++2Z-![]() 2W2++Z2
2W2++Z2
A. 只有① B. 只有② C. ①和② D. ②和③
查看答案和解析>>
科目: 来源: 题型:
【题目】氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是
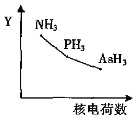
A. 相对分子质量B. 稳定性C. 沸点D. R-H键长
查看答案和解析>>
科目: 来源: 题型:
【题目】奈必洛尔是一种用于血管扩张的降血压药物,一种合成奈必洛尔中间体G的部分流程如下:
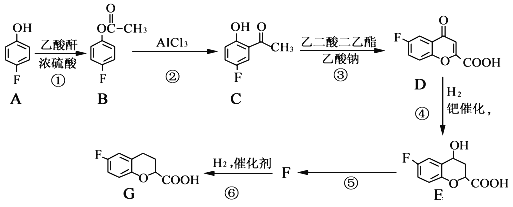
已知:乙酸酐的结构简式为![]() 。
。
请回答下列问题:
(1)A的名称是______;B中所含的含氧官能团的名称是______.
(2)G的分子式为______.
(3)反应⑤的化学方程式为______,该反应的反应类型是______.
(4)写出一种满足下列条件的E的同分异构体的结构简式:___________.
Ⅰ.苯环上只有三个取代基
Ⅱ.核磁共振氢谱图中只有4组吸收峰
Ⅲ.1 mol该物质与足量NaHCO3溶液反应生成2 molCO2
(5)根据已有知识并结合相关信息,写出以![]() 为原料制备的
为原料制备的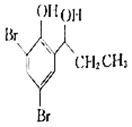 合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br
合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br ![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】中国海军航母建设正在有计划、有步骤向前推进。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为_______________________.
(2)航母甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中C原子杂化方式为______杂化,在有机物中C原子间可以形成双键,而硅烷中Si原子间难以形成双键的原因是_____________.
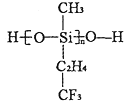
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是_________(填元素符号)
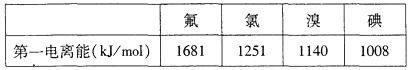
②根据价层电子对互斥理论,预测ClO的空间构型为___________形,写出一个ClO的等电子体的化学符号___________.
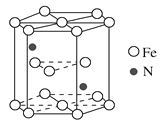
(4)海底金属软泥是在洋海底蕴藏着大量的资源,含有硅、铁、锰、锌等。某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为________________,若晶胞底边长为a nm,高为c nm,则这种磁性氮化铁的晶体密度为________g·cm3(用含a、c和NA的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com