
科目: 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列说法正确的是( )
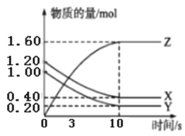
A.该反应的化学方程式为3X+Y![]() 2Z
2Z
B.3s时,正逆反应速率相等
C.平衡时X的浓度为0.40mol/L
D.10s时,该反应达到了最大限度
查看答案和解析>>
科目: 来源: 题型:
【题目】氨甲环酸(G)别名止血环酸,是一种已被广泛使用半个世纪的止血药,它的一种合成路线如下(部分反应条件和试剂略):
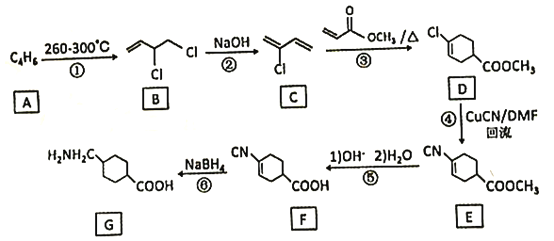
回答下列问题:
(1)A的结构简式是____。C的化学名称是_______。
(2)G在NaOH催化下发生双分子脱水形成仅含两个环的有机物,写出该反应的化学反应方程式____。
(3)①~⑥中属于取代反应的是_________。
(4)E中不含N原子的官能团名称为___________。
(5)氨甲环酸(G)的分子式为__________。
(6)满足以下条件的所有E的同分异构体有_____种。
a.含苯环 b.含硝基 c.苯环上只有两个取代基
(7)写出以![]() 和CH2=CHCOOCH2CH3为原料,制备
和CH2=CHCOOCH2CH3为原料,制备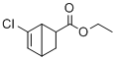 的合成路线:_______(无机试剂任性)
的合成路线:_______(无机试剂任性)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 在鸡蛋清溶液中分别加入饱和![]() 溶液,都会因盐析产生沉淀
溶液,都会因盐析产生沉淀
B. 油脂为高分子化合物,其饱和程度越大,熔点越低
C. ![]() 的水解产物是
的水解产物是![]() 和
和![]()
D. 麦芽糖及其水解产物均能与新制氢氧化铜悬浊液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验如果设计或操作不当,可能看不到预期的现象。下列关于实验现象的分析不正确的是( )
选项 | A | B | C | D |
装置 |
|
|
|
|
现象 | 量筒中未出现油状液体 | 试管中有黑色沉淀,但未出现银镜 | 试管中未看到白色沉淀 | NaOH溶液液面上 未看到油状液体 |
原因 | 甲烷与氯气未反应 | 反应未生成单质银 | 苯酚浓度 较大 | 产物水解 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】不考虑羟基与氯原子在同一个碳原子上时,有机物C4H9ClO能与Na反应放出氢气的共有![]() 不考虑立体异构
不考虑立体异构![]() ( )
( )
A. 8种B. 9种C. 10种D. 12种
查看答案和解析>>
科目: 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工业流程如下:
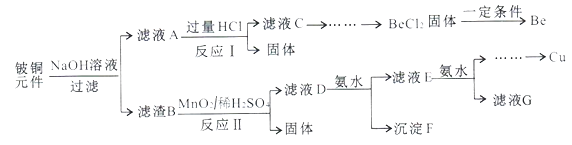
已知:i.铍、铝元素化学性质相似能形成BeO22-;ii.常温下部分难溶物的溶度积常数如下表:
难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
溶度积常数(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)用NaOH溶液溶解铍铜元件步骤中提高溶解率的措施是_______。(至少写出两种)滤液A的主要成分除NaOH外,还有_____(填化学式)。
(2)写出反应I中含铍化合物与过量盐酸反应的离子方程式_______,写出反应I中生成固体的化学方程式:________。
(3)滤液C中含NaCl、BeCl2和少量HCl。为提纯BeCl2,最合理的实验步骤顺序为____(填字母)。
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH
d.加入适量的HCl e.洗涤 f.过滤
(4)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应II中CuS发生反应的化学方程式:______。
(5)该小组从1kg该种旧铍铜元件中回收得到433g Cu,则该流程Cu的产率为_______(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】从海水中提取溴的工业流程如图:

(1)步骤I中将卤水酸化,再通入Cl2,是为了防止Cl2与碱反应,写出Cl2与碱反应的离子方程式_____。
(2)步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是__________。
(3)实验室保存液溴时,通常在盛液溴的试剂瓶中加少量的水,这与液溴的_____性质有关(填写序号)。
A.氧化性 B.还原性 C.挥发性 D.密度比水大
(4)步骤II中将吹出的溴蒸汽用纯碱溶液吸收时还有CO2生成,写出吸收时发生反应的离子方程式:___。
(5)步骤II中通入热空气吹出的Br2用纯碱溶液吸收前先经过NaBr溶液,其目的是______________。
(6)步骤III中蒸馏出工业溴后残留液的主要溶质是_______________。
(7)步骤III中若使用硝酸酸化,缺点是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中进行的反应C(s)+H2O(g)![]() CO(g)+H2(g),能使反应速率加快的措施有( )
CO(g)+H2(g),能使反应速率加快的措施有( )
①增加炭的量②升高温度③将炭粉碎④恒容通入水蒸气⑤通过减小容器体积增大压强⑥恒容通入N2
A.②③④⑤B.②③④⑤⑥C.①②③④⑤D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置略去)。
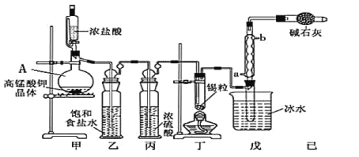
有关信息如下表

回答下列问题:
(1)甲装置中仪器A的名称为_________。
(2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为_____________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到______(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是: ①促进氯气与锡反应; ②_________。
(4)乙装置的作用 __________,如果缺少乙装置,可能发生的副反应的化学方程式为___________;己装置的作用是__________(填序号)
A.防止空气中CO2气体进入戊装置
B.除去未反应的氯气,防止污染空气
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.04g SnCl4,则SnCl4的产率为________。(保留2位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知断开 1mol Cl2(g)中Cl-Cl键需要吸收243kJ能量,根据能量变化示意图,下列说法或热化学方程式正确的是( )
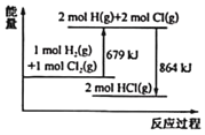
A.H2(g)+Cl2(g) = 2HCl(g) ΔH= + 185 kJ·mol-1
B.生成1mol H2(g)中的H-H键放出 121.5 kJ 能量
C.断开1mol HCl(g)中的H-C1键要吸收 864 kJ 能量
D.HCl(g) =![]() H2(g)+
H2(g)+![]() Cl2(g) ΔH= + 92.5kJ·mol-1
Cl2(g) ΔH= + 92.5kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com