
科目: 来源: 题型:
【题目】已知某样品甲为仅含有三种元素的纯净物,不溶于水,能溶于稀盐酸,为探究其组成和性质,设计并完成如下实验:
①将 21.5g 该物质溶解于 600mL 1mol·L-1 盐酸中,得到黄色溶液乙,将溶液乙分成两等份;
②将其中一份加热蒸干、灼烧,得到 8.0g 红棕色固体丙;
③向另一份溶液中加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥得到白色沉淀 57.4g。请回答:
(1)写出实验③中检出离子的结构示意图_____。
(2)样品甲中所含的三种元素为_____。
(3)写出实验①中反应的离子方程式_____。
(4)写出实验②中,检出固体丙中所含阳离子的实验方法_____。(写出实验操作、现象及结论)。
查看答案和解析>>
科目: 来源: 题型:
【题目】1-溴丙烷是一种重要的有机合成中间体。实验室用丙醇、浓硫酸和溴化钠反应来制备少量1-溴丙烷。其反应原理、实验的装置和主要步骤如下:H2SO4(浓)+NaBr ![]() NaHSO4+HBr↑ CH3CH2CH2OH+HBr
NaHSO4+HBr↑ CH3CH2CH2OH+HBr ![]() CH3CH2CH2Br+H2O
CH3CH2CH2Br+H2O

步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓![]() ;冷却至室温,搅拌下加入24g NaBr。
;冷却至室温,搅拌下加入24g NaBr。
步骤2:如图所示连接实验装置,缓慢加热,直到没有油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用![]() 溶液
溶液 ![]() 洗涤,分液,得粗产品,进一步提纯得
洗涤,分液,得粗产品,进一步提纯得![]() 溴丙烷。有关数据见下表:
溴丙烷。有关数据见下表:

(1)仪器A的名称的是_________;加入搅拌磁子的目的是搅拌和___________。
(2)反应时生成的主要有机副产物有丙烯、_________和___________。(填物质名称)
(3)反应过程中可以观察到A的上方出现红棕色气体,其分子式为__________。
(4)给A加热的目的是_______。
(5)步骡2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是_______,同时可以观察到的现象是_____。
(6) 步骤4中三次洗涤分别洗去的主要杂质①__________②___________③___________ .
(7)步骤4中![]() 的
的![]() 溶液还可以用下列哪个试剂代替_____(填字母序号)
溶液还可以用下列哪个试剂代替_____(填字母序号)
A.NaOH溶液 ![]() 溶液 C.
溶液 C.![]() 溶液 D.
溶液 D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】控制和治理CO2是解决温室效应及能源问题的有效途径。
已知:H2(g)和CH3OH(l)的标准燃烧热分別为△H=akJmol-1和△H=bkJmol-1
(1)研究表明,在Cu/ZnO催化剂存在下,CO2和H2 反应生成液态甲醇和液态水,该反应的热化学方程式为_________。
(2)已知:2CO2(g)+ 6H2(g)C2H4(g)+4H2O(g)△H,在两个固定容积均为1L的密闭容器中以不同的氢碳比[![]() ]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。
]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。

① X_______________(填“>”“<”或“=”) 2.0 ;
②若起始加入的CO2、H2的物质的量分別为1mol和2mol,计算P点时的化学平衡常数K=____________。
③比较P点和Q点的化学平衡常数:KP_________KQ(填“>”“<”或“=”),理由是__________________。
④一定温度下在体积为VL的容器中进行该反应,下列一定能说明反应达到平衡状态的是_______________(填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(CO2)=v逆(C2H4)
D.容器内混合气体的密度不再变化
(3)以CH3OH作燃料,以NaOH溶液作电解质溶液形成的燃料电池,电池工作时,溶液中的阴离子向电池的哪一极定向移动(填写电极名称)________;写出负极的电极反应式_________.
(4)常温下,若在![]() 硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的![]() 时,
时,![]() ____
____![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】按照要求填写下列空白
(1)同一条件下,下列关系不正确的是________________。(填字母序号)
A. 沸点:乙烷>乙醇
B . 与金属钠反应的剧烈程度:乙酸![]() 苯酚
苯酚![]() 乙醇
乙醇
C . 相对密度:1-丁烯<1-庚烯
D .在水中的溶解度:丙三醇![]()
(2)2-氯乙醛(ClCH2CHO)与新制的氢氧化铜悬浊液反应的化学方程式为___________________。
(3)聚丙烯的链节为_______________;聚碳酸酯 的透光率良好,现在用绿色化学原料碳酸二甲酯
的透光率良好,现在用绿色化学原料碳酸二甲酯 与__________________。(填字母序号)(A.二卤化物 B.二酚类 C.二醛类 D.二烯类)缩合聚合而成,写出该缩聚反应的方程式________________________。
与__________________。(填字母序号)(A.二卤化物 B.二酚类 C.二醛类 D.二烯类)缩合聚合而成,写出该缩聚反应的方程式________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】炼制石油能得到许多有机化合物,相关物质的转化关系如下图所示,其中A的产量是衡量一个国家石油化工发展水平的重要标志,标况下,B气体的密度为0.71gL-1,C是一种红色固体单质,D是一种混合气体。
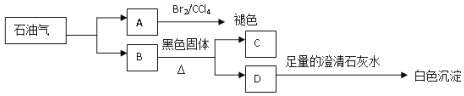
请回答:
(1)A的结构简式为__,A与溴的四氯化碳溶液的反应类型为___。
(2)B与CuO反应的化学方程式___。
(3)下列说法不正确是__。
a.A中所有原子共平面
b.A与溴的四氯化碳溶液反应现象,和A与溴水反应的现象完全相同
c.等物质的量A与B混合物在足量氧气中完全燃烧,生成水的物质的量相等
d.B是引起温室效应的气体之一
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯的产量通常用来衡量一个国家的石油化工水平,某化学实验小组为了探究石蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如下实验方案:
(查阅资料可知:乙烯与酸性高锰酸钾溶液反应产生二氧化碳。)
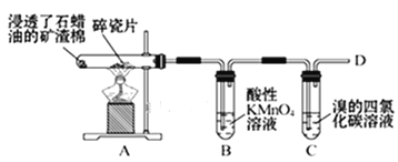
(1)乙烯的结构式是___。
(2)B中实验现象:___。
(3)C中发生反应的化学方程式:__,反应类型:___。
(4)通过上述实验探究可知,除去乙烷中混有的乙烯,可以选择的试剂是___。
A.水 B.溴水
C.氢氧化钠溶液 D.酸性高锰酸钾溶液
(5)关于乙烯,下列说法中不正确的是___。
A.聚乙烯塑料可以用做食品包装袋
B.乙烯在一定条件下可以和水反应制乙醇
C.乙烯分子中所有原子不共面
D.乙烯是一种植物生长调节剂,可以延长果实和花朵的成熟期
查看答案和解析>>
科目: 来源: 题型:
【题目】以废旧电路板为原料制备硫酸铜可以变废为宝。下图是某科研小组设计的工艺流程(流程中 RH 为萃取剂),下列说法不正确的是
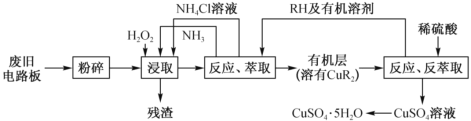
A.“粉碎”可以增大反应的接触面积,提高浸取速率和铜的浸取率
B.“浸取”发生的离子反应为 Cu+H2O2+2NH3 +2NH4+=Cu(NH3)42++2H2O
C.工艺流程中循环使用的物质有 NH3、NH4Cl、RH 和有机溶剂
D.从硫酸铜溶液获得纯净的硫酸铜晶体的操作是:加入适量乙醇,蒸发浓缩、冷却结晶、过滤、热水洗涤、干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于电解质溶液的叙述正确的是( )
A. 常温下电离常数为![]() 的酸HA溶液中
的酸HA溶液中![]()
B. 向0.1![]() 的氨水中加入少量硫酸铵固体,则溶液中
的氨水中加入少量硫酸铵固体,则溶液中 增大
增大
C. 将饱和![]() 溶液加入到饱和石灰水中,有白色沉淀产生,说明
溶液加入到饱和石灰水中,有白色沉淀产生,说明![]() 大于
大于![]()
D. 0.2![]() 溶液与0.1
溶液与0.1![]() 溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH)
溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH)
查看答案和解析>>
科目: 来源: 题型:
【题目】NaOH 溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A 的 Ka1=1.1×103 ,Ka2=3.9×106)溶液, 混合溶液的相对导电能力变化曲线如图所示,其中b 点为反应终点。下列叙述错误的是( )
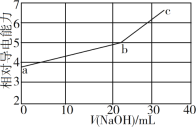
A.a 点溶液 pH<7
B.Na+与A2的导电能力之和大于 HA
C.b 点溶液中:c(H+)+c(HA-) +c(H2A)=c (OH-)
D.c 点 溶 液 中 :c(Na+)>c(K+)> c(A2)>c(OH)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】炔烃的偶联反应在开发新型发光材料、超分子等领域有重要研究价值。乙炔发生的偶联反应为 2CH≡CH ![]() CH≡CC≡CH+H2。乙炔偶联反应过程中能量变化如图甲中曲线Ⅰ所示,曲线Ⅱ为改变某一条件的能量变化。下列说法不正确的是( )
CH≡CC≡CH+H2。乙炔偶联反应过程中能量变化如图甲中曲线Ⅰ所示,曲线Ⅱ为改变某一条件的能量变化。下列说法不正确的是( )
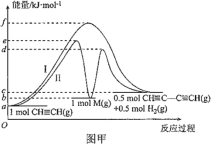
A.曲线Ⅰ,反应物的总键能大于生成物的总键能
B.曲线Ⅱ改变的条件是加入了催化剂
C.曲线Ⅱ对应条件下,第一步反应的 ΔH=+(b-a)kJ·mol-1
D.曲线Ⅱ对应条件下,决定总反应速率的大小是第二步反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com