
科目: 来源: 题型:
【题目】现有常温条件下浓度均为0.1 molL-1的甲、乙、丙、丁四种溶液,甲为NaOH溶液,乙为HCl溶液,丙为CH3COOH溶液,丁为氨水,已知Ka(CH3COOH)=Kb(NH3H2O)试回答下列问题:
(1)甲、丁种溶液中由水电离出的c(OH)的大小关系为甲___丁(填“大于”“小于”或“等于”)。
(2)将一定体积的甲与乙混合,所得溶液pH=12,则二者的体积比为v甲∶v乙=___。
(3)某同学用甲滴定丙溶液、乙滴定丁溶液,得到如图所示两条滴定曲线,请完成有关问题:
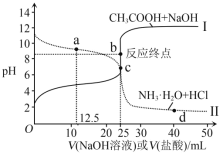
①乙溶液滴定丁溶液最适合的指示剂是___;甲溶液滴定丙溶液,选用酚酞为指示剂,则达到滴定终点的标志是___。
②计算滴定至b点时,c(CH3COOH)+c(CH3COO-)=___molL-1
③向氨水中滴加盐酸至a点,溶液中离子浓度从大到小的顺序为___,若加盐酸vmL时,溶液恰好呈中性,用含v的代数式表示出Kb=___(不考虑溶液混合体积变化)。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是 ( )
A. 可验证HCl气体在水中的溶解性
可验证HCl气体在水中的溶解性
B.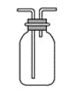 可用于收集H2、NH3、Cl2、HCl、NO2、NO等
可用于收集H2、NH3、Cl2、HCl、NO2、NO等
C.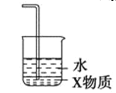 中X为四氯化碳,可用于氨气或氯化氢的尾气处理
中X为四氯化碳,可用于氨气或氯化氢的尾气处理
D.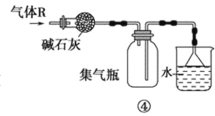 可用于干燥、收集氨气,并吸收多余的氨气
可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目: 来源: 题型:
【题目】Cu2O是重要的催化剂和化工原料,工业上制备Cu2O的主要反应如下:
Ⅰ.C(s)+CO2(g)![]() 2CO(g) ΔH=+172.5kJ·mol-1
2CO(g) ΔH=+172.5kJ·mol-1
Ⅱ.CO(g)+2CuO(s)![]() Cu2O(s)+CO2(g) ΔH=-138.0 kJ·mol-1
Cu2O(s)+CO2(g) ΔH=-138.0 kJ·mol-1
请回答:
(1)一定温度下,向5L恒容密闭容器中加入1molCO和2molCuO,发生反应Ⅱ,2min时达到平衡,测得容器中CuO的物质的量为0.5mol。
①0-2min内,用CO表示的反应速率v(CO)=___。
②CO2的平衡体积分数φ=___。
(2)向5L密闭容器中加入1molC和1molCO2,发生反应Ⅰ。CO2、CO的平衡分压(p)与温度(T)的关系如图所示(平衡分压=物质的量分数×总压强)。
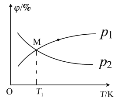
①能表示CO2的平衡分压与温度关系的曲线为___(填"p1”或“p2”),理由是___。
②温度为T1时,该反应的平衡常数K=___;温度升高,K___(填“变小”、“变大”或“不变”)
③实验测得,v正=v(CO2)消耗=k正c(CO2),v逆=v(CO)消耗=k逆c2 (CO),k正、k逆为速率常数,受温度影响,则温度为T1时,k正/k逆=___。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)镍与CO反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2除CO。已知:

则用SO2除去CO的热化学方程式为___。
(2)含乙酸钠和对氯酚(![]() )的废水可以利用微生物电池除去,其原理如图所示:
)的废水可以利用微生物电池除去,其原理如图所示:

①B是电池的___极(填“正”或“负”);
②A极的电极反应式为____。
(3)利用双模三室电解法不仅可处理含NiCl2的废水,还可回收金属镍,其装置如图所示。
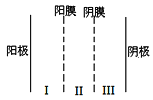
①两端电解质溶液分别为含NiCl2的废水和NaOH溶液,其中含NiCl2的废水应进___(填“Ⅰ”“Ⅱ”“Ⅲ”,下同)室。
②阳极的电极反应式为___。
(4)某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol·L-1,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。
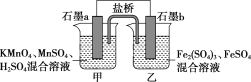
回答下列问题:
①此原电池的正极是石墨___(填“a”或“b”),发生___反应。
②电池工作时,盐桥中的SO42-移向____(填“甲”或“乙”)烧杯。
③甲烧杯中的电极反应式为____;
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各项比较中前者高于(或大于或强于)后者的是( )
A. PH3和AsH3的熔点
B. Br2在水中的溶解度和Br2在CCl4溶液中的溶解度
C. 对羟基苯甲醛(![]() )和邻羟基苯甲醛(
)和邻羟基苯甲醛(![]() )的沸点
)的沸点
D. HClO和HClO4的酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组利用下图装置制取少量氯化铝,已知氯化铝熔沸点都很低(178℃升华),且易水解。下列说法中完全正确的一组是
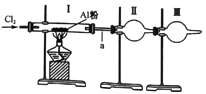
①氯气中含的水蒸气和氯化氢可通过盛有苛性钠的干燥管除去
②装置I中充满黄绿色气体后,再加热盛有A铝粉的硬质玻璃管
③装置II是收集装置,用于收集氯化铝
④装置III可盛放碱石灰也可盛放无水氯化钙,二者的作用相同
⑤a处使用较粗的导气管实验时更安全
A. ①② B. ②③⑤ C. ①④ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素W、X、Y、Z,它们在周期表中位置如图所示,X的一种氢化物与其最高价氧化物对应水化物反应生成盐。下列说法正确的是

A.T元素单质具有半导体的特性,T与Y元素可形成两种化合物TY和![]()
B.由Y、Z和氢三种元素形成的化合物中,Z的化合价越高氧化性越强
C.W的氧化物是酸性氧化物,能与碱、水反应,不能与酸反应
D.X的氢化物分子中所有原子均满足8电子结构
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是108.1°,下列有关N(NO2)3的说法不正确的是( )

A. N(NO2)3分子中既含极性键又含非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 15.2 g该物质含有6.02×1023个原子
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中不正确的是( )

A. Y的价层电子排布式可能是ns2np4
B. 四种元素所形成的氢化物中,沸点最高的可能是Y的氢化物
C. Y、Z之间可形成离子化合物
D. X、Z、W的最高价氧化物所对应的水化物可能都是强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com