
科目: 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】用煤化工产品![]() 合成高分子材料I的路线如下:
合成高分子材料I的路线如下:
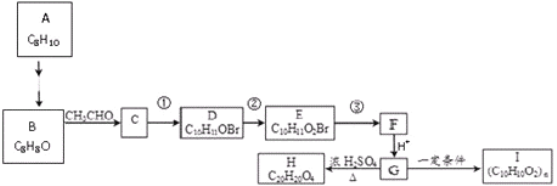
已知:(1)B、C、D都能发生银镜反应,G的结构简式为
(2)![]()
![]()
根据题意完成下列填空:
(1)A的结构简式为__________________。
(2)实验空由A制得B可以经过三步反应,第一步的反应试剂及条件为![]() /光照,第二步是水解反应,则第三步的化学反应方程式为____________________。
/光照,第二步是水解反应,则第三步的化学反应方程式为____________________。
(3)①的反应类型为_______________反应。
(4)③的试剂与条件为__________________________。
(5)I的结构简式为___________;请写出一个符合下列条件的G的同分异构体的结构简式____________。
①能发生银镜反应 ②能发生水解反应
③苯环上一氯取代物只有一种 ④羟基不与苯环直接相连
(6)由乙醇为原料可以合成有机化工原料1-丁醇(![]() ),写出其合成路线________________。(合成路线需用的表示方式为:
),写出其合成路线________________。(合成路线需用的表示方式为:![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
①晶体中分子间作用力越大,分子越稳定 ②原子晶体中共价键越强,熔点越高 ③干冰是CO2分子通过氢键和分子间作用力有规则排列成的分子晶体 ④在Na2O和Na2O2晶体中,阴、阳离子数之比相等 ⑤正四面体构型的分子,键角都是109°28′,其晶体类型可能是原子晶体或分子晶体 ⑥分子晶体中都含有化学键 ⑦含4.8 g碳元素的金刚石晶体中的共价键的物质的量为0.8 mol
A. ①②③④⑤ B. ②④⑦ C. ⑤⑥⑦ D. ③④⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )
A.单位时间生成nmol的A2同时生成nmol的AB
B.容器内的压强不随时间变化
C.单位时间生成2nmol的AB同时生成nmol的B2
D.单位时间生成nmol的A2同时生成nmol的B2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知以下反应中的四种物质由三种元素组成,其中a的分子立体构型为正四面体形,组成a物质的两种元素的原子序数之和小于10,组成b物质的元素为第三周期元素。下列判断正确的是

A. 四种分子中的化学键均是极性键
B. a、c分子中中心原子均采用sp3杂化
C. 四种分子中既有σ键,又有π键
D. b、d分子中共价键的键能:b>d
查看答案和解析>>
科目: 来源: 题型:
【题目】共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量。如H-H键的键能是436kJ/mol,H—Cl键的键能是431kJ/mol,Cl—Cl键的键能是247 kJ /mol,H2和Cl2反应生成1molHCl放出的热量是( )
A.431kJB.179kJC.89.5kJD.以上说法都不对
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表中的一部分,表中列出8种元素在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ④ | ⑥ | ||||||
3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
(1)在①~⑧元素中化学性质最不活泼的元素的名称是____,金属性最强的元素的名称是____。
(2)③、④、⑥三种元素中的原子半径最小的是_____________(填元素符号)。
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是____(用离子符号填写)。
(4)④与⑥形成的化合物的电子式为_____________。
(5)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )
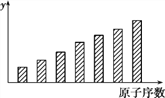
A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室中根据![]() 已知
已知![]() 熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备
熔点是16.6℃,沸点44.4℃。设计如下图所示的实验装置制备![]() 固体。
固体。
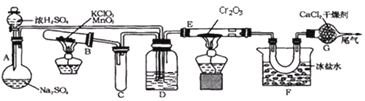
(1)实验开始时,先点燃的酒精灯是_________(填编号)。
(2)装置D中浓硫酸的作用除了混合气体并观察气体流速外还有___________。
(3)装置F的作用是____________________。
(4)由于可逆反应,所以从E管出来的气体中含有![]() 、
、![]() 。为了证明含有
。为了证明含有![]() 可以将该气体通入________(填下列编号,下同)、证明含有
可以将该气体通入________(填下列编号,下同)、证明含有![]() 可以将该气体通入_____________。
可以将该气体通入_____________。
A.品红 B.溴水 C.![]() 溶液 D.
溶液 D.![]() 溶液
溶液
(5)如果没有装置G,则F中可能看到_________________。
(6)从装置G导出的尾气常可以用烧碱或石灰乳吸收。请写出用足量烧碱吸收尾气的离子方程式为:_________________________________________________________。
(7)尾气常采用烧碱或石灰乳吸收,请分析比较两种吸收剂吸收的优点__________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为测试一铁片中铁元素的含量,某课外活动小组提出下面方案并进行了实验。将0.200g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用![]() 的
的![]() 溶液滴定,达到终点时消耗了
溶液滴定,达到终点时消耗了![]() 溶液。
溶液。
(1)配平以下方程式并标出电子转移的方向与数目____________________。
![]()
(2)滴定到终点时的现象为____________________,铁片中铁元素的质量分数为_______________________。
(3)高锰酸钾溶液往往用硫酸酸化而不用盐酸酸化,原因是:_____________。
(4)![]() 溶液呈酸性,加硫酸后
溶液呈酸性,加硫酸后![]() 增加,请结合离子方程式并利用化学平衡移动理论解释:_____________________________。
增加,请结合离子方程式并利用化学平衡移动理论解释:_____________________________。
(5)高锰酸钾在化学品生产中,广泛用作为氧化剂。可以氧化![]() 、
、![]() 、
、![]() 、
、![]() 等多种物质,如
等多种物质,如![]() ,试推测空格上应填物质的化学式为________。
,试推测空格上应填物质的化学式为________。
(6)上述反应在恒温下进行,该过程中会明显看到先慢后快的反应,原因可能是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com