
科目: 来源: 题型:
【题目】一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
(1)下列描述能说明该可逆反应达到化学平衡状态的有___。
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3molH-H键断裂,有6molN-H键形成
D.c(N2):c(H2):c(NH3)=1:3:2
E.NH3的质量分数不再改变
(2)若起始时向容器中充入10mol·L-1的N2和15mol·L-1的H2,10min时测得容器内NH3的浓度为1.5mol·L-1。10min内用N2表示的反应速率为___;此时H2的转化率为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸和氧化铁反应的离子方程式是_________;铜和上述反应得到的物质反应的离子方程式是_________;向混合溶液中通入热空气的反应的离子方程式是_________;分离蓝色滤液和红褐色沉淀的实验操作是_________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

①吸收塔中发生反应的化学方程式是_________。
②检验硫酸铵中的NH4+的离子方程式是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O。正极电极反应式为__,随着反应的进行,正极附近溶液的酸性将__。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为__,当线路中转移0.4mol电子时,则被腐蚀铜的质量为__g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为__。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
(4)如图是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,A极为电源(填“正”或“负”)___极,写出A极的电极反应式:___。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列根据实验操作和实验现象所得出的结论,正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向亚硫酸钠试样中滴入盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 试样已经氧化变质 |
B | 乙醇和浓硫酸混合加热至170℃,将产生气体通入酸性KMnO4溶液 | 紫红色褪去 | 使溶液褪色的是乙烯 |
C | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
D | 将炽热的木炭与浓硝酸混合所得气体通入澄清石灰水中 | 澄清石灰水不变浑浊 | 验证碳的氧化产物为CO |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应2NO2![]() 2NO+O2在恒容密闭容器中反应,不能判断此反应达到最大限度的标志是( )
2NO+O2在恒容密闭容器中反应,不能判断此反应达到最大限度的标志是( )
A. 单位时间内生成n mol O2 的同时,生成2n molNO2 B. 混合气体的平均相对分子质量不再改变
C. 混合气体的颜色不再改变 D. NO2, NO, O2的速率之比是2:2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】可降解聚合物P 的合成路线如下:
的合成路线如下:
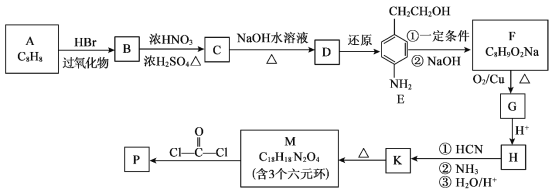
已知: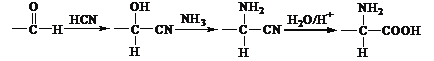
请回答:
(1)A为芳香烃,其结构简式为___________。
(2) E 中含氧官能团名称为 ___________。
(3) B→C 的反应类型为__________。
(4) C → D的方程式为________________。
(5) M 的结构简式为_______________ 。
(6)设计以A为原料,利用上述信息,合成高聚物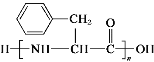 的路线: _____。( 用反应流程图表示,并注明反应条件 )
的路线: _____。( 用反应流程图表示,并注明反应条件 )
查看答案和解析>>
科目: 来源: 题型:
【题目】NO2 是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2 进行回收利用,装置中a、b均为多孔石墨电极。下列说法正确的是
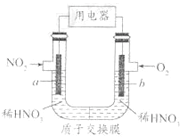
A. a 为电池的负极,发生还原反应
B. 电子流向:a 电极→用电器→b 电极→溶液→a 电极
C. 一段时间后,b 极附近HNO3浓度增大
D. 电池总反应为4NO2 +O2 +2H2O= 4HNO3
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍,Z最外层电子数等于最内层电了数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体。下列说法正确的是
A. Y的最高价氧化物对成水化物的酸性比W的强
B. W的气态氢化物比X的稳定
C. 离子半径的大小顺序:r(w)>r(X)>r(Y)>(Z)
D. XY2与ZY2中的化学键类型相同
查看答案和解析>>
科目: 来源: 题型:
【题目】铈是稀土元素,氢氧化铈[Ce(OH)4]是一种重要的氢氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2),某课题组以此粉末为原料回收铈,设计实验流程如下:
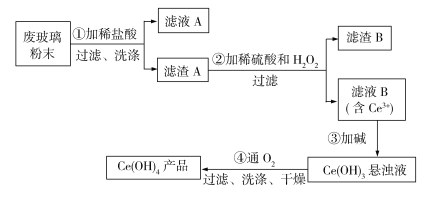
下列说法不正确的是
A.过程①中发生的反应是:Fe2O3+6H+![]() 2Fe3++3H2O
2Fe3++3H2O
B.过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒
C.过程②中有O2生成
D.过程④中发生的反应属于置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.11 g硫化钾和过氧化钾的混合物,含有的离子数目为0.4NA
B.28 g聚乙烯(![]() )含有的质子数目为16NA
)含有的质子数目为16NA
C.将标准状况下224 mL SO2溶于水制成100 mL溶液,H2SO3、![]() 、
、![]() 三者数目之和为0.01NA
三者数目之和为0.01NA
D.含63 g HNO3的浓硝酸与足量铜完全反应,转移电子数目为0.50NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com