
科目: 来源: 题型:
【题目】下列有机反应属于加成反应的是
A. C3H8 + 5O2 ![]() 3CO2 + 4H2O
3CO2 + 4H2O
B. CH2 = CH2 + Br2 → ![]()
C. 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
D. ![]() + HNO3
+ HNO3 ![]()
![]() + H2O
+ H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,反应N2(g)+3H2(g) ![]() 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A. N2、H2和NH3的质量分数不再改变
B. c(N2)∶c(H2)∶c(NH3)=1∶3∶2
C. 断裂1 mol N≡N键的同时,形成6 mol N—H键
D. N2与H2的物质的量之和是NH3的物质的量的2倍
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2 + 4H2![]() CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是
CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是
A. 适当升温能加快反应速率B. 催化剂对反应速率无影响
C. 达到平衡时,正反应速率为0D. 达到平衡时,CO2能100%转化为CH4
查看答案和解析>>
科目: 来源: 题型:
【题目】已知一定温度时:2SO2(g)+O2(g)![]() 2SO3(g),当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密闭容器中通入2mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
2SO3(g),当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密闭容器中通入2mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
A.Q=197 kJ B.Q<197×2 kJ C.Q<197 kJ D.Q>197 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】为了确认电解质溶液中部分离子相互间能否发生反应,及离子反应发生的条件,做如表四组实验:
编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
实验 |
|
|
|
|
(1)实验Ⅰ的现象________,写出反应的离子方程式________。
(2)实验Ⅱ的目的是________。
(3)实验Ⅲ的现象证明了溶液中的________两种离子之间发生了化学反应。
(4)实验Ⅳ中发生反应的离子方程式是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)现有下列几种有机物:①乙炔、②乙醇、③乙醛、④乙酸、⑤甲酸乙酯、⑥苯酚、⑦溴乙烷。其中: 能与 Na2CO3 溶液反应产生气泡的是___(填序号,下同);遇氯化铁溶液呈紫色的是________;能发生银镜反应的是_____;不能使酸性 KMnO4 溶液褪色的是______。
(2)按要求写出下列反应方程式
①实验室制取乙炔:____________
②实验室制取乙烯:________
查看答案和解析>>
科目: 来源: 题型:
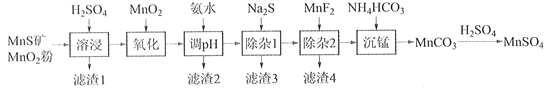
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnz2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中对离子方程式的评价合理的是
选项 | 化学反应及其离子方程式 | 评价 |
A | H2SO4溶液与Ba(OH)2溶液反应: H++ SO42-+Ba2++OH | 正确 |
B | 向碳酸镁浊液中加入足量稀盐酸: CO32-+2H+ | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O | 正确 |
D | 向NaOH溶液中通入少量CO2反应:OH+CO2 | 正确 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】电解Na2CO3溶液的工作原理如图所示。下列说法错误的是

A.A为电源的正极
B.X为氢气
C.工作时,Na+向左室迁移
D.阳极的电极反应式为4CO32-+2H2O-4e-=4HCO3-+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】企鹅酮的化学式C10H14O,因为结构类似企鹅,因此命名为企鹅酮(见图)。下列有关企鹅酮的说法正确的是

A.分子式为C10H16O
B.1 mol企鹅酮分子最多可以和2 mol氢气加成
C.可使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同
D.企鹅酮的同分异构体众多,其中遇Fe3+显色且苯环上有两个支链的结构共有12种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com