
科目: 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、Al2O3、Fe、SiO2等)制备草酸钴晶体(CoC2O4·2H2O)的流程如下:
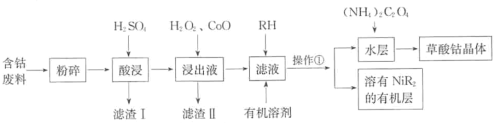
已知:①草酸钴晶体难溶于水:②RH为有机物(难电离)。
回答下列问题:
(1)酸浸时钴溶解反应的化学方程式为_______,浸出液中加入H2O2后发生反应的离子方程式为______。
(2)加入氧化钴的目的是_______,滤渣的II主要成分是_______。
(3)操作①为____________(填操作名称)。
(4)已知:NH3·H2O![]() NH4++OH- Kb=1.8×10-5;
NH4++OH- Kb=1.8×10-5;
H2C2O4![]() H ++HC2O 4- Ka1=5.4×10-2
H ++HC2O 4- Ka1=5.4×10-2
HC2O4-![]() H ++C2O42- Ka2=5.4×10-5
H ++C2O42- Ka2=5.4×10-5
该流程中所用(NH4)2C2O4溶液的pH_________(填“>”“<"或"一")7.
(5)钴的含氧酸盐受热分解最终产物多为氧化物,已知18.3g CoC2O4·2H2O热分解质量变化过程如图所示(其中600 °C以前是隔绝空气加热,6000 °C以后是在空气中加热),A、B、C均为纯净物。

①A点对应物质的化学式为________________
②B →C反应的化学方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向1 L 0.1 mol·L-1 NH4Cl溶液中,不断加入固体NaOH后,NH![]() 与NH3 · H2O的变化趋势如下图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
与NH3 · H2O的变化趋势如下图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )

A. 在M点时,n(OH-)-n(H+)=(a-0.05) mol
B. 随着NaOH的加入,![]() 不断增大
不断增大
C. M点溶液中水的电离程度比原溶液小
D. 当n(NaOH)=0.1 mol时,c(OH-)>c(Cl-)-c(NH3·H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
![]()
A. 灼烧过程中使用的玻璃仪器有酒精灯、烧杯、玻璃棒
B. 氧化过程中发生反应的离子方程式为 2I-+H2O2 =I2+2OH-
C. 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明海带中含有碘单质
D. 分液时,先打开活塞放出下层液体,再关闭活塞从上口倒出上层液体
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应A2+B2 = 2AB的能量变化如图所示,则下列说法正确的是
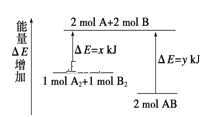
A.该反应是吸热反应
B.断裂 1molA-A 键和 1molB-B 键能放出xkJ 的能量
C.2mol AB 的总能量高于1mol A2和1mol B2和的总能量
D.断裂 2mol A-B 键需要吸收ykJ 的能量
查看答案和解析>>
科目: 来源: 题型:
【题目】将1 mol CH4和适量的氧气在密闭容器中点燃,充分反应后,甲烷和氧气均无剩余,且产物均为气体(101 kPa,120℃),其总质量为72 g,下列有关叙述不正确的是( )
A.产物的平均摩尔质量为24 g/mol
B.反应中消耗的氧气为56 g
C.若将产物通过浓硫酸充分吸收后恢复至(101 kPa,120℃),则压强变为原来的三分之一
D.若将产物通过碱石灰,则可全被吸收,若通过浓硫酸,则不能被完全吸收
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸铜是一种常见的化工产品,它在纺织、印染、医药、化工、电镀以及木材和纸张的防腐等方面有极其广泛的用途。实验室制备硫酸铜的步骤如下:
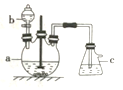
①在仪器a中先加入20g铜片、60 mL水,再缓缓加入17 mL浓硫酸:在仪器b中加入39 mL浓硝酸;在仪器c中加入20%的石灰乳150 mL。
②从仪器b中放出约5mL浓硝酸,开动搅拌器然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热。
③将仪器a中的液体倒出,取出未反应完的铜片溶液冷却至室温.析出蓝色晶体.回答下列问题:
(1)将仪器b中液体滴入仪器a中的具体操作是__________。
(2)写出装置a中生成CuSO4的化学方程式:_______。
(3)步骤②电炉加热直至仪器a中的红棕色气体完全消失,此时会产生的气体是______,该气体无法直接被石灰乳吸收,为防止空气污染,请画出该气体的吸收装置(标明所用试剂及气流方向)______。
(4)通过本实验制取的硫酸铜晶体中常含有少量Cu(NO3)2,可来用重结晶法进行提纯,检验Cu(NO3)2是否被除净的方法是_______。
(5)工业上也常采用将铜在450 °C左右焙烧,再与一定浓度的硫酸反应制取硫酸铜的方法,对比分析本实验采用的硝酸氧化法制取CuSO4的优点是_______。
(6)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成100 mL溶液,每次取20.00 mL用c mol·L-1EDTA(H2Y )标准溶液滴定至终点,平行滴定3次,平均消耗EDTA溶液b mL,滴定反应为Cu2++H2Y =CuY +2H+,蓝色晶体中Cu2+质量分数![]() _____%.
_____%.
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,发现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
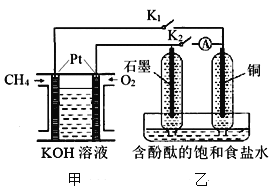
A. 断开K2,闭合K1时,石墨电极上的电极反应式为:2 H++ 2e-=H2↑
B. 断开K1,闭合K2时,铜电极上的电极反应式为:Cl2 + 2e-=2Cl-
C. 甲装置属于燃料电池,该电池正极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
D. 甲烷燃料电池的总电极反应式为:CH4+2O2 +2NaOH=Na2CO3+3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%
查看答案和解析>>
科目: 来源: 题型:
【题目】图为元素在生物体内的含量分布情况,下列表述错误的是

A. P、S、K、Ca、Zn属于大量元素
B. 在非生物界中都能找到,体现生物界与非生物界的统一性
C. Ⅱ和Ⅲ为生物体的必需元素,一旦缺乏就可能会导致相应的病症
D. Ⅲ含量虽少,却是生物体正常生命活动不可缺少的
查看答案和解析>>
科目: 来源: 题型:
【题目】25°C,改变0.01 mol·L一1 CH3COONa溶液的pH.溶液中c(CH3COOH)、c(CH3COO-)、c(H +)、c(OH- )的对数值lgc与溶液pH的变化关系如图所示,下列叙述正确的是

A.图中任意点均满足c(CH3COOH)+c(CH3COO-)=c(Na+)
B.0.01 mol·L-1CH3COOH的pH约等于线a与线c交点处的横坐标值
C.由图中信息可得点x的纵坐标值为4.74
D.25°C时,![]() 的值随 pH的增大而增大
的值随 pH的增大而增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com