
科目: 来源: 题型:
【题目】乙醛(CH3CHO)是有机合成中的二碳试剂,是合成乙酸、乙醇、乙酸乙酯、农药DDT等的原料。回答下列问题:
(1)Andrea Dasic 等提出在金属催化剂M作用下以N2O为氧化剂可以氧化乙烯生成乙醛。催化体系氧化还原循环如图所示。(物质与氧原子的结合力用OA表示)
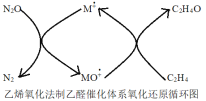
氧原子与N生成NO的结合力OA(N)= 167.4kJ·mol-1,氧原子与乙烯生成乙醛的结合力OA(C2 H4)=473 kJmol-1,则可用作该反应催化剂的金属M与氧原子的结合力OA(M)的值应满足:_______,使用催化剂会使该反应的活化能____(填“增大”或“减小”)。
(2)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJmol-1、890.31 kJ· mol-1、1167.9 kJmol-1,则乙醛的分解反应CH3CHO(l) ![]() CH4(g)+CO(g)的 H =________。
CH4(g)+CO(g)的 H =________。
(3)已知:在含有少量I2的溶液中,反应CH3CHO(aq) ![]() CH4 (g)+CO(g)分两步进行:
CH4 (g)+CO(g)分两步进行:
第I步反应为CH3CHO(aq) +I2(aq)→CH3I(l) + HI(aq) +CO(g)(慢反应),第II步为快反应。
①请写出第II步反应的化学方程式:__________。
②增大I2的浓度______(填“能"或“不能")明显增大总反应的平均速率,理由为_________。
(4)乙醛可以与饱和的NaHSO3溶液发生反应生成水溶性的![]() -羟基磺酸钠:CH3CHO+ NaHSO3
-羟基磺酸钠:CH3CHO+ NaHSO3![]() CH3CH(OH)SO3Na(
CH3CH(OH)SO3Na(![]() -羟基磺酸为易溶于水的强酸)。反应达到平衡后,若其他条件不变,向反应体系中加入足量盐酸,平衡将___ (填“ 正向”“逆向”或“不")移动。
-羟基磺酸为易溶于水的强酸)。反应达到平衡后,若其他条件不变,向反应体系中加入足量盐酸,平衡将___ (填“ 正向”“逆向”或“不")移动。
(5)在100~120 °C、PdCl2 – CuCl2催化剂存在下,乙烯可以与O2反应生成乙醛: 2CH2=CH2(g) +O2(g) ![]() 2CH3CHO(g)。 T°C时,向2 L的恒容密闭容器中通入3 mol CH2=CH2(g)和3 mol O2(g),发生上述反应,反应刚好达到平衡状态后体系压强变为初始压强的5/6,则CH2=CH2(g)的平衡转化率为____ (结果保留3位有效数字),T °C时该反应的平衡常数K为________。
2CH3CHO(g)。 T°C时,向2 L的恒容密闭容器中通入3 mol CH2=CH2(g)和3 mol O2(g),发生上述反应,反应刚好达到平衡状态后体系压强变为初始压强的5/6,则CH2=CH2(g)的平衡转化率为____ (结果保留3位有效数字),T °C时该反应的平衡常数K为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E是原子序数依次递增的五种常见元素。A、B元素组成的气态化合物M的水溶液呈碱性,C元素是地壳中含量最多的元素,D的单质在C的单质中燃烧后的产物可以使品红溶液褪色,E是金属元素。
(1)写出A、C两种元素组成的化合物A2C2的电子式_______。
(2)若将E金属投入盐酸中,生成了浅绿色溶液N。则N的酸性溶液与A2C2反应的离子方程式为______________________________________。
(3)R是B的氧化物,通常情况下呈红棕色。现有一试管R,欲使元素B全部转化为它的最高价氧化物对应的水化物,故进行如下实验操作:将盛有R的试管倒扣在水槽中,______。
(4)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式_____________,放电时,溶液中的H+移向_________(填正极或负极)。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
B. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
C. pH=1的H3PO4溶液中,含有0.1NA个H+
D. 10 g的D2O中含有的质子数与中子数分别为5NA和4NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:氧化锂(Li2O)晶体形成过程中的能量变化如图所示

下列说法正确的是
A. △H1< 0,△H2>0B. -△H5 +△H1 +△H1 +△H3+△H4 +△H6 =0
C. △H3<0,△H4 < 0D. △H1+ △H2+△H3 +△H4 =△H5+△H6
查看答案和解析>>
科目: 来源: 题型:
【题目】着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲。红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如图所示。
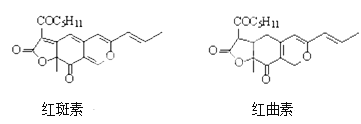
下列说法正确的是
A. 红斑素和红曲素都存在2个手性碳原子
B. 一定条件下红斑素和红曲素都能发生加聚和自身的缩聚反应
C. 红斑素中含有醚键、羰基、酯键这三种含氧官能团
D. 1 mol红曲素最多能与6molH2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.l mol·L-1的CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
A. 加入少量CH3COONH4固体,平衡不移动,c(H+)不变
B. 加入少量NaOH固体,平衡向正向移动,溶液中c(H+)减小
C. 加水,平衡向正向移动,c(CH3COOH)/ c(CH3COO-)增大
D. 通入少量 HCl气体,平衡逆向移动,溶液中c(H+)减少
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋是一个远未完全开发的巨大化学资源宝库。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)
A 氯气 B 淡水 C烧碱 D 食盐
(2)从海水制得的粗盐中含有较多的Mg2+、Ca2+、SO![]() 等,要除去这些离子,下列加入药品顺序正确的是________(填序号)
等,要除去这些离子,下列加入药品顺序正确的是________(填序号)
A NaOH溶液→Na2CO3溶液→BaCl2溶液B BaCl2溶液→NaOH溶液→Na2CO3溶液
C NaOH溶液→BaCl2溶液→Na2CO3溶液D Na2CO3溶液 →NaOH溶液→ BaCl2溶液
(3)从海水中得到溴的过程如下:
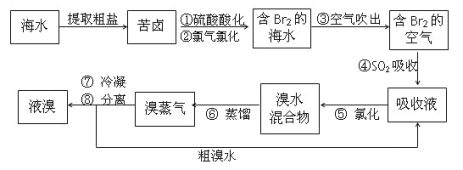
①写出由“苦卤”变成“含溴海水”的离子方程式________
②写出④发生反应的化学方程式________
③某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如图所示实验装置:

图中仪器B冷却水的出口为______(填“甲”或“乙”),D装置的作用是__________,反应的离子方程式为__________,整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
(4)已知某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,现欲使溶液中的Cl-、Br-、I-的物质的量之比为变为4:3:2,那么通入Cl2的物质的量是原溶液中I-的物质的量的__________
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A分子式为C2H4,可发生以下系列转化,已知B、D是生活中常见的两种有机物,下列说法不正确的是( )
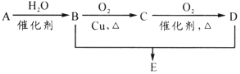
A.75%(体积比)的B溶液常用于医疗消毒
B.D、E都能与NaOH溶液反应
C.由B、D制备E常用浓硫酸作脱水剂
D.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
查看答案和解析>>
科目: 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是
A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
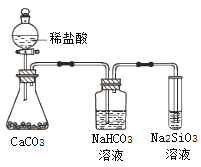
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
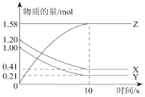
A.反应的化学方程式为: X(g)+Y(g)![]() Z(g)
Z(g)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.温度、体积不变,10s时充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com