
科目: 来源: 题型:
【题目】下表为元素周期表前三周期的一部分:
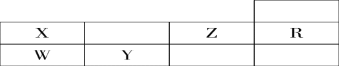
(1)判断 Y ____ Z _____ R _____(写元素符号)。
(2)写出X的氢化物的化学式:_________,W的氢化物的化学式_________,其沸点比较: ________>________ ______________ (填化学式)
(3)下图是X的基态原子的电子排布图,其中有一个是错误的,它不能作为基态原子的电子排布 图是因为它不符合________。
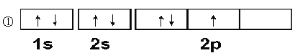
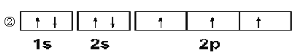
(4)以上五种元素中,________(填元素符号)元素第一电离能最大。_____元素电负性最大,Y的基态原子的电子排布式为________________
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的结构简式为_________。
(2)可以区别甲烷和乙烯的试剂是_________(填正确选项的编号)。
A.浓硫酸 B.碳酸钠溶液 C.溴的四氯化碳溶液 D.酸性高锰酸钾溶液
(3)CH3CH3可以通过乙烯和_________反应生成。
(4)已知 2CH3CHO+ O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下所示:
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下所示:
反应②的化学方程式为______________________。
工业上以乙烯为原料生产聚乙烯的化学方程式为_________,反应类型属于_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】判断下列粒子的空间构型
(1)CO2:_______________________
(2)H2S:____________
(3)SO2:___________
(4)NH4+:_________________
(5)CO32-:_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜是由铜和锌组成的合金,在黄铜中加入镍可显著提高黄铜在大气中和海水中的耐蚀性。回答下列问题:
(1)基态Ni2+的核外电子排布式为____________________,有_______个未成对电子。
(2)CuSO4溶液里逐滴滴入过量氨水,形成深蓝色溶液。
①深蓝色的溶液 是因为生成了一种配离子,其离子符号为____________________
其中配位原子是____________ 。
②NH3分子的空间构型是_______。NH3的键角______(填大于或小于)H2O,原因是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种元素,A的一种同位素可用于考古中测定生物的死亡年代; B与A同周期,其s能级电子数比p能级电子数多;C原子的最外层电子数是次外层的3倍;D与B同主族;E的原子序数为29。回答下列问题:
(1)五种元素中第一电离能最大的是_____,其中D原子价电子排布图为______。
(2)元素B的简单气态氢化物的沸点______元素A的简单气态氢化物的沸点(填大于或小于),其主要原因是____; A的简单气态氢化物中心原子的杂化轨道类型为________。
(3)BC3-的立体构型为__________,与其互为等电子体的分子是__________(写化学式)。
(4)EC在加热条件下容易转化为E2C,从原子结构的角度解释原因____________;E原子的外围电子排布式为_____________。
(5)硼与D可形成一种耐磨材料F,其结构与金刚石相似(如图)。F的晶胞边长为a cm,则该晶体密度的表达式为___________g·cm-3。(用含a、NA的式子表示, 不必化简)。
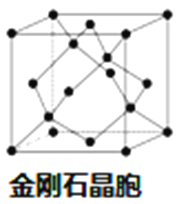
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、D、E、G、J在周期表中的位置如下:
(1)根据上表回答问题:
①D在周期表中的位置是__.
②A、B、E、G的原子半径由大到小的顺序是__(填元素符号).
③B、D的气态氢化物的稳定性关系为__(填化学式).
④34Se与D同主族,其非金属性比D__(填“强”或“弱”),从原子结构的角度解释其原因为__.
⑤E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为ⅰ.H++OH﹣=H2O、ⅱ._________、ⅲ.________.
(2)如图所示转化关系中的各物质由以上六种元素的一种或多种组成,其中甲、乙、丙、丁为两种元素组成的化合物,甲、丙的分子属于10电子微粒,丙为常见溶剂.(图中部分产物已略)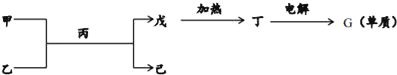
①物质己中含有的化学键的类型为__.
②用电子式表示丙分子的形成过程为__.
③由丁电解制得G单质的化学反应方程式为__.
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。

已知:①![]()
②![]()
③![]()
请回答下列问题:
(1)下列有关F的说法正确的是_________。
A.分子式是![]() B.F即能与HCl又能与
B.F即能与HCl又能与![]() 反应生成盐
反应生成盐
C.能发生取代反应和缩聚反应 D.![]() 的F最多可以和
的F最多可以和![]() 反应
反应
(2)C→D的反应类型是________。
(3)在合成F的过程中,B→C步骤不能省略,理由是______________。
(4)D→E反应所需试剂是____________。
(5)写出同时符合下列条件的A的同分异构体的结构简式(写出其中1个)____。
①苯环上只有两种不同化学环境的氢原子②分子中含有![]()
(6)利用已知信息,以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。_______________注:合成路线的书写格式参照如下示例流程图:
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】2016 年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB 族元素对应离子的萃取,如La3+、Sc2+。写出基态二价 钪离子(Sc2+)的核外电子排布式:____,其中电子占据的轨道数为_____个。

(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为_____,羟基间的相互作用力为_____。
(3)不同大小苯芳烃能识别某些离子,如:N3-、SCN等。一定条件下,SCN与 MnO2反应可得到(SCN)2,试写出(SCN)2的结构式_______。
(4)NH3分子在独立存在时 H-N-H 键角为 106.7°。 [Zn(NH3)6]2+离子中 H-N-H 键角变为 109.5°,其原因是:_________________________。
(5)已知 C60 分子结构和 C60 晶胞示意图(如图Ⅱ、图Ⅲ所示):则一个 C60 分子中含有σ键的个数为______,C60 晶体密度的计算式为____gcm3。(NA 为阿伏伽德罗常数 的值)

查看答案和解析>>
科目: 来源: 题型:
【题目】砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
(1)砷的常见氧化物有 As2O3 和 As2O5,其中 As2O5 热稳定性差。根据图 1 写出 As2O5 分解为 As2O3 的热化学方程式_________________。
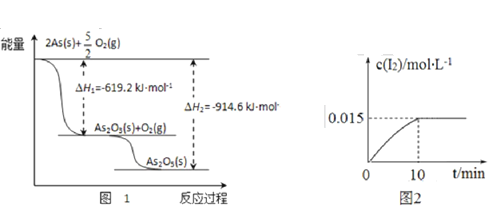
(2)砷酸钠具有氧化性,298 K 时,在 100 mL 烧杯中加入 10 mL 0.1 mol/L Na3AsO4 溶液、20 mL 0.1 mol/L KI 溶液和 20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+ ![]() AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中 c(I2)与时间(t)的关系如图 2 所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中 c(I2)与时间(t)的关系如图 2 所示(溶液体积变化忽略不计)。
①下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.溶液颜色保持不再变化 b.c(AsO33-)+c(AsO43-)不再变化
c.AsO43-的生成速率等于 I2 的生成速率 d.![]() 保持不再变化
保持不再变化
②0~10 min 内,I的反应速率 v(I)=_______。
③在该条件下,上述反应的平衡常数 K=______。
④升高温度,溶液中 AsO43-的平衡转化率减小,则该反应的 ΔH______0(填“大于”“小于”或“等于”)。
(3)雄黄(As4S4)在空气中加热至 300℃时会生成两种氧化物,其中一种氧化物为剧毒的砒霜(As2O3), 另一种氧化物为______(填化学式),可用双氧水将 As2O3 氧化为 H3AsO4 而除去,写出该反应的化学方 程式_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
I.实验室制备FeBr2实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将铁粉加热至600—700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始。不断将d中液溴滴入温度为100—120℃的D中。经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁。
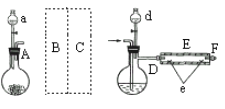
(1)若在A中盛固体CaCO3,a中盛6 mol/L盐酸。为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置和其中的试剂应是:B为_____________。C为________________。为防止污染空气,实验时应在F处连接盛___________的尾气吸收装置。
(2)反应过程中要不断通入CO2,其主要作用是____________________。
Ⅱ.探究FeBr2的还原性
(3)实验需要200 mL 0.1 mol/L FeBr2溶液,配制FeBr2溶液除烧杯、量筒、胶头滴管、玻璃棒外,还需要的玻璃仪器是_____________,需称量FeBr2的质量为:_________。
(4)取10 mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br一被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+
设计实验证明假设2是正确的:________
(5)请用一个离子方程式来证明还原性Fe2+>Br一________:
(6)若在40 mL上述FeBr2溶液中通入3×10-3mol Cl2,则反应的离子方程式为________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com