
科目: 来源: 题型:
【题目】下列有关实验现象和解释或结论都正确的是()
选项 | 实验操作 | 现象 | 解释或结论 |
A | 把SO2通入紫色石蕊试液中 | 紫色先变红后褪色 | SO2具有漂白性 |
B | 向AgCl沉淀中清加KI溶液 | 白色沉淀变为黄色 | 溶度积:AgI比AgCl更小 |
C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变浅 | 反应2NO2 |
D | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是
。有关该物质的下列说法正确的是
A. 该物质能使溴水和酸性髙锰酸钾溶液褪色,褪色原理完全相同
B. 苯乙烯分子的所有原子不可能在同一平面上
C. 该物质苯环上的一溴取代物有3种
D. 除去乙苯中混有的苯乙烯,可以通入等量氢气反应
查看答案和解析>>
科目: 来源: 题型:
【题目】氟化钡可用于制造电机电剧、光学玻璃、光导纤维、激光发生器。以钡矿粉(主要成分为BaCO3, 含有SiO2、Fe2+、Mg2+等杂质)为原料制备氟化钡的流程如下:
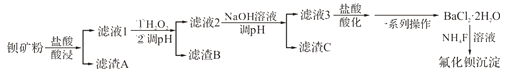
已知:常溫下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4。
(1)滤渣A的化学式为_________________。
(2)滤液1加H2O2氧化的过程中主要反应的离子方程式为__________________。
(3)加20%NaOH溶液调节pH=12.5,得到滤渣C的主要成分是___________。
(4)滤液3加入盐酸酸化后再经__________、冷却结晶、__________、洗涤、真空干燥等一系列操作后得到BaCl2·2H2O。
(5)常温下,用BaCl2·2H2O配制成0.2mol·L-1水溶液与等浓度的氟化铵溶液反应,可得到氯化钡沉淀。 已知Ksp(BaF2)=1.84×l0-7,当钡离子完全沉淀时(即钡离子浓度≤10-5mol·L-1),溶液中氟离子浓度至少是____________mol·L-1。(结果保留三位有效数字,已知![]() =1.36)
=1.36)
(6)已知:Ksp(BaCO3)=2.58×10-9,Ksp(BaSO4)=1.07×10-9。将氯化钡溶液滴入等物质的置浓度的硫酸钠和碳酸钠的混合溶液中,当BaCO3开始沉淀时,溶液中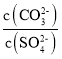 =___________(结果保留三位有效数字)。
=___________(结果保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】依据事实,回答下列问题。
(1)在 25℃、101 kPa 时,1.0 g C8H18(l,辛烷)燃烧生成CO2(g)和H2O(l),放出48.40kJ的热量,则C8H18(l)的燃烧热为_____kJ/mol
(2)已知N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol,N2H4(g)+O2(g)= N2(g)+2H2O (g) ΔH=-534kJ/mol,根据盖斯定律写出肼(N2H4)与 NO2完全反应生成氮气和气态水的热化学方程式____________。
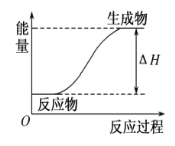
(3)某反应过程中的能量变化如图所示,则该反应是___________反应(填“放热”或“吸热”),判断依据是____________________。
(4)已知:2NH3 (g)+3Cl2(g) =N2 (g) +6HCl(g) ΔH=–462 kJmol-1
N2(g)![]() 2N(g)
2N(g)
Cl2(g)![]() 2Cl(g)
2Cl(g)
则断开1 mol H–N键与断开1 mol H-Cl键所需能量相差约为_____kJ。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.完成以下方程式:⑴写离子方程式,⑵⑶⑷写化学方程式
⑴Na与H2O:________________;
⑵氢氧化亚铁露置在空气中:________________;
⑶制粗Si:________________;
⑷少量CO2通入Na2SiO3溶液:________________。
II.有以下物质:①Fe2O3②Na2CO3③Cl2④浓盐酸⑤浓硫酸⑥SO2⑦高岭石Al2(Si2O5)(OH)4
⑸属于碱性氧化物的是________________(填序号);
⑹工业上用③与石灰乳制取漂白粉,漂白粉的有效成分的化学式是_____________;
⑺写出Cu与⑤反应的化学方程式________________。
⑻请将物质⑦改写成氧化物的形式________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 25.00 | 24.41 |
2 | 25.00 | 24.39 |
3 | 25.00 | 24.60 |
回答下列问题:
(1)如图中甲为___________滴定管,乙为_________ 滴定管(填“酸式”或“碱式 ”)
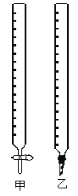
(2)实验中,需要润洗的仪器是:________________________
(3)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是________________________________________
(4)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果____________(填“偏高”“偏低”“不变”,下同);若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果___________。
(5) 未知浓度的NaOH溶液的物质的量浓度为_____________mol/l。
查看答案和解析>>
科目: 来源: 题型:
【题目】某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示,则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )
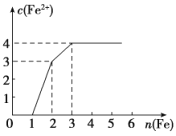
A.1∶1∶1B.1∶3∶1
C.3∶3∶8D.1∶1∶4
查看答案和解析>>
科目: 来源: 题型:
【题目】
研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________,原因是______________________________。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。
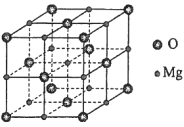
查看答案和解析>>
科目: 来源: 题型:
【题目】向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同溶液M的组成也不同.若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况(不计CO2的溶解),则下列对应图形的判断正确的是
A. 含有两种溶质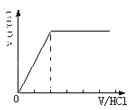 B. 只含有一种溶质
B. 只含有一种溶质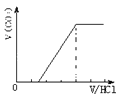 C. 只含有碳酸钠
C. 只含有碳酸钠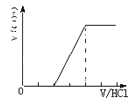 D. 有碳酸钠和碳酸氢钠
D. 有碳酸钠和碳酸氢钠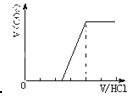
查看答案和解析>>
科目: 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 选项 | a | b | c |
A | Al | AlCl3 | Al(OH)3 | |
B | CO2 | Na2CO3 | NaHCO3 | |
C | Si | SiO2 | H2SiO3 | |
D | S | SO3 | H2SO4 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com