
科目: 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)是印刷行业重要的还原剂,易溶于水,难溶于乙醇;高铁酸钾(K2FeO4)是一种绿色环保型饮用水处理剂。某课题小组拟以硫铁矿(主要成分是FeS2)为主要原料制备连二亚硫酸钠和高铁酸钾,其简易工艺流程如下(部分步骤和条件略去):
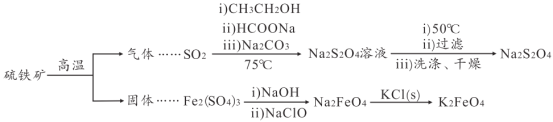
(1)FeS2中含有S22-离子,其电子式为_____。“气体”的主要成分是O2、SO2和N2,参考表中的数据,简述工业上用物理方法分离提纯二氧化硫的实验方案:_____
熔点/℃ | 沸点/℃ | 密度/gL-1(标准状况) | |
O2 | -218 | -183 | 1.429 |
SO2 | -76 | -10 | 2.9 |
N2 | -210 | -196 | 1.25 |
(2)SO2→Na2S2O4步骤中氧化剂与还原剂的物质的量之比为_____。制得的Na2S2O4溶液冷却至50℃,过滤,用_____洗涤,干燥,制得Na2S2O4。
(3)Na2FeO4与KC1发生复分解反应制备K2FeO4,说明相同温度下K2FeO4的溶解度_____(填“ > ”、“ < ”或=”) Na2FeO4的溶解度。
(4)溶液中的Na2S2O4易被空气中的氧气氧化生成NaHSO3,反应的离子方程式为_____
(5)在制备Na2FeO4时,现象是先生成红褐色沉淀,随后转化成绿色溶液,生成了 Na2FeO4。
①写出红褐色沉淀转化为Na2FeO4的化学方程式:_____。
②为探究Na2FeO4和Cl2的氧化性相对强弱,取少量上述绿色溶液于试管中,滴加适量浓盐酸,产生能使湿润的KI淀粉试纸变蓝色的气体,不能说明Na2FeO4的氧化性比Cl2的氧化性强,理由是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 正四面体烷![]() 与立方烷
与立方烷![]() 的二氯代物数目相同
的二氯代物数目相同
B. 淀粉的水解产物为葡萄糖,葡萄糖在酒化酶作用下再进一步水解可得酒精
C. 75%的乙醇溶液可用于医疗消毒,福尔马林可用于浸制动物标本,二者都使蛋白质变 性
D. 甘氨酸和丙氨酸混合物发生缩合只能形成 2 种二肽
查看答案和解析>>
科目: 来源: 题型:
【题目】某菱镁矿主要成分是MgCO3,还含有Al2O3、FeCO3、Fe2O3、SiO2等杂质,由该菱镁矿制备高纯MgO的流程如图。回答下列问题:
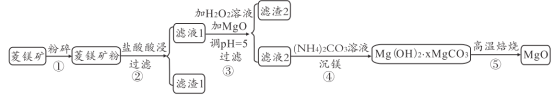
(1)将矿石粉碎的目的是_____,滤渣1的成分是_____
(2)步骤③先加入足量H2O2溶液,再加MgO调节溶液pH=5,加入足量的H2O2溶液后发生的所有氧化还原反应的方程式为_____
(3)滤渣2的成分是_____,1mol该滤渣用3mol/L硫酸溶解,需消耗硫酸_____mL
(4)列举沉镁之后的滤液的一种用途_____,称取14.2g的![]() 在_____(填仪器名称)中进行高温焙烧得到的MgO质量为8.0g,则x=_____。
在_____(填仪器名称)中进行高温焙烧得到的MgO质量为8.0g,则x=_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
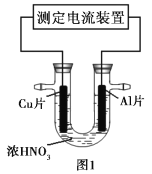
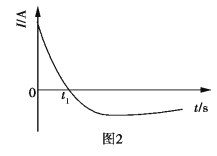
下列说法错误的是( )
A.0~t1时,原电池的负极是Al片
B.0~t1时,正极的电极反应式是![]() +2H++e=NO2↑+H2O
+2H++e=NO2↑+H2O
C.t1后,原电池的正、负极发生互变
D.t1后,正极上每得到0.3mol电子,则负极质量减少2.7g
查看答案和解析>>
科目: 来源: 题型:
【题目】色酮类化合物K具有抗菌、降血脂等生理活性,其合成路线如下:

已知:
(1)A的结构简式是_________;根据系统命名法,F的名称是__________。
(2)B→C所需试剂a是__________;试剂b的结构简式是_________。
(3)C与足量的NaOH反应的化学方程式为__________。
(4)G与新制Cu(OH)2反应的化学方程式为__________。
(5)已知:①2H![]() J+H2O;②J的核磁共振氢谱只有两组峰。以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:________。
J+H2O;②J的核磁共振氢谱只有两组峰。以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:________。

查看答案和解析>>
科目: 来源: 题型:
【题目】短周期中8种元素a-h,其原子半径、最高正化合价或最低负化合价随原子序数递增的变化如图所示。

下列判断不正确的是
A.a、d、f组成的化合物能溶于强碱溶液
B.a可分别与b或c组成含10个电子的分子
C.e的阳离子与g的阴离子具有相同的电子层结构
D.最高价氧化物对应水化物的酸性:h>g>b
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ. 实验室制得气体中常含有杂质,影响其性质检验。
下图A为除杂装置,B为性质检验装置,完成下列表格:
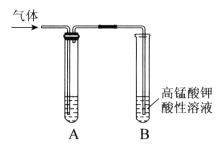
序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | _____________ |
② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是_________________ | ___________ |
③ | 乙炔 | 电石与饱和食盐水反应 | _______________ |
Ⅱ. 为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
编号 | ① | ② | ③ |
实验操作 |
|
|
|
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是________________________;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是______________;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知298K时,Ksp(MnS)=4.65×10-14,Ksp(MnCO3)=2.24×10-11,298K下,MnS、MnCO3(R2-代表S2-或CO32-)在水中的溶解曲线如图所示:
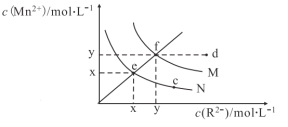
下列说法正确的是( )
A.图象中x约等于5.0×10-6
B.其它条件不变,加热N的悬浊液可使溶液组成由e点沿ef线向f点方向移动
C.常温下,加水稀释M溶液可使溶液组成由d点沿df线向f点方向移动
D.向含有MnS和MnCO3的饱和溶液中加少量MnCl2,c(CO32-)/c(S2-)增大
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醛酸(OHC-COOH )是一种重要的精细化工产品。以高硅铸铁为惰性电极材料,用恒电势电解NaBr 溶液间接氧化乙二醛(OHC-CHO)制备乙醛酸:OHC-CHO+Br2+H2O→OHC-COOH+2HBr。装置如图所示,下列说法不正确的是( )

A.电极b为负极,高硅铸铁不损耗
B.阳极的电极反应式为2Br--2e-=Br2
C.光伏电池将铸铁极的电子转移到石墨极
D.电解过程中,右室溶液的pH逐渐升高
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对两种有机物甲和乙的描述不正确的是( )
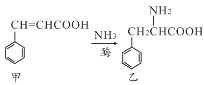
A.甲中所有碳原子不可能在同一平面上
B.甲、乙均能发生加成反应、氧化反应、取代反应
C.甲、乙均能在一定条件下通过聚合反应生成高聚物
D.甲、乙苯环上的一硝基取代物种数相同(不考虑立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com