
科目: 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______,3d能级上的未成对电子数为_______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_______,提供孤电子对的成键原子是________。
(3)单质铜及镍都是由______键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol–1、INi=1 753 kJ·mol–1,ICu> INi的原因是_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用天然气水蒸气重整制备H2的反应为CH4(g)+H2O(g)CO(g)+3H2(g) △H>0,每次只改变一种条件(X),其它条件不变,CH4的平衡转化率![]() 随X的变化趋势如下图所示。下列说法正确的是
随X的变化趋势如下图所示。下列说法正确的是

A.X为温度时,![]() 的变化趋势为曲线N
的变化趋势为曲线N
B.X为压强时,![]() 的变化趋势为曲线M
的变化趋势为曲线M
C.X为投料比![]() 时,
时,![]() 的变化趋势为曲线N
的变化趋势为曲线N
D.某条件下,若CH4(g)、H2O(g)初始浓度均为0.2 mol/L,![]() = 25%,则K=3
= 25%,则K=3
查看答案和解析>>
科目: 来源: 题型:
【题目】请用C、H、O、N、S五种元素回答下列问题
(1)除H外,其它四种元素中,第一电离能最大的元素基态原子电子排布图为______________,电负性最大的元素基态原子核外电子运动状态共有_________种。
(2)五种元素中,由其中两种元素构成甲、乙、丙、丁四种分子,所含原子的数目依次为3、4、6、8,都含有18个电子。甲和乙的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
甲 | 187 | 202 | 2.6 |
乙 | 272 | 423 | 以任意比互溶 |
①1mol乙分子含有_________个σ键;
②丁分子的中心原子采取_________杂化方式;甲分子的VSEPR模型为_________,丙分子为_________(“极性”或“非极性”)分子。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学用语对事实的表述正确的是
A..由H和Cl形成HCl的过程:![]()
B.常温时,饱和NaClO溶液的pH约为11:ClO-+H2O=HClO+OH-
C.苯酚和甲醛在一定条件下反应能生成酚醛树脂: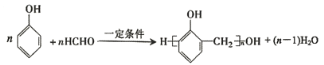
D.电解饱和食盐水的反应:2Cl-+2H+![]() Cl2↑+H2↑
Cl2↑+H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应均伴随着能量的变化,某化学反应过程能量变化如图所示,该化学反应可能是
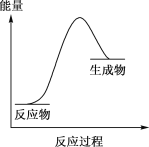
A.NaOH+HCl=NaCl+H2O
B.Fe+H2SO4=FeSO4+H2↑
C.2Na2O2+2H2O=4NaOH+O2↑
D.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为________;Z的核外电子排布式是________;
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式________;
(3)D和Y形成的化合物,其分子的空间构型为________;D原子的轨道杂化方式是________;
(4)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关晶体的叙述中,正确的是( )
A. 氯化钠和氯化铯晶体中,阳离子的配位数均为6
B. 金刚石为三维网状结构,由碳原子以sp3杂化轨道形成共价键
C. 金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8
D. 干冰晶体中,每个CO2分子周围紧邻8个CO2分子
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2O2分子的空间结构可在二面角中表示,如图所示,下列有关H2O2结构的说法正确的是( )
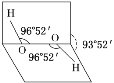
A. H2O2中有3个σ键、1个π键
B. H2O2为非极性分子
C. H2O2中氧原子为sp3杂化
D. H2O2沸点高达158 ℃,可推测H2O2分子间可形成氢键
查看答案和解析>>
科目: 来源: 题型:
【题目】液氨是富氢物质,是氢能的理想载体。下列说法不正确的是( )
A. NH3分子中氮原子的杂化方式为sp3杂化
B. [Cu(NH3)4]2+中,NH3分子是配体
C. 相同压强下,NH3的沸点比PH3的沸点低
D. NH4+与PH4+、CH4、BH4-互为等电子体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com