
科目: 来源: 题型:
【题目】下表是元素周期表的前四周期,请回答有关问题:(相关问题均用具体化学用语回答)
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ | ||||||
(1)④的原子结构示意图为_________;②在元素周期表位置________;上述元素中最高价氧化物的水化物酸性最强的是_________;(填水化物化学式)
(2)⑤的最高价氧化物的水化物和⑥的最高价氧化物反应的离子方程式________________
(3)用电子式表示元素①和⑧形成的化合物的形成过程________________
(4)⑤的最高价氧化物水化物的电子式________________
(5)请设计实验证明⑧与⑩的氧化性强弱________________
查看答案和解析>>
科目: 来源: 题型:
【题目】侯氏制碱原理:NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl,需经过制取氨气、制取NaHCO3、分离及干燥NaHCO3四个步骤,下列图示装置能达到实验目的的是
A. 制取氨气 B. 制取NaHCO3
B. 制取NaHCO3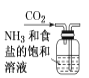
C. 分离NaHCO3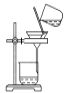 D. 干燥NaHCO3
D. 干燥NaHCO3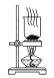
查看答案和解析>>
科目: 来源: 题型:
【题目】I磷酸氯喹是治疗新型肺炎的潜力药。磷酸是合成该药的初级原料之一,沸点高,难挥发。化学兴趣小组设计了合成磷酸的流程如图。
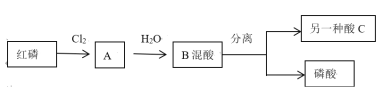
回答下列问题
(1)将一定了的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如图
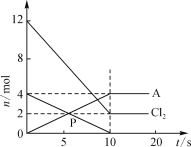
①前10s消耗的氯气为________mol,该反应的化学方程式为_________(A用化学式表示)
②前10s的平均反应速率v(Cl2)=________
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是________(写名称)
②A与热水反应的化学方程式为________
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)________

(2)该装置中负极的电极方程式为________。
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子_____________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 节日里燃放的五彩缤纷的烟花是某些金属元素化学性质的展现
B. 将等物质的量的氧化钠和过氧化钠分别投入到足量且等质量的水中,得到溶质质量分数分别是 a%和 b%的两种溶液,则a 和 b 的关系是 a=b
C. 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来, 说明金属铝的熔点较低
D. 用如图装置进行实验,将装置①中的 AlCl3 溶液滴入装置②浓氢氧化钠溶液,溶液中可观察到有大量白色沉淀产生

查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气中含有CO、NO等有害气体。
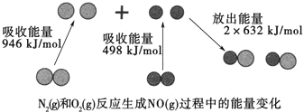
(1)汽车尾气中NO生成过程的能量变化如图示。1molN2和1molO2完全反应生成NO会________(填“吸收”或“放出”)________kJ能量。
(2)一种新型催化剂用于NO和CO的反应:2NO+2CO![]() 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在表中。
实验编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.2×10-3 | b | 124 |
Ⅲ | 350 | a | 5.80×10-3 | 82 |
①请将表中数据补充完整:a___________。
②能验证温度对化学反应速率规律的是实验____________________(填实验序号)。
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线________________(填“甲”或“乙”)。

④在容积固定的容器中发生反应2NO+2CO![]() 2CO2+N2,不能说明已达到平衡状态的是________(不定项选择);
2CO2+N2,不能说明已达到平衡状态的是________(不定项选择);
A.容器内CO浓度不变 B.容器内NO的浓度等于CO2的浓度
C.v逆(NO)=2v正(N2) D.容器内混合气体密度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】以下8种化合物中,不能通过化合反应直接生成的有
①Fe3O4 ②Fe(OH)3 ③FeCl2 ④Cu2(OH)2CO3 ⑤Al(OH)3 ⑥Na2CO3 ⑦NaHCO3 ⑧Na2O2
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq)CH3CO3H(aq)+H2O(l) △H=-13.7KJ/mol
(1)市售过氧乙酸的浓度一般不超过21%,原因是____ 。
(2)利用上述反应制备760 9 CH3CO3H,放出的热量为____kJ。
(3)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25 ℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数,数据如图2所示。
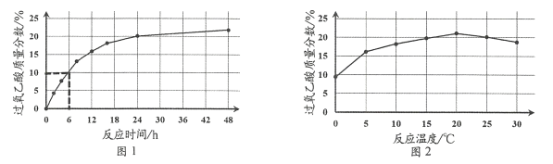
①实验1中,若反应混合液的总质量为mg,依据图1数据计算,在0—6h间,v(CH3CO3H)=____ g/h(用含m的代数式表示)。
②综合图1、图2分析,与20 ℃相比,25 ℃时过氧乙酸产率降低的可能原因是_________。(写出2条)。
(4) SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40 nm和70 nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
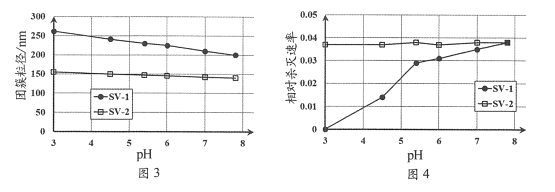
依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是______
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇做为可再生能源比化石能源具有较大的优势,如图为乙醇燃料电池,该电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O。下列关于该电池叙述错误的是
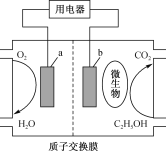
A.a极与用电器的正极相接B.该装置将化学能转化为电能
C.质子(H+)由装置左侧向右侧移动D.该装置的电解质溶液呈酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】某反应体系前30min各物质的物质的量的浓度变化如图所示。下列说法正确的是

A.该反应的化学方程式为X![]() Y
Y
B.M点的正反应速率小于逆反应速率
C.Q点正、逆反应速率相等,反应停止。
D.前20min反应速率v(X)=0.1mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】镍镉电池是应用广泛的二次电池,其总反应为:
Cd+2NiOOH+2H2O![]() 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2
制造密封式镍镉电池的部分工艺如下:
I.Ni(OH)2的制备
以硫酸镍(NiSO4)为原料制备Ni(OH)2的主要过程如下图所示。制备过程中,降低Ni(OH)2沉淀速率,可以避免沉淀团聚,提升电池性能。

已知:Ni2++6NH3H2O[Ni(NH3)6]2++6H2O
(1)操作a是 ____。
(2)制备过程中,需先加氨水,再加过量NaOH,请
①先加氨水的目的是 ___。
②用化学平衡移动原理分析加入NaOH需过量的原因是____。
(3)用无水乙醇代替水洗涤滤渣的优点是_____答出1条即可)。
II.镍镉电池的组装
主要步骤:①将Ni(OH)2和Cd(OH)2固定,中间以隔膜隔开(如下图所示);②将多组上述结构串联;③向电池中注入KOH溶液;④密封。

(4)下列对镍镉电池组装和使用的分析正确的是____(填字母序号)。
a.密封镍镉电池可以避免KOH变质
b.镍电极为电池的负极,镉电极为电池的正极
c.电池组装后,应先充电,再使用
III.过度充电的保护
电池充电时,若Cd(OH)2和Ni(OH)2耗尽后继续充电,会造成安全隐患,称为过度充电。制造电池时,在镉电极加入过量的Cd(OH)2可对电池进行过度充电保护,该方法称为镉氧循环法。
(5) Cd(OH)2耗尽后继续充电,镉电极上生成的物质为____。
(6)已知:①隔膜可以透过阴离子和分子:②O2可以与Cd发生反应生成Cd(OH)2。请结合两个电极上的电极反应式说明用镉氧循环法实现过度充电保护的原理:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com