
科目: 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
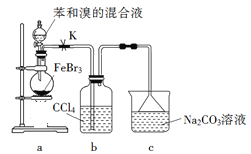
A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B. 实验中装置b中的液体逐渐变为浅红色
C. 装置c中的碳酸钠溶液的作用是吸收溴化氢
D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是一种重要的化工产品,目前硫酸的主要生产方法是“接触法”,其主要反应之一为2SO2+O2![]() 2SO3。下列有关该反应的说法不正确的是( )
2SO3。下列有关该反应的说法不正确的是( )
A.SO2和O2不可能全部转化为SO3
B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C.该反应从开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.工业上生产SO3时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
科目: 来源: 题型:
【题目】富马酸亚铁,是一种治疗缺铁性贫血的安全有效的铁制剂。富马酸在适当的pH条件下与FeSO4反应得富马酸亚铁。
已知:
物质名称 | 化学式 | 相对分子质量 | 电离常数(25℃) |
富马酸 | C4H4O4 | 116 | K1=9.5×10-4,K2=4.2×10-5 |
碳酸 | H2CO3 | K1=4.4×10-7,K2=4.7×10-11 | |
富马酸亚铁 | FeC4H2O4 | 170 |
i.制备富马酸亚铁:
①将富马酸置于100 mL烧杯A中,加热水搅拌
②加入Na2CO3溶液10 mL使溶液pH为6.5~6.7。并将上述溶液移至100 mL容器B中
③安装好回流装置C,加热至沸。然后通过恒压滴液漏斗D缓慢加入FeSO4溶液30 mL
④维持反应温度100℃,充分搅拌1.5小时。冷却,减压过滤,用水洗涤沉淀
⑤最后水浴干燥,得棕红(或棕)色粉末,记录产量。
请回答以下问题:
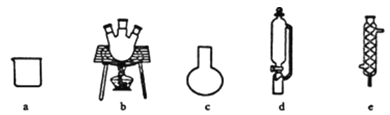
(1)该实验涉及到的主要仪器需从以下各项选择,则B为_________(填字母),C为___________(填名称);
(2)己知反应容器中反应物FeSO4和富马酸按恰好完全反应的比例进行起始投料,写出步骤②中加入Na2CO3溶液调节pH的目的是_____________,若加入Na2CO3溶液过量,对实验的影响是_____________;
(3)所需FeSO4溶液应现用现配,用FeSO4·7H2O固体配置FeSO4溶液的方法为:__________;
(4)写出容器B中制备富马酸亚铁的化学方程式:___________;
(5)步骤④检验沉淀是否洗净的方法是:________________;
ii. 计算产品的产率:
(6)经测定,产品中富马酸亚铁的纯度为76.5%、以5.80 g富马酸为原料反应制得产品8.50 g,则富马酸亚铁的产率为______________%(保留小数点后一位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中可以说明2HI(g)![]() H2(g)+I2(g)已达到平衡状态的是( )
H2(g)+I2(g)已达到平衡状态的是( )
(1)单位时间内生成n mol H2的同时生成n mol HI
(2)一个H—H键断裂的同时有两个H—I键断裂
(3)c(HI)= c(I2)
(4)反应速率υ(H2)=υ(I2)=0.5υ(HI)
(5)c(H2)∶c(I2)∶c(HI)=2∶1∶1
(6)温度和体积一定时,某一生成物浓度不再变化
(7)温度和体积一定时,容器内压强不再变化
(8)条件一定,混合气体的平均相对分子质量不再变化
(9)温度和体积一定时,混合气体的颜色不再发生变化
(10)温度和压强一定时,混合气体的密度不再发生变化
A. (1)(2)(5)(9)(10) B. (2)(6)(9) C. (6)(7)(10) D. 全部
查看答案和解析>>
科目: 来源: 题型:
【题目】环境保护是目前人类面临的一项重大课题。为应对燃料使用造成的环境污染,科学家提出了利用太阳能促进燃料循环使用的构想,其构想可用下图表示:
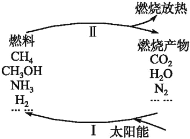
其中过程Ⅰ的主要反应为①2CO2![]() 2CO+O2,②2H2O
2CO+O2,②2H2O![]() 2H2↑+O2↑,③2N2+6H2O
2H2↑+O2↑,③2N2+6H2O![]() 4NH3+3O2,④2CO2+4H2O
4NH3+3O2,④2CO2+4H2O![]() 2CH3OH+3O2,⑤CO2+2H2O
2CH3OH+3O2,⑤CO2+2H2O![]() CH4+2O2。
CH4+2O2。
下列说法中不正确的是
A.过程Ⅱ中发生的反应均为放热反应
B.太阳能最终主要转化为热能
C.经过上述一个循环后放出O2
D.要实现上述循环,当前需要解决的关键问题是过程Ⅰ
查看答案和解析>>
科目: 来源: 题型:
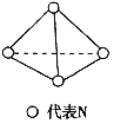
【题目】科学家已获得了气态![]() 分子,其结构为正四面体(如图所示)。已知断裂1mol N-N键吸收167kJ能量,断裂1mol
分子,其结构为正四面体(如图所示)。已知断裂1mol N-N键吸收167kJ能量,断裂1mol ![]() 键吸收942kJ能量,下列说法正确的是( )
键吸收942kJ能量,下列说法正确的是( )
A.![]() 属于一种新型的化合物
属于一种新型的化合物
B.1mol ![]() (g)完全转化为N(g)的过程中释放1002kJ能量
(g)完全转化为N(g)的过程中释放1002kJ能量
C.1mol ![]() (g)完全转化为
(g)完全转化为![]() (g)时放出882kJ能量
(g)时放出882kJ能量
D.![]() 和
和![]() 互为同素异形体,
互为同素异形体,![]() 转化为
转化为![]() 属于物理变化
属于物理变化
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D是4种常见的短周期元素,其原子半径随原子序数的变化如图所示。已知A的一种核素可表示为![]() ,该核素中有10个中子,简单离子B+与Ne原子的核外电子排布相同,C的单质是一种常见的半导体材料,D的最高价氧化物对应水化物的分子式为HDO4。下列说法不正确的是( )
,该核素中有10个中子,简单离子B+与Ne原子的核外电子排布相同,C的单质是一种常见的半导体材料,D的最高价氧化物对应水化物的分子式为HDO4。下列说法不正确的是( )
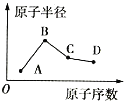
A.B的简单离子半径小于D的简单离子半径
B.气态氢化物的稳定性:C<D
C.A、B、D元素组成的某种化合物能用于杀菌消毒
D.C的氧化物与B和D的最高价氧化物对应的水化物均能反应
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.1mol/L CH3COOH溶液加入水稀释或加入少量CH3COONa晶体时,都会引起
A. 溶液中pH增大B. CH3COOH的电离程度变大
C. 溶液的导电能力减弱D. CH3COO-的浓度变小
查看答案和解析>>
科目: 来源: 题型:
【题目】铟(In)主要应用于透明导电图层、荧光材料、有机合成等,以ITO靶材废料(主要由In2O3、SnO2组成)为原料回收铟的工艺流程如图:

已知:i. 锡、锌的性质均与铝的性质相似.
ii. 铟不与强碱反应,氢氧化铟难与强碱性溶液反应,在较浓的氢氧化钠溶液中也只有少量溶解。
iii. Ksp[In(OH)3]=1×10-33 Ksp[Sn(OH)4]=1×10-56
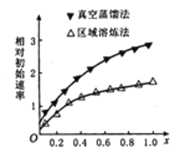
(1)海绵状ITO[xIn2O3(1-x)SnO2]可作异佛尔酮二胺合成的催化剂,如图表示相同条件下,两种不同方法制得的催化剂催化异佛尔酮二胺的相对初始速率随x的变化曲线。真空蒸馏法的相对初始速率较大的原因可能是_________,In2O3、SnO2两种氧化物中,催化效果更好的是__________;
(2)酸浸时,铟的浸出率随温度和硫酸浓度的关系如表,锡的浸出率小于20%。
30℃ | 50℃ | 70℃ | 90℃ | |
3 mol/L H2SO4 | 56% | 72% | 83% | 91% |
4 mol/L H2SO4 | 68% | 81% | 89% | 94% |
①写出“浸出”反应的化学方程式:___________________________;
②由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而_____________(填“增大”“减小”或“不变”下同),温度越高,硫酸浓度对铟的浸出率影响__________;
(3)现有一份In2(SO4)3和Sn2(SO4)2的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量关系如图所示:
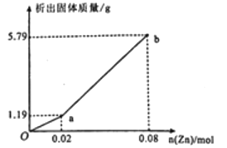
该混合溶液中,In3+和Sn4+的物质的量浓度之比为_______________;
(4)若“浸酸”后的溶液中In2(SO4)3的浓度为1 mol/L,取100 mL该溶液向其中滴加氨水,当Sn4+沉淀完全[设c(Sn4+)=1×10-6 mol/L]时,溶液的pH=____________,此时In3+是否开始形成沉淀_____(填“是”或“否”);
(5)“碱熔”时主要反应的离子方程式为___________;
(6)以粗铟为阳极,纯铟为阴极,H2SO4、NaCl和InCl3混合液为电解液可提纯粗铟。写出阴极反应的电极方程式:___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】海藻中含有丰富的碘元素,如图是实验室从海藻中提取捵的部分流程:
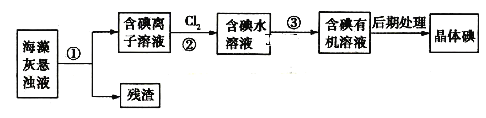
下列判断不正确的是
A.步骤①、③的操作分别是过滤、萃取分液
B.步骤②中反应的离子方程式为:![]()
C.可用淀粉溶液检验步骤②中的反应是否进行完全
D.步骤③中加入的有机溶剂可以是![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com