
科目: 来源: 题型:
【题目】某科研小组采用如下方案拆解废钴酸锂电池并从拆解的正极片中回收锂和钴,主要的实验流程如下:

已知:①正极片中主要含LiCoO2(难溶于水)以及少量乙炔炭黑及铝箔等;负极为石墨,充电时Li+嵌入石墨电极。
②P2O4为磷酸二异辛酯,密度为0.973g.cm-3。
③3HBrO+CO(NH2)2=3HBr+N2↑+2H2O+CO2↑。
(1)“放电处理”时,有关说法正确的是__________(填标号)。
A.有利于锂的回收,提高锂的回收率
B.处理的主要目的是回收残余的电能
C.处理过程中产生的气体只有O2
D.可防止在电池拆解过程中,发生短路引起火灾、爆炸事故等安全问题
(2)“还原浸取”时,发生反应的离子方程式为_____________(S2O32-被氧化为SO42-)。
(3)“除铁、铝”时,应调整溶液的pH范围为___________(下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。

(4)“萃取”与“反萃取”时,静置后(如图所示),获得有机相的操作方法是__________;“反萃取”试剂X适宜是___________(填“H2SO4”或“NaOH”)溶液。

(5)设计以流程中产品Li2CO3为原料,制取LiBr·H2O的实验方案:向烧杯中加入适量冷水,______________,干燥得LiBr·H2O[实验中必须使用的试剂:饱和溴水、尿素及活性炭]。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁铁水滑石(镁、铁的碱式碳酸盐)是具有层状结构的无机功能材料,可由Mg(NO3)2·6H2O、Fe(NO3)3·9H2O及CO(NH2)2等按一定比例在温度高于90℃时反应制得。
(1)其他条件不变时,n[CO(NH2)2]/n(Fe3+)对镁铁水滑石产率和溶液pH的变化关系如图所示:

① <3,反应液中产生少量气体,测氨仪未检出NH3,说明逸出的气体主要是____________(填化学式)。
<3,反应液中产生少量气体,测氨仪未检出NH3,说明逸出的气体主要是____________(填化学式)。
②n[CO(NH2)2]/n(Fe3+)>12,溶液的pH处于稳定状态,这是因为_________________
(2)镁铁水滑石表示为:[FexMgy(OH)z](CO3)w·pH2O(摩尔质量为660g·mol-1),可通过下列实验和文献数据确定其化学式,步骤如下:
I.取镁铁水滑石3.300g加入足量稀硫酸充分反应,收集到气体112mL(标准状况)。
II.文献查得镁铁水滑石热分解TG-DSC图:303~473K,失去层间水(结晶水)失重为10.9%;473~773K时,CO32-和OH-分解为CO2和H2O;773K以上产物为MgO、Fe2O3。
Ⅲ.称取0.4000g热分解残渣(773K以上)置于碘量瓶中,加入稍过量盐酸使其完全溶解,加入适量水和稍过量的KI溶液,在暗处放置片刻,用0.1000mol·L-1Na2S2O3标准溶液滴定到溶液呈淡黄色,加入3mL淀粉溶液,继续滴定到溶液蓝色消失。(2Na2S2O3+I2=2NaI+Na2S4O6),消耗Na2S2O3溶液20.00mL。通过计算确定镁铁水滑石的化学式______________(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物H是制备某褪黑素受体激动剂的中间体,其合成路线如下:

已知:RCOOH![]()
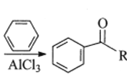 ,其中—R为烃基。
,其中—R为烃基。
(1)A中含氧官能团的名称为__________和__________。
(2)B→C的反应类型为___________。
(3)F的分子式为C11H8O2Br2,写出F的结构简式:________
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_____。
①能与FeCl3溶液发生显色反应;
②碱性条件水解生成两种产物,酸化后两种分子中均只有2种不同化学环境的氢。
(5)写出以![]() 和
和![]() 为原料制备
为原料制备 的合成路线流程图______________(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图______________(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是 ( )
A. 标准状况下,22.4LH2O含有的分子数为1 NA
B. 常温常压下,16g O2含有的原子数为1 NA
C. 通常状况下,1NA 个SO2分子占有的体积约为22.4L
D. 物质的量浓度为0.5mol/L的K2SO4溶液中,含有SO42-个数为0.5 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】用磷铁渣(含Fe、FeP、Fe2P及少量杂质)制备FePO4·2H2O(磷酸铁)的工艺流程如下:

(1)“浸取”时,在密闭反应器中加入硝酸、硫酸及活性炭,硝酸首先分解生成NO2和O2,O2将铁和磷分别氧化为Fe2O3、P2O5。
①Fe2P与O2反应的化学方程式为__________。
②加入硫酸的目的是__________;加入活性炭能降低有害气体的产生,这是因为__________。
③c(HNO3)与磷铁渣溶解率关系,如题图-1所示,当c(HNO3)在1.5~2.0mol·L-1时,磷铁渣溶解率随硝酸的浓度增大而减小的原因是__________
 图-1
图-1
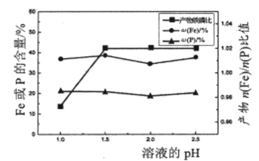 图-2
图-2
(2)“制备”时,溶液的pH对磷酸铁产品中铁和磷的含量及n(Fe)/n(P)比值的影响,如题图-2所示(考虑到微量金属杂质,在pH=1时,n(Fe)/n(P)为0.973最接近理论值])。在pH范围为1~1.5时,随pH增大,n(Fe)/n(P)明显增大,其原因是___________;写出生成FePO4·2H2O的离子方程式:__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应能用离子方程式CO![]() +2H+=CO2↑+H2O表示的是
+2H+=CO2↑+H2O表示的是
①Na2CO3+2HCl=2NaCl+CO2↑+H2O ②K2CO3+H2SO4=K2SO4+CO2↑+H2O
③CaCO3+2HCl=CaCl2+CO2↑+H2O ④2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O
A.①②B.①②③C.①③④D.②④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的离子方程式不正确的是
A.铁与稀盐酸反应:Fe +2H+ =2Fe2+ + H2↑
B.氢氧化钠溶液与盐酸反应:OH- + H+ = H2O
C.钠与硫酸铜溶液反应:2Na + Cu2+ = 2Na+ + Cu
D.氯化钡溶液与稀硫酸反应:Ba2+ + SO![]() = BaSO4↓
= BaSO4↓
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为2.0L的恒容密闭容器中充入3.0molCl2和4.0molPCl5,473K 时发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1,各物质的物质的量随时间变化关系如图所示:
PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1,各物质的物质的量随时间变化关系如图所示:
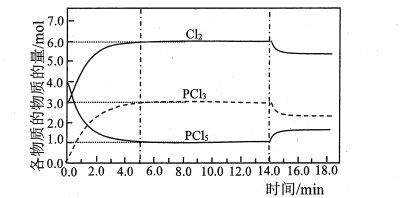
下列说法正确的是
A.0.0~5.0min,PCl5分解的平均速率为0.6mol·L-1·min -1
B.起始时,若用3.0mol37Cl2和4.0mol P35Cl5,达平衡时,PCl3 中不含37C1
C.图中14.0min时,改变的外界条件可能是缩小容器的体积
D.若在14.0min时,向容器中各充入1.0mol 的Cl2、PCl5 及PCl3,维持其他条件不变,重新达到平衡前,v(正)>v(逆)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示部分反应条件、产物省略:
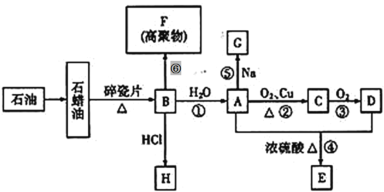
回答下列问题:
(1)工业上由石蜡油获得B的方法称为___________。
(2)①决定化合物A的化学特性的原子团的名称为___________。
②B到A的反应类型为___________,A到E的反应类型为___________。
(3)写出下列反应的化学方程式。
反应②:___________
反应⑥:___________
查看答案和解析>>
科目: 来源: 题型:
【题目】某种钢闸门保护法原理示意图如下,下列说法不正确的是
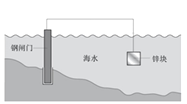
A. 锌块发生氧化反应:Zn-2e–= Zn2+
B. 钢闸门有电子流入,可以有效减缓腐蚀
C. 若通过外加电源保护钢闸门,应将钢闸门与电源正极相连
D. 锅炉内壁装上若干镁合金的防腐原理与该种钢闸门保护法原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com