
科目: 来源: 题型:
【题目】有一固体混合物,可能由K2CO3、NaNO2、FeCl3、KClO3、AgNO3混合而成,为检验它的成分,做了如下实验:取固体加入足量的稀硝酸中,搅拌充分反应,得到无色透明溶液,同时有黄绿色气体和白色沉淀生成![]() 已知NaNO2不能被稀硝酸氧化)。根据以上实验现象,你认为以下判断正确的是
已知NaNO2不能被稀硝酸氧化)。根据以上实验现象,你认为以下判断正确的是
A.一定含有KClO3、AgNO3、NaNO2,不能肯定是否含有氯化铁
B.一定含有KClO3,且在反应过程中被还原生成了两种还原产物
C.另取适量固体加水溶解,若出现白色沉淀,即可证明K2CO3的存在
D.将反应产生的气体通入少量澄清石灰水,若有无沉淀出现,即可证明K2CO3不存在
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某溶液中含有SO42-、CO32-、Cl-,若只允许取一次该溶液而把三种离子分别检验出来,则应采取的措施是:
①先加入_____________检验_____________________;
②然后加入_________________,检验_____________;
③最后加入______________检验____________________________。
(2)阅读、分析下列两个材料:
材料一、(见图)

材料二、
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm3 | 溶解性 |
乙二醇( C2H6O2) | 11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题(填写序号):
A.蒸馏法 B.萃取法
C.“溶解、结晶、过滤”的方法 D.分液法
①纯碱从氯化钠和纯碱的混合物中分离出来,最好应用______。
②将乙二醇和丙三醇相互分离的最佳方法是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.2 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题
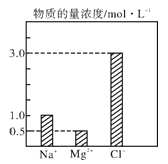
(1)该混合液中,NaCl的物质的量为_________mol,含溶质MgCl2的质量为_______g。
(2)该混合液中CaCl2的物质的量为___________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为__________mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组用数字实验系统测定一定浓度碳酸钠溶液的pH与温度的关系,得到如图所示曲线。下列分析不正确的是

A.b点溶液中OH-浓度在整个过程中最大
B.水的电离平衡也会对溶液的pH产生影响
C.a→b段水解平衡向右移动
D.a点溶液显碱性,且离子浓度从大到小为:Na+>CO32->OH->HCO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子个数之比为__;氧原子个数之比为___。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92g该氧化物的体积为448mL,则该氧化物的摩尔质量为___,R的相对原子质量为__。
(3)常温下,在27.5g水中溶解12.5gCuSO4·5H2O,恰好达到饱和,该溶液的密度为1.21g/cm3,则该溶液中CuSO4的物质的量浓度约为__,从中取出20.0mL该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积是__mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外兴趣小组需要用18mol/L 的浓硫酸配制80mL3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④检漏、转移、洗涤 ⑤定容、摇匀。回答下列问题:
(1)所需浓硫酸的体积是___mL,量取浓硫酸所用的量筒的规格是___(用下列编号填空)。
A.10 mL B.25mL C.50mL D.100mL
(2)第⑤步实验的操作是继续向容量瓶中注入蒸馏水至离刻度线1-2cm处,改用___向容量瓶中滴加蒸馏水至凹液面和刻度线相切为止。塞紧瓶塞,倒转摇匀并装试剂瓶。
(3)下列情况对所配制的稀硫酸浓度有何影响?(填“偏大”“偏小”或“无影响”)
①容量瓶用蒸馏水洗涤后残留有少量的水___;
②在转入容量瓶前烧杯中溶液未冷却至室温___;
③取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯___。
查看答案和解析>>
科目: 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是
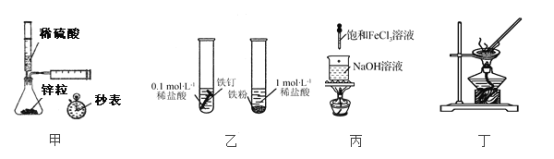
A. 用甲装置测定一定时间内产生氢气的体积,可测定该反应的速率
B. 用乙所示方法探究固体表面积对反应速率的影响
C. 用丙装置制备Fe(OH)3胶体
D. 用丁装置蒸发结晶制AlCl3晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图所示。

(1)指出提取碘的过程中有关的实验操作名称___、___。
(2)写出流程图中氧化②的离子反应议程式___。
(3)提取碘的过程中,可供选择的有机试剂是___。
A.酒精 B.四氯化碳 C.醋酸 D.水
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器,尚缺少的玻璃仪器是___。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出图中实验装置中的错误之处。

①____;
②____;
③____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为一“铁链”图案,图案上由左到右分别写了H2O、CO2、Na2O、NaCl、FeCl35种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号。请回答下列问题:

(1)请将分类依据代号填入相应的括号内:
(____)两种物质都是非金属氧化物
(____)两种物质都是钠的化合物
(____)两种物质中一种是酸性氧化物,一种是碱性氧化物
(____)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入图中某种物质M的水溶液,继续煮沸可制得一种红褐色胶体。
①物质M的化学式为________。
②证明有红褐色胶体生成的最常用的实验操作是______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家使用双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH<0,在低温下获得较高反应速率,反应过程如图:
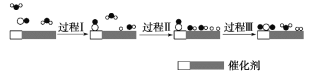
下列说法正确的是
A.若已知CO和H2的标准燃烧热,由此可推算出该反应的ΔH
B.过程Ⅰ、过程Ⅱ均为吸热过程,且吸收的热量相等
C.在该反应过程中,实际有两个H2O参与反应,断裂了三个氢氧键
D.使用催化剂降低了水煤气变换反应的ΔH,提高了反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com