
科目: 来源: 题型:
【题目】化学计量是化学学习中的重要工具,请根据物质的量有关知识填空(NA表示阿伏伽德罗常数)
(1) _____molCO2中含有氧原子数跟1.806×1024个H2O分子含有的氧原子数相同。
(2)标准状况下,体积为11.2L的N2的质量是_____g,所含质子数目为___。
(3)0.2L0.5mol/LAl2(SO4)3溶液和0.5L 0.5mol/L Na2SO4溶液,所含SO42—离子的物质的量浓度之比为____。
(4)标准状况下,NH3和CH4组成的混合气体的密度为0.75g/L,则NH3的体积分数为___。
(5)标准状况下,将VLA气体(摩尔质量为M g/ mol )溶于0.1L水中,所得溶液的密度为ρg/cm3,则此溶液的物质的量浓度为____mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.已知某可逆反应:aA(g)+bB(g) ![]() cC(g)+dD(g)。请回答下列问题:
cC(g)+dD(g)。请回答下列问题:

(1)根据实验测定结果,描绘出了该反应达到平衡状态时及改变外界条件后,反应速率与时间的关系图像(如图1所示),有利于提高D产量的变化过程是图像中的______段;引起该变化过程的外界条件是_________________________________________。
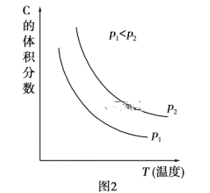
(2)根据实验测定结果描绘出了图2。由此图像可以得出,升高温度,上述平衡将向____(填“正反应”或“逆反应”)方向移动;反应计量数之间的关系:a+b______c+d(填“大于”、“小于”、“等于”或“不确定”)。
Ⅱ.工业合成氨反应如下:N2+3H2![]() 2NH3。请回答下列问题:
2NH3。请回答下列问题:
(1)在一定条件下2L的密闭容器中进行实验,并测得下列数据:
物质 | N2 | H2 | NH3 |
起始(mol) | 2 | 7 | 0 |
10s(mol) | 1.6 | ||
平衡时(mol) | 2 |
则10s内,用氢气表示的化学反应速率是______,该反应的化学平衡常数是________。
(2)根据混合气体各成分的物质性质,你认为工业上将氨气从混合气体中分离出来的措施是________,从而达到反应气体循环利用的目的。实验室检验氨气的方法是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g)△H=-49.0kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
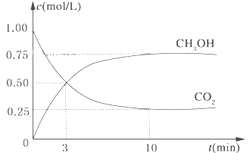
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=______mol/(Lmin);
(2)氢气的转化率=______;
(3)该反应的平衡常数为______(保留小数点后2位);
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是______。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去 D.再充入1mol H2
(5)当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2,则c1______c2的关系(填“>”、“<”或“=”)
查看答案和解析>>
科目: 来源: 题型:
【题目】2A ![]() B+C在某一温度时,达到平衡。
B+C在某一温度时,达到平衡。
(1)若温度升高,平衡向正反应方向移动,则正反应是________反应(填“放热”或“吸热”);
(2)若B为固体,减小压强平衡向逆反应方向移动,则A呈______态;
(3)若A、B、C均为气体,加入催化剂,平衡______移动(填“正向”、“逆向”或“不”)
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、秋冬季节是流感发作的高峰期,“84消毒液”能有效杀灭流感病毒。巴蜀中学某同学购买的“84消毒液”瓶体部分标签如图所示,通常稀释100倍(体积比)后使用。请回答下列问题:
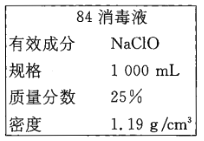
(1)该“84消毒液”的物质的量浓度约为______mol/L。
(2)该同学参阅“84消毒液”的配方,欲用NaClO固体配制250mL上述浓度的消毒液:
①需要用托盘天平称量NaClO固体的质量为_______g。
②实验中所用的玻璃仪器除烧杯、玻璃棒、量筒外,还有_____________。
(3)实验过程中下列操作或说法不正确的是_____。
A、容量瓶用蒸馏水洗净之后,应烘干后才能用于溶液的配制
B、配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致所得溶液浓度偏低
C、定容时,俯视刻度线会导致所得溶液浓度偏低
D、摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
(4)经过查阅资料,测定所配消毒液中NaClO的物质的量浓度的方法如下:准确取出10.00mL消毒液稀释至1000.00mL,量取稀释液20.00mL于锥形瓶中,加入过量的NaI溶液,用足量的醋酸酸化,充分反应后向溶液中滴加0.0500 mol/L Na2S2O3溶液,完全反应时消耗Na2S2O3溶液30.40mL。反应过程中的相关化学方程式为: ![]()
![]() ,通过计算求出所配消毒液中NaClO的物质的量浓度为___________mol/L 。(保留两位有效数字)
,通过计算求出所配消毒液中NaClO的物质的量浓度为___________mol/L 。(保留两位有效数字)
Ⅱ、某工厂的工业废水中含有大量FeSO4,较多的CuSO4和少量的Na2SO4,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。请根据下列流程,完成实验方案(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液)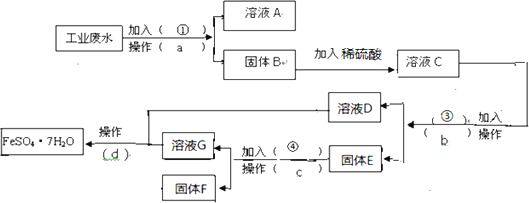
(1)操作a的名称为____,所需的玻璃仪器有_____。
(2)固体E的成分为____(填化学式),加入的试剂④为_________。
(3)加入试剂①的目的是__________。
(4)从溶液D和溶液G中得到FeSO4.7H2O晶体的操作为_______,过滤,洗涤,干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知电解质溶液的导电能力与离子浓度和离子所带电荷数均呈正相关。在两份等物质的量浓度且等体积的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
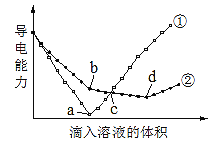
A.①代表滴加NaHSO4溶液的变化曲线
B.反应到b点时,过滤,向滤液中滴加溶液,发生反应的离子方程式为![]()
C.c点两溶液导电能力相同,所以两溶液中含有等物质的量浓度的OH—
D.a点对应的溶液显中性,d点对应的溶液显酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,向10 mL 0.10molL1-1YOH溶液中逐渐滴加0.20molL-1HX 溶液,混合溶液的pH 变化如图所示(温度和体积变化忽硌不计)。下列结论错误的是
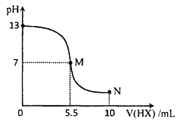
A.HX为一元弱酸,YOH 为一元强碱
B.M点对应溶液中水的电离程度大于N 点溶液中水的电离程度
C.N点对应溶液中粒子浓度:c(HX)> c(X - ) > c(Y+ ) > c(H+ ) > c(OH-)
D.室温时,pH = a 的YX溶液中水电离出的c(OH-)=l.0×10-(14-a)molL-1
查看答案和解析>>
科目: 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
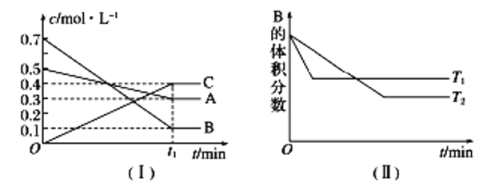
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为________,正反应为_____(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有______(填字母序号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目: 来源: 题型:
【题目】某结晶水合物的化学式为![]() ,其相对分子质量为M。25℃时,a g该晶体能够溶于b g水中形成VmL饱和溶液。下列关系中不正确的是( )
,其相对分子质量为M。25℃时,a g该晶体能够溶于b g水中形成VmL饱和溶液。下列关系中不正确的是( )
A.该溶液的密度ρ=![]()
B.该溶液的物质的量浓度为![]()
C.该溶液中溶剂与溶质的质量比为m(溶剂):m(溶质)=![]()
D.该溶液中溶质的质量分数为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某新型可充电电池构造如图所示,工作时(需先引发Fe 和KClO3的反应,从而使 LiCl-KCl共晶盐熔化),某电极(记为X )的反应式之一为:xLi++ xe- +LiV3O8=Lii+xV3O8。下列说法正确的是
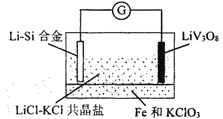
A.放电时,正极的电极反应式为: Li – e- = Li+
B.放电时,总反应式为:xLi + LiV3O8 = Lii+xV3O8
C.充电时,X电极与外接电源负极相连
D.充电时,X电极的质量增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com