
科目: 来源: 题型:
【题目】氨基钠(NaNH2)常用作有机合成的促进剂,是合成维生素 A 的原料。某学习小组用如下装置,以NH3和Na为原料加热至 350-360 ℃制备氨基钠,并检验其生成的产物和测定产品的纯度。
已知:NaNH2极易水解且易被空气氧化。回答下列问题 :

A C
(1)仅从试剂性质角度分析,下列各组试剂不宜用于实验室制备NH3的是________(填字母序号)。
A.浓氨水、CaO B. NH4Cl固体、Ca(OH)2固体
C.浓氨水 D.NH4NO3固体 、NaOH固体
(2)仪器D名称为___________,其中盛放的试剂为 ___________。
(3)装置A中发生反应的化学方程式为 __________,能证明装置A中已发生反应的实验依据是__________________________ 。
(4) 装置B的作用是______________ 。
(5) 制备时,通入的氨气过量,待钠充分反应后,取 mg 产品, 按如图装置进行实验(产品所含杂质仅为 Na2O )。

用注射器向试管中缓慢加入H2O至恰好完全反应立即停止,G中液面从刻度V1变 为 V2(已知V2>Vi,单位 mL,忽略固体体积,读取刻度时保持两使液面相平,实验过程处于标准状况下),则产品纯度为________:若读取V1时,G中液面低于漏斗侧液面,则所测得的纯度比实际产品纯度_________(填“偏高”、“ 偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组以链烧烃 (C4H6) 和丙烯醛( CH2= CHCHO) 为原料合成某药物中间体环戊基甲酸(部分反应条件、产物已省略),其流程如下:

已知:i.![]() +2RBr
+2RBr  +2HBr
+2HBr
ii. ![]() +2CO2
+2CO2
请回答下列问题:
(1) B中的官能团名称为________,D→E的反应类型是 ____________ .
(2)写出C与银氨溶液反应的化学方程式①:_____________ 。
(3)一定条件下,H可制取F, 则所需试剂和反应条件是____________________ 。
(4) I的结构简式为______________。
(5)环戊基甲酸与苯酚反应生成一种酯X,写出一种同时符合以下条件的 X 的同分异构体的结构简式:________(不考虑立体异构)。
①核磁共振氢谱有四组峰,峰面积比为9:2:2:l
②能与FeCl3发生显色反应
③与浓溴水反应时,l molX可消耗4mol Br2
(6)参照上述合成路线,设计以乙醇和化合物E为原料制备2.2-二乙基丙二酸(结构简式: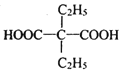 )的合成路线(无机试剂任选):___________________。
)的合成路线(无机试剂任选):___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组探究盐酸和NaOH反应过程中溶液pH的变化规律,得到如图所示曲线。下列有关该实验事实的说法正确的是( )
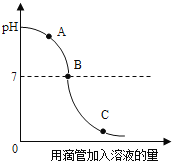
A.A点时溶液呈酸性
B.B点表示盐酸和NaOH恰好完全反应
C.C点时,溶液中的溶质只有氯化钠
D.该实验是将NaOH溶液滴入盐酸中
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年4月23日,中国人民军成立70周年。提到海军就不得不提航空母舰,我国正在建造第三艘航空母舰。航母的龙骨要耐冲击,甲板要耐高温,外壳要耐腐蚀.
(1)镍铬钢抗腐蚀性能强,基态C r 原子价层电子的电子排布式为_______________。
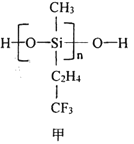
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图申所示)。基态Si原子电子占据最高能级的电子云轮廓图为_______形:H、C、O、Si 四种元素中的电负性最高的是______。
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①钛卤化物的熔点如下表所示:
TiF4 | TiCl4 | TiBr4 | TiI4 | |
熔点/℃ | 377 | -24 | 38 | 150 |
解释表中卤化物之间熔点差异的原因是________________________。
②OF2的空间构型为___________,其中O原子杂化方式为__________杂化。
③氯元素可以形成多种含氧酸,其酸性由弱到强的顺序为:HClO <HClO2<HClO3<HClO4。试解释其酸性强弱的原因是_______________ 。
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏大着极的资源,含有硅、氧、锰、锌等。如图是从铁氧体离子晶体Fe3O4 中取出的能体现其晶体结构的一个立方体。
①晶体中的氧离子是否构成了面心立方最密堆积?________(填“是”或“否”);
②已知:Fe3O4 晶体的密度为5. 18gcm -3, 根据该图计算a________nrn (写出计算式即可,阿伏加德罗常数的值为N A)

查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
A.升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.25℃时,欲使醋酸溶液pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸
查看答案和解析>>
科目: 来源: 题型:
【题目】某元素A形成气态的A2分子共有3种,其分子量分别为158、160、162,此三种分子的物质的量之比为7:10:7,则下列说法正确的是( )
A.该元素具有三种同位素
B.A的一种同位素的质量数为80
C.三种分子的平均相对分子质量为159
D.A的各种同位素的原子个数百分组成相同
查看答案和解析>>
科目: 来源: 题型:
【题目】SO2的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法、吸收法或电解法处理SO2。利用催化还原 SO2法 不仅可消除SO2污染,而且可得到有经济价值的单质S。
(1)已知CH4和S的燃烧热(△H)分别为-890.3 kJ/ mol和一297.2 kJ/ mol , 则CH4 催化还原SO2反应:CH4(g) +2 SO2 (g) =CO2(g)+ 2S(s)+ 2 H2O(1) △H =_____kJ/mol
(2)在恒容密闭容器中,用 H2还原SO2生成S 的反应分两步完成(如图1所示),该过程中相关物质的物质的量浓度随时间的变化关系如图2所示 :

分析可知X为_______(填化学式),o~t1时间段的温度为_______,o~ t1时间段用SO2表示的化学反应速率为______________。
(3)焦炭催化还原SO2生成S2, 化学方程式为2C(s)+ 2 SO2 (g)![]() S2(g)+2CO2(g)△H < 0。
S2(g)+2CO2(g)△H < 0。
实验测得:v正= k 正c2 (SO2 ) , v逆= k 逆c(S2 ) c2 ( CO 2) ( k正、k逆为速率常数,只与温度有关).某温度下,向2L的恒容密闭容器中充入lmol SO2,并加入足量焦炭,当反应达平衡时,SO2 转化率为80%,则:
①k正:k 逆=_______________。
②若升高温度,k正增大的倍数______( 填“> ”、“< ”或“= ”) k 逆增大的倍数。
(4) 利用如图所示装置(电极均为惰性电极)可吸收SO2。

直流电源a为_______极,电解时.电极B的电极反应式为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.N2电子式为![]()
B.Cl-的结构示意图为![]()
C.CO2的结构式为O—C—O
D.氯化镁的电子式:Mg2+[C![]() ]
]![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】现有1L未知成分的混合溶液,其中除了含有0.2mol/L的Na+外,还可能含有下列离子中的一种或几种:
![]()
现进行如下实验操作(每次实验所加试剂均过量):
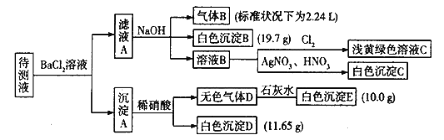
已知:①![]() ,②
,②![]() ,Cl2在常温下为黄绿色气体,可溶于水,其水溶液为浅黄绿色;Br2在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
,Cl2在常温下为黄绿色气体,可溶于水,其水溶液为浅黄绿色;Br2在常温下是深红棕色液体,微溶于水,其水溶液为黄色。
(1)由气体B可确定待测液中含有的离子是____________。
(2)由沉淀D和沉淀E可以判断待测液中一定含有_____离子,据此可以排除的离子是_____。
(3)由白色沉淀B可确定待测液中含有的离子是____,写出产生沉淀B的离子方程式_______。
(4)某同学读图后,认为待测液中一定不含Br—,他的判断依据是______。
(5)综合分析,待测液中![]() 的物质的量浓度的取值范围为________。
的物质的量浓度的取值范围为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )
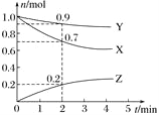
A. X+3Y![]() 2Z 0.1 mol/(L·min) B. 2X+Y
2Z 0.1 mol/(L·min) B. 2X+Y![]() 2Z 0.1 mol/(L·min)
2Z 0.1 mol/(L·min)
C. X+2Y![]() Z 0.05 mol/(L·min) D. 3X+Y
Z 0.05 mol/(L·min) D. 3X+Y![]() 2Z 0.05 mol/(L·min)
2Z 0.05 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com