
科目: 来源: 题型:
【题目】碘酸钾可用作食用盐的加碘剂,为无色或白色颗粒或粉末状结晶 ,加热至560℃ 开始分解,是一种较强的氧化剂,水溶液呈中性,溶解度在0℃ 时为4.74g,100℃ 时为32.3g。 下图是利用过氧化氢氧化法制备碘酸钾的工业流程 :

(1)步骤①需控制温度在70℃ 左右,不能太高,可能的原因是_______;不能太低 ,原因是________________________
(2)写出步骤②中主要反应的离子方程式:__________
(3)步骤⑤用冰水冷却至0℃ ,过滤出碘酸钾晶体,再用适量冰水洗涤2~3次。用冰水洗涤的优点是_____________
(4)产品纯度测定:取产品9.0g,加适量水溶解并配成250mL溶液。取出25.00mL该溶液并用稀硫酸酸化,加入过量的KI溶液,使碘酸钾反应完全,最后加入指示剂,用物质的量浓度为1.00molL-1的Na2S2O3溶液滴定,消耗25.00mL该滴定液时恰好达到滴定终点。已知![]()
①实验中可用_______作指示剂。
②产品的纯度为_____%(精确到小数点后两位)。求得的纯度比实际值偏大,可能的原因是________________________。
查看答案和解析>>
科目: 来源: 题型:
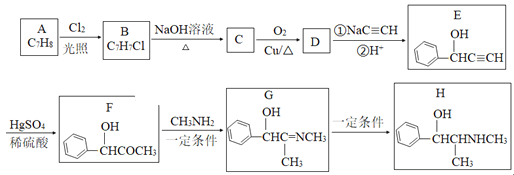
【题目】有机物H是一种中枢神经兴奋剂,其合成路线如图所示。
请回答下列题:
(1)A的化学名称为___,C的结构简式为___。
(2)E中官能团的名称为___。B→C、G→H的反应类型分别为___、__。
(3)D分子中最多有___个原子共平面。
(4)写出C→D反应的化学方程式为___。
(5)同时满足下列条件的E的同分异构体有___种(不考虑立体异构)。
①与E具有相同官能团;②苯环上有三个取代基。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W为短周期的四种元素,其最高正价依次为+1、+3、+5、+7,核电荷数按照Z、X、Y、W的顺序增大。已知Z的原子次外层的电子数为2,W、X原子次外层电子数为8。
(1)请写出元素Y的原子结构示意图_______________;其中元素W在周期表中的位置_______________________________。
(2)用电子式表示X在空气中生成的氧化物的形成过程:__________________________。
(3)X、Y、Z、W的原子半径由大到小的顺序为:_____________________________。(用元素符号表示)
(4)请写出W的单质与X的最高价氧化物对应水化物反应的离子方程式:_______________________________。
(5)写出Z与氢元素形成的10电子微粒化学式_____________________(任写两种)。
(6)元素X与元素Y相比,金属性较强的是_____(用元素符号表示),请举一例实验事实证明这一结论__________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)某同学取10 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=__________(保留2位有效数字)。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。需要准备的实验仪器有托盘天平、药匙、烧杯、胶头滴管、__________、__________。
(3)配制时,其正确的操作顺序是__________。
A 盖好瓶塞,反复上下颠倒,摇匀
B 根据计算结果,称量NaClO固体
C 将称好的NaClO固体放入烧杯中,用适量蒸馏水溶解
D 将烧杯中的溶液注入容量瓶,用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液均注入容量瓶,振荡
E 改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F 继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(4)下列操作使配制溶液浓度偏高的是________,使配制溶液浓度偏低的是_______,对配制溶液浓度无影响的是______(填序号)
①选用的容量瓶内有少量蒸馏水;
②定容时仰视容量瓶刻度线;
③定容时俯视容量瓶刻度线;
④烧杯中溶液倾倒完毕,忘记洗涤烧杯和玻璃棒;
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)典型物质的电子式
NH4Cl:__________Na2O2:________CO2:___________-OH:__________
(2)某短周期元素含氧酸的化学式为HXO3,其气态氢化物的化学式为HX,则X元素在周期表中的位置为_______。
(3)石油的综合利用方法有四种,其中____的目的是提高轻质油的产量,_____主要是得到甲烷、乙烯、丙烯等化工原料,_______是从石油中获得苯、甲苯等化工原料。
(4)填写有机除杂试剂
C2H6(C2H4) __________
乙酸乙酯(乙酸或乙醇)_____
乙醇(水)____________
苯(溴)________________
(5)无机方程式书写
①海带提碘的氧化环节,使用稀硫酸酸化的双氧水氧化I-的离子方程式为_______
②海水提溴吸收塔(SO2的水溶液)中的反应离子方程式为__________
③以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
a.高温下,向金红石与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体__________
b.在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛_____
(6)有机方程式书写
①乙醇去氢催化氧化生成乙醛的化学方程式:_______
②对苯二甲酸与乙二醇在一定条件下发生缩聚反应生成涤纶的化学方程式:___
③苯的硝化反应____________
查看答案和解析>>
科目: 来源: 题型:
【题目】已知NaHISO4溶于水时电离出Na+、H+、SO42-,某同学欲探究其化学性质,称取了12.0g NaHSO4,固体配成100mL溶液,做了如下实验:
①取20 mL该溶液加入足量Zn粒有大量气体生成;
②取20 mL该溶液加入Fe2O3后溶液变黄色;
③取20 mL该溶液加入BaCl2溶液后有大量白色沉淀产生。
请回答下列问题:
(1)该实验所配置的NaHSO4溶液物质的量浓度为__________。
(2)请用离子方程式解释①中的实验现象___________,该实验过程中产生的气体体积为__________(请按标准状况下计算)。
(3)请用离子方程式解释②中的实验现象_________________。
(4)请用离子方程式解释③中的实验现象__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物的结构是:关于它的性质的描述正确的是( )
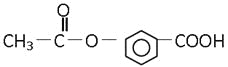
①能发生加成反应; ②能溶解于NaOH溶液中; ③能水解生成两种有机物;
④不能使溴水褪色; ⑤能发生酯化反应; ⑥有酸性
A. ①②③B. ②③⑤C. 仅⑥D. 全部正确
查看答案和解析>>
科目: 来源: 题型:
【题目】等体积,不同浓度的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质和量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量浓度之比是
A.1:2:3B.3:2:1C.6:3:2D.1:1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】关于乙醇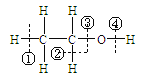 在化学反应中断键位置说法错误的是 ( )
在化学反应中断键位置说法错误的是 ( )
A. 乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应。
B. 乙醇与钠反应,在④位置断裂,对比钠与水反应,乙醇比水更难失去氢离子。
C. 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应。
D. 乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1mol CO2和2.7g水。
②用质谱仪测定其相对分子质量,得如图(Ⅰ)所示的质谱图。
③用核磁共振仪处理该化合物,得到如图(Ⅱ)所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:


(1)有机物A的相对分子质量是________。
(2)有机物A的实验式是________。
(3)A的分子式是________。
(4)推测有机物A的结构简式为____,A中含官能团的名称是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com