
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.31g白磷晶体中含有P-P键数是NA
B.22.4LSO2含有NA个SO2分子
C.标准状况下,等质量的NO2和N2O4所含有原子个数相等
D.1molCl2通入热的NaOH溶液中(产物是NaCl、NaClO3),充分反应后转移的电子数为NA个
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y、Z、W是中学常见的四种元素,原子序数依次增大。X的原子最外层电子数是次外层的2倍,Y 的氧化物属于两性氧化物,Y、Z 位于同周期,X、Y、Z的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)X在元素周期表中的位置是_________________。
(2)下列事实能用元素周期律解释的是_____________________________________(填字母序号)。
A.Y 的最高价氧化物对应水化物的碱性弱于Mg(OH)2
B.Z的气态氢化物的稳定性小于HF
C.WZ3的溶液可用于刻蚀铜制的印刷电路板
(3)Z的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是______________________。
(4)工业上用电解法制备Y单质,化学方程式为___________________________。
(5)家用“管道通”的有效成分是烧碱和Y 的单质,使用时需加入一定量的水,此时发生反应的化学方程式为______________________________。
(6)W的单质可用于处理酸性废水中的NO3-,使其转化成为铵根离子,同时生成磁性的W的氧化物H,再进行后续处理。相应离子方程式为____________。Y 的单质与H在高温下反应的化学方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列A、B、C、D是中学常见混合物分离或提纯的基本装置。请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
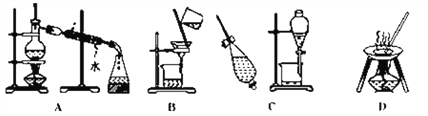
(1)除去Ca(OH)2溶液中悬浮的CaCO3_________________;
(2)从碘水提取碘______________;
(3)用自来水制取蒸馏水_________________;
(4)分离植物油和水_____________;
(5)与海水晒盐原理相符的是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
①标准状况下,6. 02×1023个分子所占的体积约是22. 4 L
②0. 5 mol H2所占体积为11. 2 L
③标准状况下,1 mol H2 O的体积为22.4 L
④标准状况下,28 g CO与N2的混 合气体的体积约为22. 4 L
⑤各种气体的气体摩尔体积都 约为22. 4 L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤B.④⑥C.③④⑥D.①④⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.1mol的KCl和0.1mol的AlCl3溶于水配成100mL混合溶液,下列溶液中Cl-浓度与该混合溶液中Cl-浓度相等的是
A. 3mol/L的NaCl溶液 B. 2mol/L的FeCl3溶液
C. 2mol/L的MgCl2溶液 D. 2mol/L的NaCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】NaClO2是一中重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示。请回答下列问题:
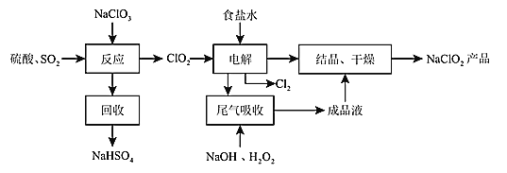
(1)NaClO2中Cl元素的化合价为_____________;
(2)写出“反应”步骤中生成ClO2的化学方程式________________________。
(3)“尾气吸收”步骤中发生的反应为2NaOH + H2O2 + 2ClO2 = 2NaClO2 + O2↑ + 2H2O ,其中氧化剂与还原剂的物质的量之比为_________;若有3 mol 电子发生转移,则有__________L(标准状况下)O2生成。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,是指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。则NaClO2的有效氯含量为_____(结果保留两位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示实验装置用于验证某些物质的性质。在A试管中装入足量的固体NaHCO3。试回答下列问题:

(1)在A试管内发生反应的化学方程式是_____________;
(2)B装置的作用是_____________________;
(3)在双球干燥管内发生反应的化学方程式为_________;
(4)实验时在C装置中观察到的现象是_______________;
(5)若将双球干燥管内的Na2O2换成Na2O,则实验时观察到的现象是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】填空:
(1)同温同压下,同体积的甲烷和二氧化碳物质的量之比为____,质量比为____;
(2)在标准状况下,4 g H2,11.2 L O2,1 mol H2O中,所含分子数最多的是______,体积最小的是________;
(3)硫酸钾和硫酸铝的混合溶液中,已知其中Al3+的浓度为0.4 mol/L,SO42-的浓度为0.7 mol/L,则K+的浓度为________mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2mL0.1mol/LBa(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色。
探究1:白色沉淀产生的原因。
(1)白色沉淀是___。
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
①支持甲同学观点的实验证据是_____________________________________。
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式___________________________________。
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
实验操作 | 实验现象 |
向2mL____mol/L____溶液(填化学式)中通入SO2 | ____________ |
探究2:在氧化SO2的过程中,NO3-和O2哪种微粒起了主要作用。
实验操作 | 实验数据 |
向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,通入SO2,用pH传感器测定溶液pH随时间(t)的变化曲线 |
图1:向BaCl2(无氧)溶液中通入SO2 |
向烧杯中分别加入25mL0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线。 |
图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 |
(3)图1,在无氧条件下,BaCl2溶液pH下降的原因是______________________________。
(4)图2,BaCl2溶液中发生反应的离子方程式为_________。
(5)依据上述图像你得出的结论是________,说明理由_________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】向四瓶盛有相同物质的量的NaOH溶液中通入体积不同的CO2气体,得到①②③④四瓶溶液。分别向四瓶溶液中逐滴加入等体积、等浓度的盐酸,产生的气体体积V(CO2)与所加盐酸体积V(HCl)的关系如下图所示,且图②③④中分别有0A<AB、0A=AB、0A>AB。则下列分析与判断正确的是(忽略CO2的溶解)( )

A.①中通入的CO2最少B.③中的溶质只有Na2CO3
C.有两种溶质的是②和③D.若④中AB>20A,则有c(Na2CO3)>c(NaHCO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com