
科目: 来源: 题型:
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入 1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如下图所示。

(1)从3 min到9 min,υ(H2)=________mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为______________。
(4)平衡时混合气体中CH3OH(g)的体积分数是__________________。
(5)一定温度下,第9分钟时υ逆(CH3OH) _______(填“大于”、“小于”或“等于”)第3分钟时υ正(CH3OH)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.NaCl(aq) ![]() Na(s)
Na(s) ![]() Na2O2(s)
Na2O2(s)
B.SiO2(s) ![]() Si(s)
Si(s) ![]() SiCl4(l)
SiCl4(l)
C.SO2(g) ![]() NH4HSO3(aq)
NH4HSO3(aq) ![]() (NH4)2SO4(aq)
(NH4)2SO4(aq)
D.Cu2(OH)2CO3(s) ![]() CuO(s)
CuO(s) ![]() Cu(OH)2(s)
Cu(OH)2(s)
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化钡广泛用于玻璃、陶瓷工业,是制取过氧化钡和钡盐的原料。一种利用钡泥[含BaCO3、BaSO3、Ba(FeO2)2等]制取氧化钡的绿色工艺流程如下:

回答下列问题:
(1)酸溶时,Ba(FeO2)2与稀硝酸反应的化学方程式为_____________________。
(2)产生滤渣1的反应离子方程式是____________________________________________。
(3)操作Ⅰ调pH=4~5的目的是_________________________________________________。
(4)过滤3所得母液应返回______________工序循环使用。
(5)Ba(NO3)2可用于汽车尾气中还原性气体的催化转化。科技工作者用H2模拟尾气中的还原性气体,研究Ba(NO3)2的催化还原过程。该过程分两步进行,如图表示该过程相关物质浓度随时间的变化关系。第二步反应消耗的NH3与NO3-的物质的量之比是_________。

(6)“气体2”为混合气体。标准状况下a L“气体2”溶于水得到bL溶液,则所得溶液的物质的量浓度为_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】化学学习小组在实验室中对铁盐与亚铁盐的相互转化进行如下探究。
已知:SCN-具有强还原性,易被氧化为(SCN)2。
实验Ⅰ:Fe3+转化为Fe2+

(1)Fe2(SO4)3溶液与Cu粉发生反应的离子方程式为________________________。
(2)探究白色沉淀产生的原因:
①提出假设:
假设1:白色沉淀是Fe2+与SCN-直接结合所得;
假设2:白色沉淀是Cu2+与SCN-直接结合所得;
假设3:_____________________________________________。
②实验验证:
向CuSO4溶液中通人过量SO2,将Cu2+还原,再加入KSCN溶液,观察到有白色沉淀生成,证明假设三成立。写出CuSO4溶液与KSCN溶液反应的离子方程式:________。
实验Ⅱ:Fe2+转化为Fe3+
实验方案 | 现象 |
向3mL 0.1mol·L-1 FeSO4溶液中加入3mL 4mol·L-1稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
(3)实验Ⅱ中,Fe2+转化为Fe3+的离子方程式是_____________________________。
(4)设计如下实验,探究溶液变为棕色的原因:
①向Fe2(SO4)3溶液中通入NO,溶液颜色无变化
②向FeSO4溶液中通入NO,溶液颜色变为棕色
③向Fe(NO3)3溶液中通入NO,溶液颜色无变化
由上述实验分析溶液变为棕色的原因是_________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)0.5 mol CH4的质量是_____________,在标准状况下的体积为____________;含电子的物质的量是_____________。
(2)同温同压下,等质量的O2和CO2 ,物质的量之比为______________,原子个数比为_____________,密度比为_______________。
(3)下列数量的各物质所含原子数按由大到小的顺序排列是____________________。
①0.5 mol氨气 ②标准状况下22.4 L氦气
③4 ℃时9 mL水 ④0.2 mol磷酸钠(Na3PO4)
查看答案和解析>>
科目: 来源: 题型:
【题目】“共生系统”能很大程度上提高经济效益。研究硫酸工业尾气的“共生系统”具有重要意义。回答下列问题:
(1)工业上,将Na2CO3和Na2S以合适的物质的量比配成溶液,吸收富集的SO2,可制取重要的化工原料Na2S2O3,同时放出CO2。该反应的化学方程式为___________________。
(2)工业上,将富含SO2的工业尾气降温液化,收集液态SO2。用液态SO2、硫磺(用S表示)、液氯为原料,在200℃~250℃活性炭催化条件下合成氯化剂SOCl2。该反应中氧化剂与还原剂的物质的量之比为________________。
(3)SOCl2分子的空间构型为______________。下列关于O、S、Se三种同主族元素的叙述正确的是____________(填序号)。
a.沸点:H2O>H2S>H2Se
b.H2O分子中H—O—H键的键角小于H2S分子中H—S—H键的键角
c.热稳定性H2O>H2S>H2Se
d.CS2是一种直线型分子,分子中C、S原子都满足8电子稳定结构
(4)氯化亚砜(SOCl2,易挥发液体,易水解)常用作脱水剂。ZnCl2·xH2O制取无水ZnCl2流程如图所示:

①利用SOCl2和ZnCl2·xH2O混合加热可制得无水ZnCl2的原因是_________________________________(用化学方程式和必要的文字解释)。
②甲同学认为SOCl2也可用于FeCl3·6H2O制取无水FeCl3,但乙同学认为该过程会发生氧化还原反应。要验证乙同学观点是否正确,可选择下列试剂中的___________(填序号)。
a.K3[Fe(CN)6]溶液 b.BaCl2溶液和稀盐酸
c.AgNO3溶液和稀硝酸 d.酸性KMnO4溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是中学化学常用于混合物分离和提纯的装置,请根据装置回答问题:
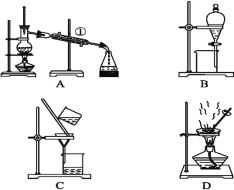
(1)从氯化钾溶液中得到氯化钾固体,选择装置____(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置_________。
(2)从碘水中分离出I2,选择装置____,该分离方法的名称为__________。
(3)装置B在分液时为使液体顺利下滴,应进行的具体操作是__________________________
(4)海水中蕴藏着丰富的资源,取少量海水按如下流程进行实验:
海水![]() 粗盐
粗盐![]() 食盐水
食盐水![]() 氯化钠晶体
氯化钠晶体
粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是____(填写字母序号)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】(12分)现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
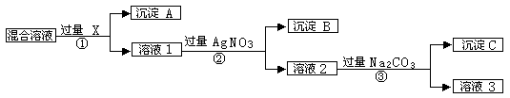
请回答下列问题:
⑴写出实验流程中下列物质的化学式: 试剂X : ,沉淀A:
⑵上述实验流程中加入过量的Na2CO3的目的是 。
⑶按此实验方案得到的溶液3中肯定含有 (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的 ,之后若要获得固体NaNO3需进行的实验操作是 (填操作名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中分子数相同的是( )
A.2 L CO和2 L CO2B.9 g H2O和标准状况下11.2 L CO2
C.标准状况下1 mol O2和22.4 L H2OD.0.2 mol NH3和4.48 L HCl气体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法正确的是( )
A.臭氧的摩尔质量是48 g
B.同温同压条件下,等质量的氧气和臭氧体积比为2∶3
C.16 g臭氧中含有6.02×1023个原子
D.1.00 mol臭氧中含有电子总数为18×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com