
科目: 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
Al | NaAlO2 | Al(OH)3 | Al2O3 | ||
② | Na | NaOH | Na2CO3 | NaCl | |
③ | C | CO | CO2 | H2CO3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①② B. ①③④ C. ②③ D. ①④
查看答案和解析>>
科目: 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. N2![]() NO2
NO2![]() HNO3
HNO3
B. 石油![]() CH3CH3
CH3CH3![]() CH2BrCH2Br
CH2BrCH2Br
C. Al ![]() Al(NO3)3(aq)
Al(NO3)3(aq)![]() Al(OH)3(s)
Al(OH)3(s)
D. CH2=CH2 ![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示过程除去 AlCl3溶液中含有的 Mg2+、K+ 杂质离子并尽可能减小 AlCl3 的损失。下列说法正确的是
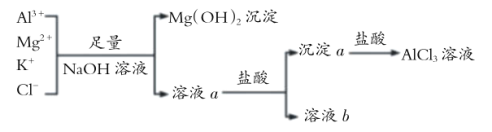
A.NaOH 溶液可以用Ba(OH)2溶液来代替B.溶液a中含有 Al3+、K+、Cl-、Na+、OH-
C.溶液 b 中只含有 NaClD.向溶液a和沉淀a中滴加盐酸都要过量
查看答案和解析>>
科目: 来源: 题型:
【题目】3 mol A和2.5 mol B混合于2 L密闭容器中,发生的反应:3A(g)+B(g)![]() xC(g)+2D(g) 5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1 mol/(L·min),下列结论不正确的是
xC(g)+2D(g) 5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1 mol/(L·min),下列结论不正确的是
A. A的平均反应速率为0.15mol/(L·min)
B. 平衡时,A的转化率为20%
C. 平衡时,C的浓度为 0.25 mol/L
D. 容器内的起始压强和平衡压强之比为11:10
查看答案和解析>>
科目: 来源: 题型:
【题目】欲进行下列实验,其方案设计合理的是
A | B | C | D |
检验装置气密性 | 制过氧化钠 | 验证浓H2SO4的脱水性、强氧化性 | 比较NaHCO3和Na2CO3溶解度 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.物质的量浓度为0.5 mol/L的MgCl2溶液中含有NA个Cl-
C.标准状况下,11.2 L H2O含有的分子数为0.5 NA
D.在常温常压下,1.06 g Na2CO3含有的Na+数为0.02 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用密度为1.25g·mL-1,质量分数36.5%的浓盐酸配制0.1mol·L-1的盐酸240mL,请回答下列问题:
(1)浓盐酸的物质的量浓度为_______。
(2)配制240 mL0.1mol·L-1的盐酸应选用_______mL的容量瓶,需要量取浓盐酸体积为_______mL。
(3)定容时,除了烧杯、玻璃棒、容量瓶外,还需要的玻璃仪器是_______。
(4)正确的操作顺序是________(填序号)
①用胶头滴管逐滴加水,使溶液凹液面恰好与容量瓶刻度线相切
②向容量瓶中加水至液面接近瓶颈上的刻度线1-2cm处
③根据计算,用量筒称取一定体积的浓盐酸
④将容量瓶盖紧,振荡,摇匀
⑤将浓盐酸倒入烧杯中加水稀释,并不断用玻璃棒搅拌,静置待其冷却
⑥将溶液用玻璃棒引流注入查漏过的容量瓶中
⑦少量水洗涤烧杯及玻璃棒2至3次,并将每次的洗涤液也注入容量瓶中
(5)下列操作对所配溶液的浓度大小有何影响 (填“偏大”、“偏小”或“无影响”)。
①定容时,俯视刻度线,浓度_________;
②定容摇匀后发现溶液凹面低于刻度线,加水至刻度线,浓度________。
查看答案和解析>>
科目: 来源: 题型:
【题目】100℃时,向某恒容密闭容器中加入1.6 mol ·L-1的Q后会发生如下反应:2Q(g) ![]() M(g) 。其中M的物质的量浓度随时间的变化如图所示。
M(g) 。其中M的物质的量浓度随时间的变化如图所示。
下列说法错误的是

A.从反应开始到刚达到平衡时间段内,v(Q)=0.02 mol·L-1·s-1
B.a、b两时刻生成Q的速率:v(a)<v(b)
C.用Q浓度变化值表示的ab、bc两个时段内的反应速率:v(ab)>v(bc)=0
D.其他条件相同,起始时将0. 2 mol·L-1氦气与Q混合,则反应达到平衡所需时间少于60 s
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)3.6gH2O物质的量为________mol,约含有_______个原子;
(2)已知1.204×1023个X气体的质量是6.4g。则X气体的摩尔质量是________;
(3)制备Fe(OH)3胶体的化学方程式:________;
(4)实验室通常用MnO2和浓盐酸共热制取Cl2,反应的化学方程式为(MnCl2是可溶性盐)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,该反应中氧化剂是_______,氧化产物是________(填化学式),写出上述化学方程式对应的离子方程式__________。
MnCl2+Cl2↑+2H2O,该反应中氧化剂是_______,氧化产物是________(填化学式),写出上述化学方程式对应的离子方程式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将4 mol A(g)和2 mol B(g)在2 L的恒容密闭容器中混合并在一定条件下发生反应:2A(g)+B(g) 2C(g) ΔH<0,反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是
A.2 s后物质A的转化率为70%
B.当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态
C.达到平衡状态时,增加A的物质的量,A和B的转化率都提高
D.达到平衡状态时,升高温度,平衡逆向移动,同时化学平衡常数K减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com