
科目: 来源: 题型:
【题目】AA705合金(含Al、Zn、Mg和Cu)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。但这种合金很难被焊接。最近科学家将碳化钛纳米颗粒(大小仅为十亿分之一米)注入AA7075的焊丝内,让这些纳米颗粒充当连接件之间的填充材料。注入了纳米粒子的填充焊丝也可以更容易地连接其他难以焊接的金属和金属合金。回答下列问题:
(1)基态铜原子的价层电子排布式为__________。
(2)第三周期某元素的前5个电子的电离能如图1所示。该元素是_____(填元素符号),判断依据是_______。

(3)CN—、NH3、H2O和OH—等配体都能与Zn2+形成配离子。1mol [Zn(NH3)4]2+含___ molσ键,中心离子的配位数为_____。
(4)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有_____个镁原子最近且等距离。
(5)在二氧化钛和光照条件下,苯甲醇可被氧化成苯甲醛:

①苯甲醇中C原子杂化类型是__________。
②苯甲醇的沸点高于苯甲醛,其原因是__________。
(6)钛晶体有两种品胞,如图所示。

①如图3所示,晶胞的空间利用率为______(用含п的式子表示)。
②已知图4中六棱柱边长为x cm,高为y cm。该钛晶胞密度为D g·cm-3,NA为______mol—1(用含x y和D的式子表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将2mol A和2mol B两种气体相混合于体积为2L的某密闭容器中(容积不变),发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),2min末反应达到平衡状态(温度不变),生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态(温度不变),生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)X的值等于__________;
(2)A的转化率为_________________。
(3)生成D的反应速率为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃、101 kPa时某些物质的燃烧热数据如下:
名称 | 化学式 | ΔH (kJ/mol) | 名称 | 化学式 | ΔH (kJ/mol) |
石墨 | C(s) | 393.5 | 乙烷 | C2H6(g) | 1560 |
金刚石 | C(s) | 395.0 | 乙烯 | C2H4(g) | 1411 |
氢气 | H2(g) | 285.8 | 乙炔 | C2H2(g) | 1300 |
一氧化碳 | CO(g) | 283.0 | 乙醇 | C2H5OH(l) | 1367 |
(1)相同质量的上述八种物质,完全燃烧放热最多的名称是____。
(2)石墨与金刚石互为____。
a.同位素 b.同素异形体 c.同分异构体 d.同系物
常温常压下,二者更稳定的是___。(填中文名称)
(3)在标准状况下,22.4LCO和C2H2的混合气体在过量的氧气中完全燃烧放出1096.6 kJ的热,则燃烧产生的CO2的物质的量为___mol。
(4)估算在Ni作催化剂时,乙烯与氢气发生加成反应的焓变。C2H4(g)+H2(g)=C2H6(g) ΔH=____。
(5)已知破坏下列化学键需要吸收的能量如下:
C-C | C=C | H-H |
347kJ/mol | 619kJ/mol | 436kJ/mol |
根据(4)的结论,估算C-H键的键能为____kJ/mol。
a.322.5 b.422.5 c.522.5 d.622.5
查看答案和解析>>
科目: 来源: 题型:
【题目】氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl、NHCl2和NCl3)。
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质的结构式为________,二氯胺与水反应的化学方程式为_____________。将0.01 mol NCl3通入100 mL 0.5 mol/L Na2SO3溶液中,转移电子的物质的量为_______mol。
(2)已知部分化学键的键能和化学反应的能量变化如下表和下图所示。
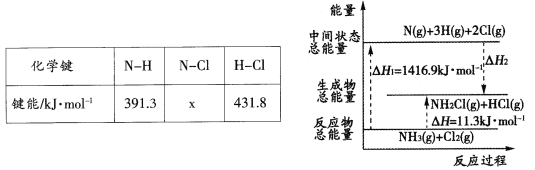
则反应过程中的△H2=____kJ·mol-1,表中的x=_____。
(3)在密闭容器中反应NH3(g)+Cl2(g)![]() NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,通过热力学定律计算,不同温度下理论上NH2Cl的体积分数随![]() 的变化如下图所示。
的变化如下图所示。
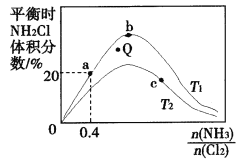
①a、b、c三点对应平衡常数的大小关系是(分别用Ka、Kb、Kc表示)_________。b点时,该反应的平衡常数为________;
②T2℃,Q点对应的速率:![]() __________
__________![]() (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
③在氨氯比一定时,提高NH3的转化率的方法是__________(任写1种);
④若产物都是气体,实验测得NH2C1的体积分数始终比理论值低,原因可能是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】水煤气变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g)。我国研究人员结合实验与计算机模拟结果,揭示了在金催化剂表面上水煤气变换的反应历程(如图所示),其中吸附在金催化剂表面上的物质用·标注。下列说法正确的是
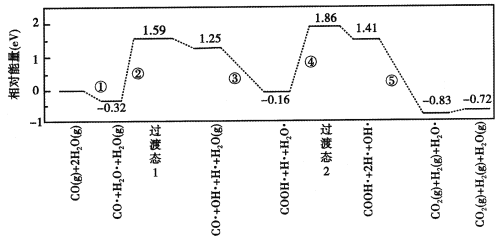
A.水煤气变换反应的△H<0
B.该历程中最大能垒(活化能)E正=1.70 eV
C.步骤⑤只有H-H键和H-O键形成
D.步骤③的转化关系可表示为:CO·+OH·+H2O(g)=COOH·+H2O·
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于实验室制氯气的说法中错误的是( )
A.该反应是一个氧化还原反应,其中二氧化锰是氧化剂
B.每生成1mol氯气,就要转移2mol电子
C.该反应的离子方程式为MnO2+4H++4Cl-![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.该方法是瑞典化学家舍勒最先发现的
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 强酸跟强碱的反应热一定是中和热
B. 1molC完全燃烧放热383.3kJ,其热化学方程为:C+O2=CO2ΔH=-383.3kJ·mol-1
C. 在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热叫做中和热
D. 表示中和热的离子方程式为:H+(aq)+OH-(aq)![]() H2O(l);ΔH=57.3KJ·mol-1
H2O(l);ΔH=57.3KJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】T℃时,在20.00 mL 0.10 mol/LCH3COOH溶液中滴入0.10 mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是

A.T℃时,CH3COOH的电离平衡常数Ka=1.0×10-3
B.M点对应的NaOH溶液的体积为20.00 mL
C.N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.N点与Q点所示溶液中水的电离程度:N>Q
查看答案和解析>>
科目: 来源: 题型:
【题目】某科学兴趣小组查阅资料得知,反应温度不同,氢气还原氧化铜的产物就不同,可能是Cu或Cu2O,Cu和Cu2O均为不溶于水的红色固体,但Cu2O能与稀硫酸发生反应:Cu2O+H2SO4=CuSO4+Cu+H2O。为探究反应后的红色固体的成分,他们提出了以下假设:
假设一:红色固体只有Cu
假设二:红色固体只有Cu2O
假设三:红色固体中有Cu和Cu2O
下列判断正确的是
A.取少量红色固体,加入足量的稀硫酸,若溶液无明显现象,则假设一和二都成立
B.少量红色固体与足量稀硫酸反应,若溶液呈蓝色且仍有红色固体,则只有假设三成立
C.若将7.2克红色固体通入足量的H2还原,最后得到固体6.4克,则假设二成立
D.实验室可用向新制Cu(OH)2悬浊液(碱性)中加入葡萄糖后加热,来制取Cu2O
查看答案和解析>>
科目: 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段,氮元素的常见化合价与部分物质类别的对应关系如图所示。
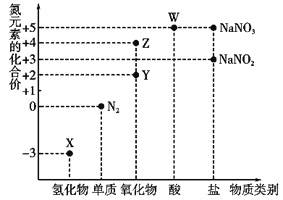
(1)从氮元素化合价的角度分析,X、Y、Z、W中既具有氧化性又具有还原性的有______(填化学式)。
(2) N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_______________。尾气中的NO用酸性NaClO溶液吸收,其原理是HClO氧化NO生成Cl和NO3-,其离子方程式为______________________________________。
(3)将集满红棕色气体Z的试管倒置于盛有水的水槽中,观察到的现象为_______________________。
(4)W的稀溶液与铜单质发生反应的离子方程式为__________________________。
(5)已知NaNO2能被酸性KMnO4溶液氧化为NaNO3,则50mL0.01 mol·L-1 NaNO2溶液与10mL0.02 mol·L-1 KMnO4溶液恰好完全反应时,还原产物中Mn元素的化合价为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com