
科目: 来源: 题型:
【题目】将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。则下列说法错误的是( )
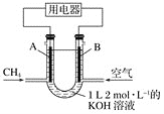
A.通入CH4的一端为原电池的负极,通入空气的一端为原电池的正极
B.0<V≤22.4 L时,电池总反应的化学方程式为CH4+2O2+2KOH=K2CO3+3H2O
C.22.4 L<V≤44.8 L时,负极电极反应为CH4-8e-+![]() +3H2O=
+3H2O=![]()
D.V=33.6 L时,溶液中只存在阴离子![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.lmolL-1的盐酸滴定10.0mL0.lmolL-1Na2A溶液,所得滴定曲线如图所示.下列说法正确的是
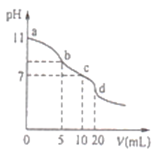
A.常温下,A2-的水解常数Khl(A2-)的数量级为10-6
B.b点溶液中:c(HA-)+2c(H2A)+c(H+)=c(Cl-)+c(OH-)
C.c点溶液中:c(HA-)+c(A2-)+c(H2A)=0.lmolL-1
D.d点溶液中:c(A2-)+c(HA-)=c((H+)<c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】有一镁铝合金共51 g,把其加入到1 L 5 mol·L-1的盐酸中,恰好反应完。
(1)关于合金的下列说法正确的有________。
A.合金只能由两种或两种以上的金属组成
B.合金的硬度一般比其组成成分金属的硬度大
C.镁铝熔成合金的过程是一个化学过程
D.合金的熔点一般比其组成成分的熔点低
E.合金具备金属的特性
(2) 该合金中镁铝的质量分别为________g、________g。
(3) 反应中共收集到标况下的氢气的体积为___________L。
(4)向反应后的溶液中逐滴加入5 mol·L-1的NaOH溶液,若要使沉淀恰好达到最大值,需要加入NaOH________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积恒定的密闭容器中,一定量的二氧化硫与1.100mol氧气在催化剂作用下加热到600℃发生反应:2SO2+O2![]() 2SO3。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是( )
2SO3。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是( )
A. 三氧化硫生成的速率与二氧化硫消耗的速率相等时反应达到平衡
B. 降低温度,正反应速率减小,逆反应速率增大
C. 平衡混合气体通入过量氯化钡溶液中,得到沉淀的质量为161.980g
D. 达到平衡时,二氧化硫的转化率为90%
查看答案和解析>>
科目: 来源: 题型:
【题目】燃料电池发电站,与普通火力发电站相比,其有害物排放少,运行噪音低,被誉为“绿色”发电站。如图为某空气燃料电池工作原理,下列说法错误的是
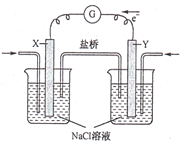
A.该电池工作时,X电极附近的溶液pH升高
B.该电池工作时,盐桥中的阴离子向Y电极移动
C.若用甲醇作燃料,则X电极上的反应为CH3OH-6e-+H2O=CO2+6H+
D.若用甲烷作燃料,当电路中通过0.8mol电子时,则消耗甲烷的质量为1.6g
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以软锰矿(主要成分是MnO2,还含有少量SiO2、Fe2O3)为主要原料制备高性能的磁性材料碳酸猛(MnCO3)。其工业流程如图所示,下列说法错误的是
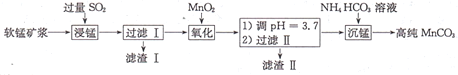
A.滤渣I可用于制造光导纤维、滤渣II可用于制作颜料
B.“浸锰”过程MnO2参与反应的化学方程式为MnO2十SO2=MnSO4
C.“沉锰”时,反应体系的温度越高,越有利于生成MnCO3
D.检验高纯碳酸锰是否洗涤干净,可选用BaCl2溶液和盐酸试剂
查看答案和解析>>
科目: 来源: 题型:
【题目】利用湿法工艺从阳极泥(主要含有Cu、Ag、Au)中提取Ag、Au的流程如图所示:
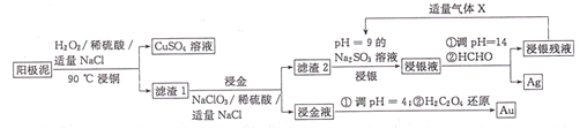
回答下列问题:
(1)“浸铜”时,铜参与反应的离子方程式为______________;若温度过高,铜的浸出率会降低,原因是______________。
(2)“浸金液”的主要成分是H[AuCl4],则“浸金”步骤发生反应的化学方程式为NaCl+NaClO3+Au+H2SO4→Na2SO4+H2O+H[AuCl4](未配平),该反应中氧化剂与还原剂物质的量之比为______________,“王水”也可溶解金,王水的成分为______________。
(3)从“浸金液”中提取金时氧化剂和还原剂的物质的量之比为______________。
(4)“浸银”时发生反应AgCl+2SO32-![]() Ag(SO3)23-+C1-,Ag(SO3)23-将HCHO氧化为CO32-。向“浸银残液”中通入气体X,可得到Na2SO3再生液,X的化学式为______________,Na2SO3再生液的循环使用次数与银的浸出率关系如图所示:
Ag(SO3)23-+C1-,Ag(SO3)23-将HCHO氧化为CO32-。向“浸银残液”中通入气体X,可得到Na2SO3再生液,X的化学式为______________,Na2SO3再生液的循环使用次数与银的浸出率关系如图所示:
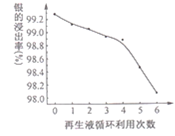
从平衡移动角度解释上述曲线的变化原因:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在如图所示的三个容积相同的容器①②③中进行如下反应:3A(g)+B(g) ![]() 2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )

A. ③②①B. ③①②C. ①②③D. ②①③
查看答案和解析>>
科目: 来源: 题型:
【题目】降冰片烯(结构见 F)的衍生物在橡胶工业有重要用途。一种利用脱羰偶联反应合成其衍生物的路线如下:

回答下列问题
(1)A→B 所需的试剂为_______________ 。
(2)B→C 第一步反应的化学方程式为_____。
(3)D 的结构简式为_____,C→D 的反应类型为_______。
(4)E 中的官能团名称为_____。
(5)芳香化合物X 是E 的同分异构体,X 能与热的NaOH 溶液反应生成稳定化合物, 0.1mol X 消耗 NaOH 0.2mol,化合物 X 共有_____种(不考虑立体异构)。其中核磁共振氢谱显示有 5 种不同化学环境的氢,峰面积比为 2∶2∶2∶1∶1 的结构简式为_____。
(6)参照上述路线,设计由苯甲醛、甲醇和 制备成
制备成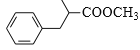 路线_____。(无机试剂任选)
路线_____。(无机试剂任选)
查看答案和解析>>
科目: 来源: 题型:
【题目】电—Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应,Fe2++H2O2=Fe3++OH-+OH,生成的烃基自由基(OH)能氧化降解有机污染物。下列说法正确的是( )
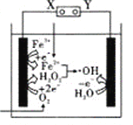
A. 电解池左边电极的电势比右边电极的电势高
B. 电解池中只有O2和Fe3+发生还原反应
C. 消耗1 molO2,电解池右边电极产生4mol OH
D. 电解池工作时,右边电极附近溶液的pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com