
科目: 来源: 题型:
【题目】某实验小组尝试在钢制钥匙上镀铜。
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。
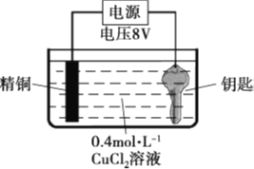
实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是_______。
(2)实验II中钥匙应与电源的_______极连接。
(3)钥匙表面产生的气体是_______。
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是________。
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是________。(已知CuOH是一种难溶于水的黄色固体)
查看答案和解析>>
科目: 来源: 题型:
【题目】氰(CN)2,硫氰(SCN)2等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为: Cl-<Br-<CN-<SCN-<I-,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是
A.4HCN(浓)+MnO2![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
B.(CN)2+H2O=2H++CN-+CNO-
C.(CN)2+2OH-=CN-+CNO-+H2O
D.(CN)2+2SCN-=2CN-+(SCN)2
查看答案和解析>>
科目: 来源: 题型:
【题目】ag 硝酸钾溶于bg水,形成VmL饱和溶液。下列关系式错误的是( )
A. 该溶液的物质的量浓度:c(KNO3)=![]() mol·L-1
mol·L-1
B. 该溶液的质量分数:w(KNO3)=![]() %
%
C. 20 ℃时KNO3的溶解度S=![]() g
g
D. 该溶液的密度ρ=![]() g·L-1
g·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加罗常数的值,下列说法正确的是( )
A.标准状况下,22.4 L H2O中含有氢原子数目为2NA
B.17 g NH3所含质子数为10NA
C.0.1 mol Cu(NO3)2中含有的离子数目为0.2NA
D.28 g N2体积为22.4L
查看答案和解析>>
科目: 来源: 题型:
【题目】能源在人类生活中应用广泛。回答下列问题:
(1)氢气燃烧时放出大量的热,这是由于反应物的总能量____生成物的总能量(选填“大于”“小于”或“等于”,下同),从化学反应的本质角度来看,是由于断裂反应物中的化学键吸收的总能量_____形成产物的化学键释放的总能量。
(2)H2被认为是21世纪矿物燃料的理想能源,每克氢气和汽油燃烧放出的热量分别为55kJ和46kJ。汽油可由石油经___和____获得;请分析氢气作为能源替代汽油的优势:_____;____(写两点)。
(3)在氢氧碱性燃料电池中,负极发生反应的电极反应式:___,正极的电极反应式为____。若反应后得到5.4g液态水,此时氢氧燃料电池转移的电子数为____。
(4)如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。

片刻后可观察到的现象是(指悬吊的金属圈)____。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(5)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
①写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_____。
②若将①中的反应设计成原电池,写出负极的电极反应式____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
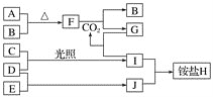
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2其原理如图所示,正确的是( )

A. 通电后,H+通过质子交换膜向右移动,最终右侧溶液pH减小
B. 电源A极为负极
C. 通电后,若有22.4LH2生成,则转移2mol电子
D. 与电源A极相连的惰性电极上发生的反应为CH3COOH-8e-+2H2O=2CO2↑+8H+
查看答案和解析>>
科目: 来源: 题型:
【题目】应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下"Fe与水蒸气反应的实验"。
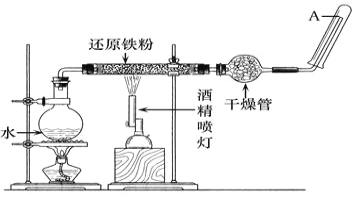
请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是_____________。
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_______________;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_______________。
(3)酒精灯和酒精喷灯点燃的顺序是__________。
(4)干燥管中盛装的物质可以是_____________,作用是__________。
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行_________,这一操作的目的_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知常温下,酸性:HF>HCN,分别向1L1mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积的变化),溶液中的(X表示F或CN)随pH变化如图所示,下列说法正确的是
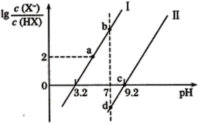
A.HF的电离常数Ka(HF)的数量级10-4
B.d点溶液中:c(Na+)=c(X-)>c(HX)
C.a到b点的过程中水的电离程度先变大后变小
D.b点溶液和d点溶液中c(Na+):b<d
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图装置可以验证非金属性的变化规律。
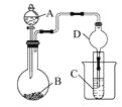
(1)仪器A的名称为________,干燥管D的作用是________________。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。
(3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com