
科目: 来源: 题型:
下列离子方程式不正确的是( )。
A.硝酸跟氢氧化钠溶液;
H++OH—=H2O
B.氯化铝溶液跟偏铝酸钠溶液反应:
Al3++3A1O2—+6H2O=4Al(OH)3↓
C.氢氧化钾溶液与碳酸氢钙溶液混合;
Ca2++2OH—+2HCO3—=CaCO3↓+CO32—+2H2O
D.碳酸钠溶液跟盐酸混合;
Na2CO3+2H+=2Na++CO2↑十H2O
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| △ |

| HIO4△ |
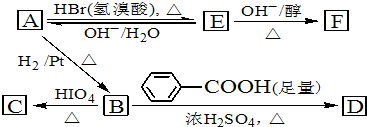
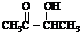
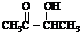
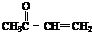
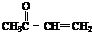
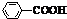 +
+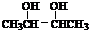

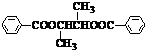 +2H2O
+2H2O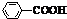 +
+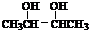

 +2H2O
+2H2O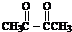
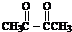
查看答案和解析>>
科目: 来源: 题型:
 ,请填空:
,请填空: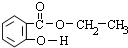 是其中之一,它属于(填字母)
是其中之一,它属于(填字母)

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:阅读理解
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g/100g水 | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |

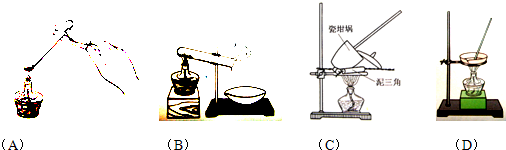
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com