
科目: 来源: 题型:
【题目】废气中的 H2S 通过高温热分解可制取氢气:2H2S(g) ![]() 2H2(g)+S2(g)。现在 3L 密闭容器中,控制不同 温度进行 H2S 分解实验。
2H2(g)+S2(g)。现在 3L 密闭容器中,控制不同 温度进行 H2S 分解实验。
(1)某温度时,测得反应体系中有气体 1.31mol,反应 tmin 后,测得气体为 1.37mol,则 tmin 内 H2 的生成 速率为___________________。
(2) 某温度时,可作为判断反应达到平衡的标志依据是_____(选填编号)。
a. 气体的压强不发生变化 b. 气体的密度不发生变化
(3)实验结果如图。图中曲线 a 表示 H2S 的平衡转化率与温度关系,曲线b 表示不同温度下、反应经过相同时间且未达到化学平衡时 H2S 的转化率。
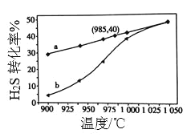
该反应为________反应(填“放热”或“吸热”)。在容器体积不变的情况下, 如果要提高 H2的体积分数,可采取的一种措施是_______________________
(4)使 1LH2S 与 20L 空气(空气中 O2 体积分数为 0.2)完全反应后恢复到室温,混合气体的体积是________L。若 2gH2S 完全燃烧后生成二氧化硫和水蒸气,同时放出 29.4kJ 的热量,该反应的热化学方程式是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是硫酸试剂瓶标签上的部分内容。据此下列说法中正确的是( )
硫酸 化学纯CP500 mL
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84 g·cm-3
质量分数:98%
A.该硫酸的物质的量浓度18.0 mol·L-1
B.1molZn与足量的该硫酸反应能产生22.4L H2
C.配制230mL4.6mol·L-1的稀硫酸需取该硫酸62.5mL
D.若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可用微生物处理含 KCN 的废水。第一步是微生物在氧气充足的条件下,将 KCN 转化成 KHCO3和 NH3(最佳 pH:6.7~7.2);第二步是把氨转化为硝酸:NH3+2O2 ![]() HNO3+H2O。 请完成下列填空:
HNO3+H2O。 请完成下列填空:
(1) 写出第一步反应的化学反应方程式_____,第二步反应的还原产物是________________(填写化学式)。
(2) N 原子、H 原子、O 原子的半径由大到小的顺序是____________________。
(3) 碳原子的结构示意图为________________,水分子的电子式为_______________________。
(4) 室温下,0.1mol/LK2CO3、KCN、KHCO3 溶液均呈碱性且 pH 依次减小,则 0.1mol/L 的 KCN、KHCO3、K2CO3 溶液中,CN-、HCO3-、CO32-的物质的量浓度由大到小的顺序是_____。
(5) 工业上还常用氯氧化法处理含 KCN 的废水:KCN+2KOH+Cl2=KOCN+2KCl+H2O,2KOCN+4KOH+3Cl2=N2+6KCl+2CO2+2H2O。两者相比,微生物处理法的优点与缺点是(各写一条)。 优点:__________________,缺点:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】从元素化合价变化的角度分析,下列反应中,画线的物质发生氧化反应的是
A. SO2 + 2NaOH = Na2SO3 + H2O B. 2CuO + C![]() 2Cu + CO2↑
2Cu + CO2↑
C. 2FeCl3 + Fe = 3FeCl2 D. Zn+2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】向溶液中加入新物质时, 其导电性(I)符合下图变化趋势的实验操作是

A. 乙酸溶液中通入氨气至过量
B. 石灰水中通入CO2至过量
C. 亚硫酸中通入氯气至过量
D. 氨水中通入氯化氢气体
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气和氟气反应生成氟化氢的过程中能量变化如图所示。由图可知

A. 生成1 molHF气体放出的热量为270 kJ
B. H2(g)+ F2(g)→ 2HF(l)+ 270 kJ
C. 反应物的总能量大于生成物的总能量
D. 该反应是吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用化学平衡移动原理解释的是
A.新制氯水长时间放置颜色变浅
B.高压比常压更有利于 SO2 转化为 SO3
C.蒸干 AlCl3 溶液无法得到无水 AlCl3
D.滴加少量 CuSO4 溶液可以加快 Zn 与稀 H2SO4 反应的速率
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
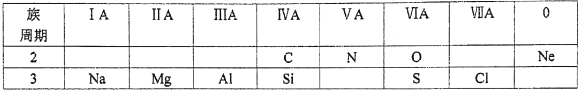
(1)镁的原子结构示意图为____。
(2)H2SO4与HClO4中,酸性较强的是____。
(3)NaOH与Al (OH)3中,属于两性氢氧化物的是____。它常用作治疗胃酸(含盐酸)过多的药物,该反应的离子方程式为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.22.4 L H2O的物质的量为1mol
B.常温常压16 g O2的物质的量为0.5mol
C.标准状况下16 g O2中含有的氧原子数为0.5mol
D.物质的量浓度为0.5 mol·L-1 MgCl2 溶液中,Cl-浓度为0.5 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
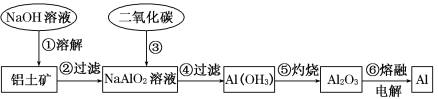
(1)请用离子方程式表示以上工艺流程中第①步反应:_____________________。
(2)写出以上工艺流程中第③步反应的离子方程式:___________________________。
(3)若第③步加入的是过量的盐酸,则发生反应的化学方程式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com