
科目: 来源: 题型:
【题目】.某兴趣小组采用10.0 g废易拉罐(含90%的Al,还含有少量的Fe、Mg等杂质)制备明矾[KAl(SO4)2·12H2O]的实验流程如图:

(1)试剂①应选用________(填字母)。
a.盐酸 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为__________________________。
(3)从溶液C中得到明矾的实验操作为________、________、过滤,如用图所示装置进行该操作,其中的一处主要错误是______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】反应A(g)+3B(g)![]() 2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是( )
2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是( )
A. v(A)=0.15 mol·L-1·min-1B. v(B)=0.01 mol·L-1·s-1
C. v(C)=0.40 mol·L-1·min-1D. v(D)=0.45 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的定容密闭容器中,发生反应:![]() 。当下列所给有关量不再变化时,不能表明该反应已达平衡状态的是
。当下列所给有关量不再变化时,不能表明该反应已达平衡状态的是![]()
![]()
A.混合气体的压强B.混合气体的密度
C.混合气体的平均相对分子质量D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。(已知:装置C的作用是吸收Cl2)
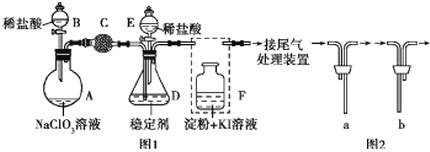
(1)仪器B的名称是________。安装F中导管时,应选用图2中的_________________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜_______________(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,NaClO2中Cl的化合价为______。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为__________。
(5)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应离子方程式为___________________。(已知:在酸性条件下SO32-被ClO3-氧化为SO42-)
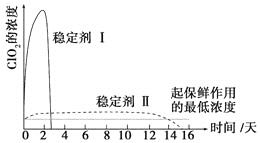
(6)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是__________,原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温恒压下,在容积可变的密闭容器中,反应2NO2(g) N2O4(g)达到平衡后,再向容器中通入一定量的NO2,又达到平衡时,N2O4的体积分数( )
A.不变B.增大C.减小D.无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:______________________。
(2)某工程师为了从使用过的腐蚀废液(主要含CuCl2、FeCl3溶液等)中回收铜,并重新获得纯净的FeCl3溶液,准备采用如图所示流程:(已知:加过量①为Fe;加过量④为稀盐酸;通入⑥为Cl2)
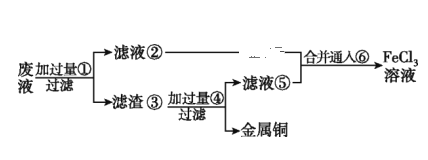
①上述实验中滤渣③的主要物质为___________________(填化学式),写出向②⑤的合并液中通入⑥的离子方程式:______________________________。
②配制并保存FeCl2溶液时,需加入铁屑,其目的是_______________________________。
③要证明FeCl3溶液是否含有Fe2+,可选择下列选项中的______________(已知:加入该物质后,生成蓝色沉淀)。
A.加入 K3[Fe(CN)6]溶液 B.加入NaOH溶液 C.加入KSCN溶液
(3)现有1.2 L含3 mol FeCl2的酸性溶液恰好与0.6 mol HIO3完全反应,还原产物为_______(填化学式,已知该物质遇淀粉溶液变蓝),该反应离子方程式为___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备 Fe(OH)2,装置如右图所示,其中电解池两极材料分别为铁和石墨,通电一段时间后,右侧玻璃管中产生大量的白色沉淀。则下列说法正确的是
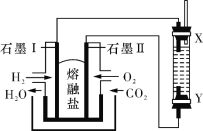
A. 石墨电极Ⅱ处的电极反应式为O2+4e-=2O2-
B. X是铁电极
C. 电解池中有1mol Fe溶解,石墨Ⅰ耗H2 22.4 L
D. 若将电池两极所通气体互换,X、Y两极材料也互换, 实验方案更合理。
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的X、Y气体充入一个密闭容器中,一定条件下发生反应并达到平衡:X(g)+Y(g) ![]() 2Z(g) ΔH<0。改变条件达到新平衡后,下列正确的是( )
2Z(g) ΔH<0。改变条件达到新平衡后,下列正确的是( )
A. 升高温度,X的体积分数减小
B. 增大压强(缩小容器体积),Z的浓度不变
C. 保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
D. 保持容器体积不变,充入一定量的Z,X的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。粗食盐中常含有少量K+、Ca2+、Mg2+、Fe3+、SO42—等杂质离子,实验室提纯NaCl的流程如下:
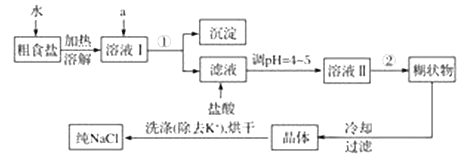
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇。
(1)在过滤过程中所需要的玻璃仪器有________________________________________。
(2)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42—,选出a所代表的试剂,按滴加顺序依次为_______(只填化学式)。
(3)用于沉淀的试剂需过量,否则不能将杂质除尽,检验过滤的滤液中是否含有Fe3+的方法__________,过滤所得沉淀需要洗涤,洗涤沉淀的方法__________________。
(4)用提纯的NaCl配制成480ml 0.2molL-1的NaCl溶液,用托盘天平称取___________ g纯的NaCl晶体,用蒸馏水在_______________中溶解,完全溶解后,全部转移至________________中,加蒸馏水至______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图曲线a表示放热反应 X(g) + Y(g)![]() Z(g) + M(g) + N(s) △H <0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
Z(g) + M(g) + N(s) △H <0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
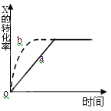
A.升高温度B.加大X的投入量C.加催化剂D.增大体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com