
科目: 来源: 题型:
【题目】凯库勒提出了有机物分子中碳原子为四价,而且可以互相结合成碳链的思想,为现代结构理论奠定了基础。1865年发表“论芳香族化合物的结构”论文,第一次提出了苯的环状结构理论。这一理论极大地促进了芳香族化学的发展和有机化学工业的进步。有关下列几种有机物叙述正确的是

A.a、d互为同分异构体,b、c互为同系物
B.a和d的二氯代物均有3种,一氯代物均有1种
C.4种有机物均能使酸性高锰酸钾溶液褪色
D.a和b中所有原子可能共平面,c和d中所有原子都不可能共平面
查看答案和解析>>
科目: 来源: 题型:
【题目】amol FeS与bmol FeO投入到VL、c mol/L的硝酸溶液中充分反应产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
( )
①(a+b)×63g ②(a+b)×189g ③(a+b)mol ④![]() mol
mol
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目: 来源: 题型:
【题目】11.2g Fe加入一定量的HNO3充分反应后,生成Fe2+、Fe3+的物质的量之比为1:4,将生成的气体与一定量的O2混合后通入水中,最后无气体剩余,则通入的氧气的物质的量是
A. 0.12mol B. 0.14mol
C. 0.2mol D. 0.13mol
【答案】B
【解析】
铁与硝酸反应生成Fe2+、Fe3+和氮的氧化物,氮的氧化物与一定量的O2混合后通入水中,最后无气体剩余,说明氮的氧化物与O2完全反应生成硝酸,铁还原硝酸的量与生成硝酸的量相同,即铁失去电子的数目与O2得到电子数目相同,据此计算。
由题意可知,铁还原硝酸的量与氮的氧化物与O2完全反应生成硝酸的量相同,即铁失去电子的数目与O2得到电子数目相同。11.2gFe的物质的量为0.2mol,Fe全部溶解,生成Fe2+和Fe3+的物质的量之比为1:4,所Fe2+的物质的量为0.04mol,Fe3+的物质的量为0.16mol,共失去电子为0.04mol×2+0.16mol×3=0.56mol,由得失电子守恒,O2得到电子的物质的量为0.56mol,所以O2的物质的量为0.56mol/4=0.14mol,故选B。
【点睛】
本题考查铁和硝酸反应的有关计算,该题的关键是在明确反应原理的基础上灵活运用电子得失守恒。
【题型】单选题
【结束】
23
【题目】10mLNO、CO2的混合气体通过足量的Na2O2后,气体的体积变为5mL(相同状况),则CO2和NO的体积比不可能为
A. 1∶1 B. 1∶2
C. 2∶1 D. 3∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】图中曲线表示短周期元素的原子序数(按递增顺序连续排列)及其常见最高化合价的关系,下列叙述不正确的是 ( )
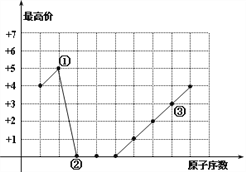
A. 单核简单离子半径大小为:②<③
B. ①、③可以按原子个数比1︰1形成化合物
C. ②、③形成的化合物是两性物质
D. ①、②形成的化合物的摩尔质量可能是44g/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】研究![]() 等大气污染气体的处理具有重要意义。
等大气污染气体的处理具有重要意义。
(1)已知:![]() ;
;![]() ;
;
则反应![]() 的
的![]() =________。
=________。
(2)一定条件下,将![]() 与
与![]() 以体积比
以体积比![]() 置于密闭容器中发生上述反应,测得上述反应平衡时
置于密闭容器中发生上述反应,测得上述反应平衡时![]() 与
与![]() 体积比为
体积比为![]() ,则平衡常数
,则平衡常数![]() =________(保留两位小数)。
=________(保留两位小数)。
(3)![]() 可用于合成甲醇,反应方程式为
可用于合成甲醇,反应方程式为![]() 。
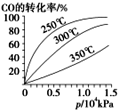
。![]() 在不同温度下的平衡转化率与压强的关系如图所示。该反应
在不同温度下的平衡转化率与压强的关系如图所示。该反应![]() ________
________![]() (填“>”或“<”)。实际生产条件控制在
(填“>”或“<”)。实际生产条件控制在![]() 、
、![]() 左右,选择此压强的理由是__________________。
左右,选择此压强的理由是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子半径依次增大,X、Y同主族,且X、Y原子序数之和是W、Z原子序数之和的2倍。m、n、p、r是由这些元素组成的二元化合物,甲、乙是其中两种元素对应的单质,n与乙在常温下均是淡黄色固体。上述物质间的转化关系如图所示(部分生成物已省略)。下列说法正确的是

A.简单离子半径大小:X>Y>Z
B.热稳定性:r>p
C.含Y元素的含氧酸一定都是强酸
D.二元化合物n 是碱性氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室探究SO2与Fe(NO3)3溶液反应的原理,装置如下图,实验中Y装置产生白色沉淀。下列说法不正确的是
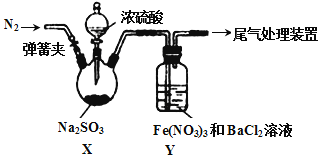
A. 滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N2
B. Y中产生的白色沉淀是BaSO4或BaSO3
C. 产生白色沉淀的原因可能是在酸性条件下SO2与NO3- 反应生成了SO42-
D. 若将Fe(NO3)3换成FeCl3,Y中也能产生白色沉淀,说明Fe3+也能将SO2氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】洁厕灵和84消毒液混合使用会发生反应:![]() ,生成有毒的氯气。NA代表阿伏加德罗常数的值,下列说法正确的是
,生成有毒的氯气。NA代表阿伏加德罗常数的值,下列说法正确的是
A.每生成![]() 氯气,转移的电子数为2NA
氯气,转移的电子数为2NA
B.![]() 含有的电子数为28NA
含有的电子数为28NA
C.![]() 溶液中含有的次氯酸根离子数为0.2NA
溶液中含有的次氯酸根离子数为0.2NA
D.将分子总数为NA的![]() 和
和![]() 的混合气体置于标准状况下,其体积约为
的混合气体置于标准状况下,其体积约为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:

(1)反应开始至2min,以气体Z表示的平均反应速率为_________.
(2)该反应的化学方程式为_________.
(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:此时体系的压强是开始时的_________倍;达平衡时,容器内混合气体的平均相对分子质量比起始投料时_________(填"增大""减小"或"相等").
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应
B.电热水器用镁棒防止内胆腐蚀,原理是牺牲阴极的阳极保护法
C.门捷列夫根据元素的性质随着相对原子质量递增呈现周期性变化规律,制出了第一张元素周期表
D.石灰乳与海水混合,过滤得![]() ,将其溶于盐酸,再蒸发结晶得到
,将其溶于盐酸,再蒸发结晶得到![]() ,电解熔融
,电解熔融![]() 可得到金属镁
可得到金属镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com