
科目: 来源: 题型:
【题目】有氯化钠和碘化钠的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为 17.55 g。
(1)原混合物中碘化钠的质量是________。
(2)原混合物中氯化钠的质量分数是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术。下列说法中不正确的是( )。
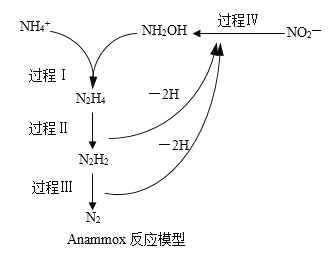
A.1mol![]() 所含的质子总数为10NA
所含的质子总数为10NA
B.联氨(N2H4)中含有极性键和非极性键
C.过程Ⅱ属于氧化反应,过程Ⅳ属于还原反应
D.过程Ⅰ中,参与反应的![]() 与NH2OH的物质的量之比为1:1
与NH2OH的物质的量之比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料![]() ,其工艺流程如图所示:
,其工艺流程如图所示:
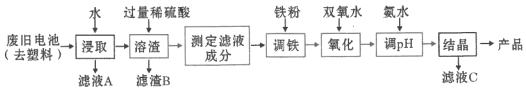
(1)碱性锌锰电池的工作原理:________![]() ________
________![]() ________
________![]() ________
________![]() ________(配平方程式),其中的电解质溶液是
________(配平方程式),其中的电解质溶液是![]() 溶液。滤液
溶液。滤液![]() 中主要溶质的电子式为______。
中主要溶质的电子式为______。
(2)已知![]() 中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为________。
中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为________。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将![]() 价锰的化合物全部还原成
价锰的化合物全部还原成![]() ,写出该反应的离子方程式________。
,写出该反应的离子方程式________。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式![]() 相符合。
相符合。
①写出“调铁”工序中可能发生反应的离子方程式________,________。
②若“测定滤液成分”结果为![]() ,
,![]() ,滤液体积为
,滤液体积为![]() ,“调铁”工序中,需加入的铁粉质量为________
,“调铁”工序中,需加入的铁粉质量为________![]() (忽略溶液体积变化,用含
(忽略溶液体积变化,用含![]() 、
、![]() 的代数式表示)。
的代数式表示)。
(5)在“氧化”工序中,加入双氧水的目的是把![]() 氧化为
氧化为![]() ;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是________。
;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是________。
(6)从滤液![]() 中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为________。
中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对于硝酸的认识,不正确的是![]()
![]()
A. 浓硝酸在见光或受热时会发生分解 B. 久置的浓硝酸会变为稀硝酸
C. 金属与硝酸反应不产生氢气 D. 稀硝酸与铁反应而浓硝酸不与铁反应
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制取氯气,将多余的氯气用100 mL 1.7mol/L的NaOH溶液完全吸收。对吸收后的溶液进行分析化验,测知c(OH-)=0.1mol/L (不考虑反应前后溶液的体积变化) 。ClO-和ClO3-的物质的量浓度之比为5∶1。请回答:
(1)吸收氯气消耗的NaOH的物质的量为_______________mol。
(2)被氧化的氯气的物质的量为_______________mol,被还原的氯气的物质的量为 _______________mol。
(3)若采用二氧化锰和浓盐酸共热的方法制氯气,制备尾气中的氯气所消耗的二氧化锰的质量为_______________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉碘化钾试纸、湿润的红色纸条。
已知常温下浓盐酸与高锰酸钾能反应生成氯气;
可选择的试剂有:大理石、碳酸钠粉末、浓盐酸、稀硝酸、硅酸钠溶液。
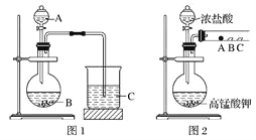
(1)甲同学实验中(图1):
①从给出试剂中选出最佳物质(填化学式):A________,B________。
②烧杯C中发生反应的离子方程式为__________________________。
(2)乙同学实验中(图2):
①写出A处反应的离子方程式________________________。
②B处实验现象是________________________。
③若高锰酸钾的还原产物为Mn2+,当有0.04 mol高锰酸钾参加反应时,则可生成标准状况下的氯气的体积为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物M(C16H14O2)是一种香料,工业上常利用烃A和甲苯为主要原料,按下列路线合成:

已知:①气态烃A在标准状况下的密度是1.25g·L-1;
②醛在碱性溶液中能发生羟醛缩合反应,再脱水生成不饱和醛:
![]() 请回答下列问题:
请回答下列问题:
(1)F的名称是_______________;M中含有的官能团名称是________________。
(2)写出B→C的化学方程式_______________________________________。
(3)D→E的反应类型是___________________;K的结构简式是______________________。
(4)同时满足下列条件的G的同分异构体有________________种(不考虑立体异构)。
①含有碳碳三键
②遇FeCl3溶液发生显色反应
其中核磁共振氢谱为四组峰的结构简式为______________________。
(5)以乙醛为起始原料,选用必要的无机试剂合成1-丁烯,写出合成路线________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各装置不能达到实验目的是
A.利用①吸收多余的氨气
B.装置②可用于除去Cl2中的HCl
C.装置③可用于干燥氨气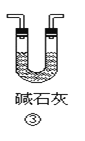
D.装置④可用于排空气法收集H2、CO2、Cl2、HCl等气体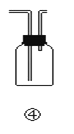
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是
A.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
B.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-=CO2↑+H2O
C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将充满NO2和O2的试管倒立于水槽中,充分反应后,剩余气体的体积为原混合气体体积的![]() ,则原混合气体中NO2和O2的体积之比是
,则原混合气体中NO2和O2的体积之比是
A.8:1B.7:3C.1:7D.4:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com