
科目: 来源: 题型:
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图, 图中分液制斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
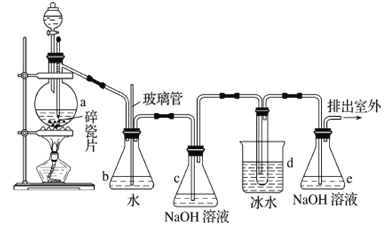
己知:CH3CH2OH![]() CH2=CH2↑+H2O;2CH3CH2OH
CH2=CH2↑+H2O;2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)实验中应迅速将温度升卨到170℃左右的原因是______________________________。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,
请写出发生堵塞时瓶b中的现象:①_______________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是②_______________________________________________;安全瓶b还可以起到的作用是③__________________。
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是_______________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正确情况下超过许多,如果装罝的气密性没有问题,试分析可能的原因:______________、______________(写出两条即可)。
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为___________,要进一步提纯,下列操作中必需的是_____________ (填字母)。
A.重结晶 B.过滤 C.萃取 D.蒸馏
(6)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则 此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】处理超标电镀废水,使其NaCN含量低于0.5 mg/L,即可达到排放标准,反应分两步进行。第一步NaCN与NaClO反应,生成NaOCN和NaCl。第二步NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN是弱酸,易挥发,有剧毒;HCN、HOCN中N元素的化合价相同。下列说法正确的是
A. 处理NaCN超标电镀废水的过程中无元素化合价的改变
B. 第一步反应溶液应调节为酸性,可避免生成有毒物质HCN
C. 第二步发生的反应为2OCN- + 3ClO- ![]() 2CO2↑ + CO32 + 3Cl- + N2↑
2CO2↑ + CO32 + 3Cl- + N2↑
D. 处理100 m3含NaCN 10.3 mg/L的废水实际至少需要50 mol NaClO
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。

步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收。2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水。
步骤二:通过仪器分析得知X的相对分子质量为106。
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3。如图Ⅰ。
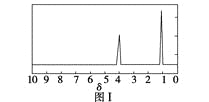
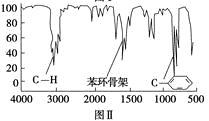
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ。
试填空:
(1)X的分子式为________;X的名称为 。
(2)步骤二中的仪器分析方法称为________。
(3)写出X与足量浓硝酸和浓硫酸混合物反应的化学方程式: 。
(4)写出X符合下列条件的同分异构体结构简式 。
①芳香烃 ②苯环上一氯代物有三种
(5)X以醋酸为溶剂在催化剂作用下用氧气氧化得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:25 ℃时0.25 g、50 ℃时0.97 g、95 ℃时7.17 g。得到的粗产品中有部分不溶性杂质,请简述实验室中提纯PTA的实验方案: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】他米巴罗汀是一种对白血病、阿尔茨海默症等疾病具有较好治疗效果的药物,其一种合成路线:
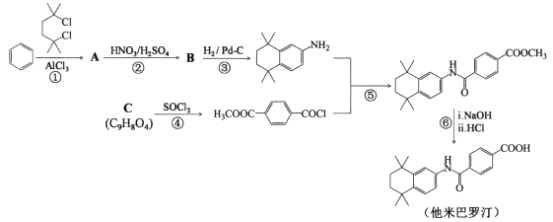
回答下列问题:
(1)A的结构简式是_________,C中含氧官能团的名称是_________
(2)①和③的反应类型分别是_________
(3)下列说法正确的是_________(填标号)。
a.A为苯的同系物b.B的一氯代物有5种
c.1molC最多可与2molNaOH反应d.弱碱性条件有利于反应⑤进行
(4)草酰氯![]() 与乙二胺(
与乙二胺(![]() )反应可得到一种六元环状化合物,该反应的化学方程式为_________
)反应可得到一种六元环状化合物,该反应的化学方程式为_________
(5)化合物W与C互为同分异构体,且满足下列条件:①属于芳香族化合物且能与NaHCO3反应:②能发生银镜反应;③酸性条件下可发生水解反应,其产物能之一与FeCl3发生显色反应,则W共有_________种,其中一种核磁共振氢谱为1:2:2:2:1,其结构简式为__________。
(6)参照上述合成路线,设计由苯和1,3-丁二烯合成![]() 的路线(其它无机试剂任选)。__________
的路线(其它无机试剂任选)。__________
查看答案和解析>>
科目: 来源: 题型:
【题目】钴及其化合物有着广泛的应用前景。回答下列问题:
(1)基态Co原子的核外电子排布式为_________.
(2)以无水乙醇作溶剂,Co(NO3)2可与某多齿配体结合形成具有催化活性的配合物,其结构简式如图所示。
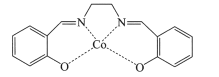
①配合物中提供孤对电子的原子是_________(填元素符号);
②该多齿配体中所含元素电负性由大到小的顺序为__________(填元素符号):
③下列化合物与上述配合物中C和N原子的杂化类型均相同的是__________(填标号)。
A.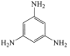 B.
B.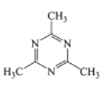 C.
C.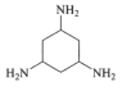 D.
D.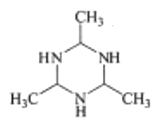
(3)亚硝酸钴钠可与K+结合形成K2Na[Co(NO2)6],从而实现对K+的定量测定。
①K2Na[Co(NO2)6]中存在的化学键类型有_________(填标号);
A.金属键 B.离子键 C.极性共价键 D.配位键
②与亚硝酸根互为等电子体的化合物有_________(写一种)。
(4)Co与Ca属于同一周期,且最外层电子数相同,但金属Co的熔点、沸点均比金属Ca的高,原因是____。
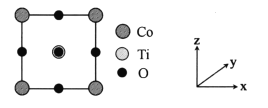
(5)某种铁酸钴(CoTiO3)晶胞沿x、y或z轴任意一个方向的投影如下图所示。晶胞中Co处于各顶角位置,则O处于_________位置,与Co紧邻的O的个数为_________。若晶胞中Co与O的距离为anm,阿伏加德罗常数的值为NA,该晶体的密度为_________g.cm-3(列出计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】以CH4、CO2为原料合成乙酸,是综合开发温室气体资源的新方向。
I.CH4.CO2催化重整间接制乙酸
CH4、CO2催化重整制合成气,再利用合成气制乙酸,涉及的反应如下:
反应l:CH4(g)+CO2(g) 2H2(g)+2CO(g)△H
反应2:2H2(g)+CO(g) CH3OH(g)△H=-90.9kJ·mol-1
反应3:CH3OH(g)+CO(g) CH3COOH(g)△H=-118.2kJ·mol-1
(1)已知:CH4(g)+CO2(g) CH3COOH(g)△H=+37.9kJ·mol-1则“反应l”的△H=_________
(2)“反应1”的化学反应速率v=k[![]() ]m·[
]m·[![]() ]n,k为速率常数。1123K和1173K时,分别保持
]n,k为速率常数。1123K和1173K时,分别保持![]() 或
或![]() 不变,测得速率v与
不变,测得速率v与![]() 、
、![]() 的关系如图所示:
的关系如图所示:

①由图可知,下列叙述正确的是_________(填标号)。
A.当10kPa≤![]() ≤25kPa时,m=l
≤25kPa时,m=l
B.其他条件不变,增大![]() ,速率v不一定增大
,速率v不一定增大
C.a、b、c三点速率常数的大小关系为:ka>kb>kc
②若初始时按n(CH4):n(CO2)=1:1进气,且Kb=1.3×10-2mol·g-1·s-1·Kpa-2,则b点的化学反应速率v=_________mol·g-1·s-1。
(3)向盛有催化剂的刚性容器中通入等物质的量的CH4(g)和CO2(g),发生“反应1”。在923K和1173K时,CH4(g)的转化率(α)与时间(t)的关系如图所示。

923K时,CH4(g)的平衡转化率α=_________,若平衡时体系的总压强为p0,平衡常数K923K=____(用含有p0的代数式表示)。
II.CH4、CO2两步法制乙酸
(4)反应CH4(g)+CO2(g)CH3COOH(g)不能自发进行。将该反应拆分成两个连续的步骤进行,可在较温和的条件下实现上述转化,具体过程:

①第二步反应的化学方程式为_________
②为增大CH3COOH的平衡产率,从温度角度考虑,第一步反应在高温下进行,第二步反应在_________进行;从H2浓度的角度考虑,应采取的措施是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2是生产、生活、实验中常用的试剂。
I.工业上制备H2O2的流程如下:

(1)“转化”中反应的化学方程式为_________:“低温放置”的目的是_________
(2)图甲为“减压蒸馏”的部分装置,该装置由克氏蒸馏头和_________(填仪器名称)组成。
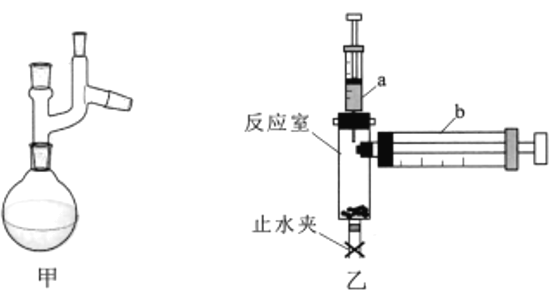
lI.实验小组利用图乙装置测定阿伏加德罗常数(NA)
(3)实验准备
①H2O2溶液浓度标定。可选用_________(填标号)试剂对H2O2溶液进行滴定,测定其浓度。
A.H2C2O4B.KMnO4C.淀粉KI
②装置气密性检查。打开止水夹,将注射器b的活塞推至底部,拉动注射器a活塞吸入10mL空气,关闭止水夹。向下推动注射器a活塞至底,当观察到注射器b的现象为_________,说明装置的气密性良好。
(4)测定过程
①在反应室中加入适量MnO2,将注射器b活塞推至底部,关闭止水夹。用注射器a准确抽取cmol/LH2O2溶液VlmL,缓慢地注入反应室后,固定注射器a活塞。
②反应结束后,待反应体系处于_________状态时,读取注射器b的气体体积为V2mL,则产生O2的体积为____mL。
③设室温下O2的密度为ρg/L,一个O2实际质量为mg,则NA=____(用含ρ等字母的代数式表示)。
(5)该实验利用H2O2作为生氧剂的优点有_________(写两条)。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,向50mL浓度均为l.0mol/L的醋酸和醋酸钠混合溶液中,缓慢滴加1.0mol/L的NaOH溶液,所得溶液的pH变化情况如图所示(已知:25℃时,Ka(CH3COOH)=1.8×10-5)。下列叙述错误的是
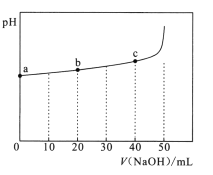
A.a点溶液中,c(H+)约为![]()
B.b点溶液中,![]()
C.V(NaOH)≤50mL时,随V(NaOH)增大,溶液中离子总浓度增大
D.从a到c的过程中,溶液中 不变
不变
查看答案和解析>>
科目: 来源: 题型:
【题目】一种新型电池的工作原理如图所示。该电池工作时,下列说法错误的是
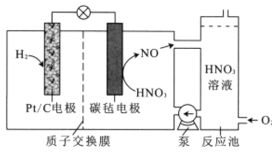
A.Pt/C电极为负极,质子通过交换膜从负极区移向正极区
B.正极的电极反应为NO3-+4H+3e-=NO↑+2H2O
C.反应池中发生总反应4NO+3O2+2H2O=4HNO3,实现HNO3再生
D.理论上,当消耗22.4L(标准状况下)H2时,会消耗1molO2
查看答案和解析>>
科目: 来源: 题型:
【题目】硅是制作光伏电池的关键材料。在Si晶体中掺杂不同种类的元素,可形成多电子的n型或缺电子的p型半导体。n型和p型半导体相互叠加形成p-n结,此时自由电子发生扩散运动,在交界面处形成电场。下列说法正确的是

A.1molSi晶体中含有的Si-Si键数目为4NA
B.若在Si晶体中掺入P元素,可得n型半导体
C.p-n结中,n型一侧带负电,p型一侧带正电
D.光伏电池的能量转化形式为:光能→化学能→电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com