
科目: 来源: 题型:
【题目】(1)科研人员设想用如图所示装置生产硫酸。
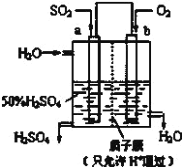
①上述生产硫酸的总反应方程式为_____,b 是_____极,b 电极反应式为______________,生产过程中H+向_____(填 a 或 b)电极区域运动。
②该小组同学反思原电池的原理,其中观点正确的是_____(填字母)。
A.原电池反应的过程中可能没有电子发生转移
B.原申池装置一定需要2个活泼性不同的金属电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
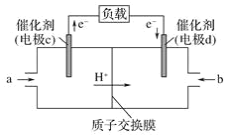
(2)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜(只允许H+通过)质子交换膜左右两侧的溶液均为1L 2mol·L-1H2SO4溶液。燃料电池的结构示意图如:电池总反应为2CH3OH+3O2=2CO2+4H2O,c电极为_____(填“正极”或“负极”),c电极反应方程式为___________________________。当电池中有1mol e-发生转移时左右两侧溶液的质量之差为______g (假设反应物耗尽,忽略气体的溶解)。
查看答案和解析>>
科目: 来源: 题型:
【题目】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图示,下列与此原理有关说法错误的是
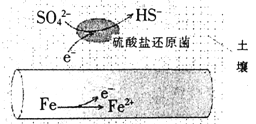
A. 正极反应为:SO42-+5H2O+8e-=HS-+9OH-
B. 输送暖气的管道不易发生此类腐蚀
C. 这种情况下,Fe腐蚀的最终产物为Fe2O3·xH2O
D. 管道上刷富锌油漆可以延缓管道的腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】宝鸡被誉为“青铜器之乡”,出土了大盂鼎、毛公鼎、散氏盘等五万余件青铜器。研究青铜器(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是

A. 青铜器发生电化学腐蚀,图中c作负极,被氧化
B. 正极发生的电极反应为O2+ 4e-+2H2O=4OH-
C. 环境中的Cl- 与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH-+Cl-=Cu2 (OH)3Cl↓
D. 若生成0.2 mol Cu2(OH)3Cl,则理论上消耗的O2体积为4.48L
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )

A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
查看答案和解析>>
科目: 来源: 题型:
【题目】处理烟气中的SO2,可以采用碱吸-电解法,其流程如图:模拟过程Ⅱ如图,下列推断正确的是( )
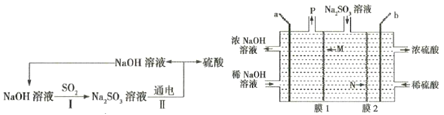
A.膜1为阳离子交换膜,膜2为阴离子交换膜
B.SO2是含有极性键的极性分子
C.a极的电极反应式为2H2O-4e-=4H++O2↑
D.若收集22.4 L的P(标准状况下),则有2 mol N离子移向右室
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。下列有关说法正确的是
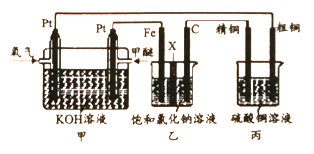
A. 反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B. 乙装置中铁电极为阴极,电极反应式为Fe-2e-= Fe2+
C. 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
D. 通入氧气的一极为正极,发生的电极反应为O2 - 4e- + 2H2O = 4OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍。下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A. 电解后,电解槽底部的阳极泥中只有金属Pt
B. 电解过程中,电解质溶液的质量可能保持不变
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 阳极发生氧化反应,其电极反应式:Ni2++2e-![]() Ni
Ni
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中Cl-的物质的量浓度最大的是
A. 150 mL1 mol/L NaCl溶液 B. 50 mL2mol/L NH4Cl溶液
C. 150 mL 0.5 mol/L CaCl2溶液 D. 50 mL l mol/L AlCl3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】中国人自古就有泡药酒的习惯。药酒多选用50-60度的白酒,将中药材浸泡在酒中,经过一段时间,中药材中的有效成分(主要是有机物)溶解在酒中,此时即可过滤去渣后饮用。泡药酒的原理属于

A.萃取B.结晶C.干燥D.置换
查看答案和解析>>
科目: 来源: 题型:
【题目】MnO2和Zn是制造普通干电池的重要原料,现用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制备MnO2和Zn的工艺流程如图。下列说法错误的是( )

A.干电池是一种将化学能转变为电能的装置
B.原料硫酸可以循环使用,且可用盐酸代替硫酸进行酸溶
C.酸溶时ZnS作还原剂,操作1为过滤
D.通电电解时MnO2在阳极处生成,电极反应为:Mn2+-2e-+2H2O=MnO2+4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com