
科目: 来源: 题型:
【题目】某混合气体由一种气态烷烃和一种气态烯烃(含一个双键)组成,在同温同压下,混合气体对氢气的相对密度13,在标准状况下,将56L混合气体通入足量的溴水中,溴水的质量增重35g。
(1)计算确定混合气体中烃的化学式_____。
(2)混合气体中两种烃的物质的量之比_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其实验装置如图所示。其实验操作为预先使棉花团浸透乙醇,并按照图示安装好装置;在铜丝的中间部分加热,片刻后开始(间歇性)鼓入空气,即可观察到明显的实验现象。
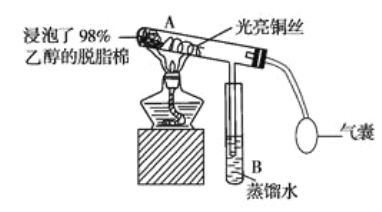
请回答以下问题:
(1)被加热的铜丝处发生反应的化学方程式为________________________________。
(2)从A管中可观察到____________的实验现象。从中可认识到在该实验过程中,催化剂参加了化学反应,还可认识到催化剂起催化作用时需要一定的_______________________。
(3)实验一段时间后,如果撤掉酒精灯,反应还能否继续进行?__________,原受热部分的铜丝有什么现象?____________,产生这种现象是因为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是
A. AgNO3 B. Na2SO4 C. CuCl2 D. KCl
查看答案和解析>>
科目: 来源: 题型:
【题目】下列不能用勒夏特列原理解释的事实是
A. 红棕色的NO2加压后颜色先变深后变浅
B. 氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C. 黄绿色的氯水光照后颜色变浅
D. 合成氨工业使用高压以提高氨的产量
查看答案和解析>>
科目: 来源: 题型:
【题目】为了检验淀粉的水解情况,某同学设计了以下三个实验方案,并根据实验现象,得出相应的结论:
甲:淀粉液![]() 水解液
水解液![]() 溶液变蓝 实验结论:淀粉未水解。
溶液变蓝 实验结论:淀粉未水解。
乙:淀粉液![]() 水解液
水解液![]() 无银镜现象 实验结论:淀粉未水解。
无银镜现象 实验结论:淀粉未水解。
丙:淀粉液![]() 水解液NaOH溶液,中和液
水解液NaOH溶液,中和液![]() 生成银镜 实验结论:淀粉完全水解。
生成银镜 实验结论:淀粉完全水解。
根据上述三个方案的操作及现象,首先回答结论是否正确,然后简要说明理由。如果三个结论均不正确,请另设计一个方案来证明淀粉已经水解完全了。
(1)方案甲:____________。
(2)方案乙:________。
(3)方案丙:___________。
(4)你的方案:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学课外小组查阅资料知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成溴苯和溴化氢,此反应为放热反应。他们设计了下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中。

请回答下列问题:
(1)装置A中发生反应的化学方程式是______________________________。
(2)装置C中看到的现象是__________________,证明_________。
(3)装置B内盛有四氯化碳,实验中观察到的现象是_____________,原因是____。
(4)如果没有B装置,将A、C直接相连,你认为是否妥当(填“是”或“否”)________,理由是_________________________________。
(5)实验完毕后将A试管中的液体倒在装有冷水的烧杯中,烧杯____层(填“上”或“下”)为溴苯,这说明溴苯____________且____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知甲苯(![]() )能使酸性KMnO4溶液退色。某有机物的结构简式为
)能使酸性KMnO4溶液退色。某有机物的结构简式为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.该有机物使溴水褪色和在催化剂作用下与液溴反应原理一样
B.能用酸性KMnO4溶液判断分子中存在碳碳双键
C.该有机物在一定条件下与浓硝酸发生反应生成的一硝基取代物可能有3种
D.1 mol该有机物在一定条件下最多与4 mol H2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】用间接电化学法可对大气污染物 NO 进行无害化处理,其工作原理如图所示。下列说法正确的是 ( )
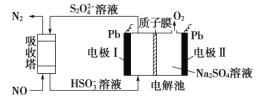
A.电极I为阴极,电极反应式为2H2O+2e- = 2OH-+H2↑
B.电解时 H+ 由电极II向电极I迁移
C.吸收塔中的反应为2NO+2S2O![]() +2H2O =N2 +4HSO
+2H2O =N2 +4HSO![]()
D.每处理1mo1NO,可同时得到32gO2
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列物质变化,只与范德华力有关的是___。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:
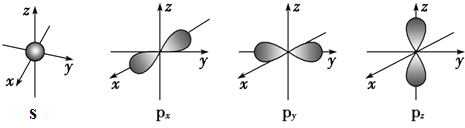
请回答下列问题:
s电子的原子轨道呈__形,每个s能级有__个原子轨道;p电子的原子轨道呈___形,每个p能级有___个原子轨道.
(3)Na、Mg、Al第一电离能的由大到小的顺序:___。
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。

根据信息回答下列问题:
(1)周期表中基态Ga原子的电子排布式为___。
(2)Fe元素位于周期表的___分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为___。
(3)已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为___和___(填化学式)。在CO、CH3OH中,碳原子采取sp3杂化的分子有___。
(4)根据VSEPR理论预测ED4-离子的空间构型为___。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子有__(任写2种化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com